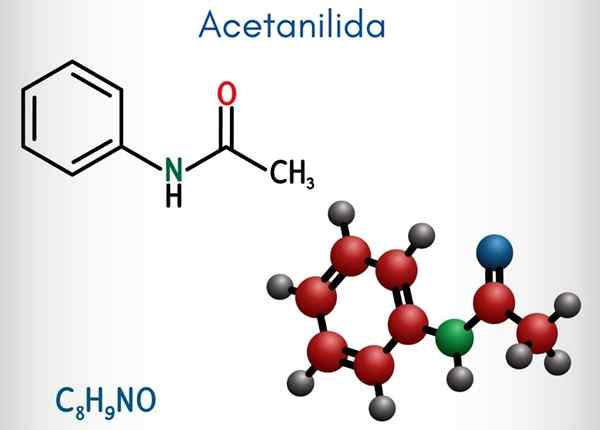
Acetanylide (C8H9NO)
- 2585
- 515
- Ismael Turner
Apa itu acetanylide?
The acetanylide (C8H9Tidak) ia adalah amida aromatik yang menerima beberapa nama tambahan: n-asetilarilamine, n-feenilacetamide dan atethanil. Ia dibentangkan sebagai tandas pepejal dalam bentuk serpihan, sifat kimianya adalah amida, dan oleh itu ia dapat membentuk gas mudah terbakar ketika bertindak balas dengan ejen pengurangan yang kuat.
Di samping itu, ia adalah asas yang lemah, dapat bertindak balas dengan agen dehidrasi seperti p2Sama ada5 Berasal dari nitril. Didapati bahawa acetanylide mempunyai tindakan analgesik dan antipyretik, dan digunakan pada tahun 1886 dengan nama Antifebrin oleh a. Cahn dan p. Hepp.
Pada tahun 1899, asid acetylsalicylic (aspirin) diperkenalkan ke pasaran, yang mempunyai tindakan terapeutik yang sama seperti asetanilida. Apabila penggunaan acetanylide berkaitan dengan penampilan sianosis pada pesakit - akibat methemoglobinemia yang disebabkan oleh acetanylide - penggunaannya dibuang.
Selanjutnya ia ditubuhkan bahawa tindakan analgesik dan antipyretik acetanylide tinggal dalam metabolit paracetamol yang dipanggil ini (acetoaminophen), yang tidak mempunyai kesan toksiknya, seperti yang dicadangkan oleh Axelrod dan Brodie yang dicadangkan.
Struktur kimia

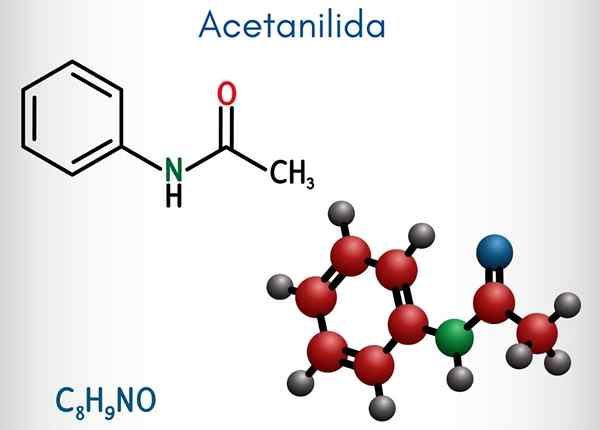
Di bahagian atas, struktur kimia acetanylide diwakili. Di sebelah kanan adalah cincin aromatik heksagon benzena (dengan garis putus -putus), dan kiri adalah sebab mengapa kompaun terdiri daripada amida aromatik: kumpulan acetamide (hncoch3).
Kumpulan acetamide memberikan cincin benzena watak kutub yang lebih besar; Iaitu, buat momen dipole dalam molekul atetanylide.
Kerana? Kerana nitrogen lebih banyak elektronegatif daripada mana -mana atom karbon cincin dan juga dikaitkan dengan kumpulan acyl, yang atom atau juga menarik kepadatan elektronik.
Ia boleh melayani anda: urethane: struktur, sifat, mendapatkan, menggunakanSebaliknya, hampir keseluruhan struktur molekul acetanylide terletak pada satah yang sama kerana hibridisasi SP2 atom yang mengarangnya.
Terdapat pengecualian yang dikaitkan dengan kumpulan -ch3, Atom hidrogen yang membentuk simpul tetrahedron (sfera putih hujung kiri meninggalkan pesawat).
Struktur resonans dan interaksi intermolecular
Tork bersendirian tanpa berkongsi atom N beredar melalui sistem π cincin aromatik, yang berasal dari beberapa struktur resonans. Walau bagaimanapun, salah satu struktur ini berakhir dengan beban negatif dalam atom O (lebih banyak elektronegatif) dan beban positif dalam atom n.
Oleh itu, terdapat struktur resonans di mana beban negatif bergerak di cincin, dan satu lagi di mana ia berada di atom atau. Akibat daripada "asimetri elektronik" ini, yang berasal dari tangan asimetri molekul-, acetanylide berinteraksi secara intermolecularly oleh daya dipole-dipolo.
Walau bagaimanapun, interaksi hidrogen jambatan (n-h-o- ...) antara dua molekul asetanylida adalah, sebenarnya, daya utama dalam struktur kristalnya.
Dengan cara ini, kristal acetanylide terdiri daripada sel -sel unit ortorrhrombik lapan molekul berorientasikan dengan bentuk "pita rata" oleh jambatan hidrogen mereka.
Di atas boleh digambarkan jika molekul acetanylide diletakkan di atas yang lain, selari. Jadi, seperti kumpulan HNCOCH3 Mereka bertindih dengan jauh, mereka membentuk jambatan hidrogen.
Di samping itu, antara kedua -dua molekul ini juga boleh "dicuri" yang ketiga, tetapi dengan cincin aromatiknya menunjuk ke arah yang bertentangan.
Boleh melayani anda: bromotimol biruSifat kimia acetanylide
 Penampilan Rayuan
Penampilan Rayuan Berat molekul
135,166 g/mol.
Penerangan Kimia
Pepejal putih atau kelabu. Bentuk serpihan putih terang atau serbuk putih kristal.
Bau
Lavatory.
Rasa
Sedikit pedas.
Takat didih
304 ºC hingga 760 mmHg (579 ºF pada 760 mmHg).
Takat lebur
114.3 ºC (237.7 ºF).
Flash atau mudah terbakar
169 ºC (337 ºF). Pengukuran dibuat dalam kaca terbuka.
Ketumpatan
1,219 mg/ml pada suhu 15 ° C (1,219 mg/ml pada 59 ºF)
Ketumpatan wap
4.65 dengan hubungan udara.
Tekanan wap
1 mmHg pada 237 ºF, 1.22 × 10-3 mmHg pada 25 ºC, 2A pada 20 ° C.
Kestabilan
Ia menderita semula bahan kimia apabila terdedah kepada cahaya ultraviolet. Bagaimana struktur berubah? Kumpulan asetil membentuk pautan baru di gelanggang di kedudukan ortho dan untuk. Di samping itu, ia stabil di udara dan tidak serasi dengan ejen pengoksidaan yang kuat, kaustik dan alkali.
Turun naik
Secara tidak menentu pada 95 ºC.
Diri sendiri
1004 ºF.
Penguraian
Ia terurai apabila dipanaskan, memancarkan asap yang sangat toksik.
Ph
5 - 7 (10 g/L H2Atau 25 ºC)
Kelarutan
- Di dalam air: 6.93 × 103 mg/ml pada 25 ° C.
- 1 g Kelarutan acetanylide dalam cecair yang berbeza: Dalam 3.4 ml alkohol, 20 ml air mendidih, 3 ml metanol, 4 ml aseton, 0.6 ml alkohol mendidih, 3.7 ml kloroform, 5 ml gliecerol, 8 ml dari Dioxan, 47 ml benzena dan 18 eter. Hidrat kloral meningkatkan kelarutan acetanilide di dalam air.
Sintesis
Ia disintesis dengan bertindak balas anhidrida asetik dengan acetanylide. Reaksi ini muncul dalam banyak teks kimia organik (Vogel, 1959):
C6H5NH2 + (Ch3Co)2O => c6H5NHCOCH3 + Ch3COOH
Ia boleh melayani anda: borax: sejarah, struktur, sifat, kegunaan, sintesis, risikoAplikasi
- Ia adalah agen inhibitor proses penguraian hidrogen peroksida (hidrogen peroksida).
- Menstabilkan varnis ester selulosa.
- Campur tangan sebagai perantara dalam percepatan pengeluaran getah. Begitu juga, perantara dalam sintesis beberapa pewarna dan camphor.
- Ia bertindak sebagai pendahulu dalam sintesis penisilin.
- Ia digunakan dalam pengeluaran 4-acetamidefonilbenzene chloride. Acetanylide bertindak balas dengan asid chlorosulfonic (HSO3Cl), dengan itu menghasilkan klorida 4-aminosulfonilbenzene. Ini bertindak balas dengan ammonium atau amina organik utama untuk membentuk sulfonamida.
- Ia digunakan secara eksperimen pada abad kesembilan belas dalam perkembangan fotografi.
- Acetanylide digunakan sebagai penanda aliran elektroosmotik (EOF) dalam elektroforesis kapilari untuk mengkaji hubungan antara ubat dan protein.
- Baru. Acetanylide menyertai kedudukan 3 cincin pirimidin.
- Hasil eksperimen menunjukkan pengurangan replikasi genom virus, tanpa mengira genotip virus.
- Sebelum mengenal pasti ketoksikan acetanylide, ia digunakan sebagai analgesik dan antipyretik dari tahun 1886. Seterusnya (1891), ia digunakan dalam rawatan bronkitis kronik dan akut oleh Grün.