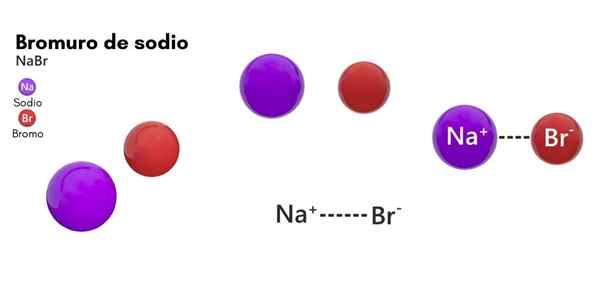
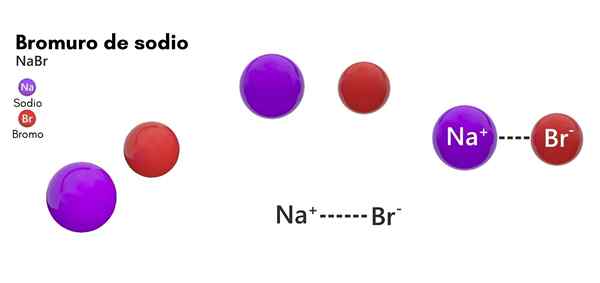
Natrium Bromide (NABR)
- 4184
- 561
- Kerry Schmitt
Apa itu natrium bromida?
Dia Natrium bromida Ia adalah spesies kimia yang dimiliki oleh garam asal bukan organik. Strukturnya terdiri daripada halogen bromik dan elemen natrium logam dalam 1: 1. Formula kimianya adalah Nabab dan berada dalam keadaan agregasi pepejal dalam keadaan suhu standard (25 ° C dan 1 atm).
Biasanya ia dapat diperhatikan sebagai debu putih, dan dianggap sebagai sebatian jenis kristal yang juga menunjukkan tingkah laku hygroscopic; iaitu, ia mempunyai keupayaan untuk menyerap kelembapan dari persekitarannya.
Begitu juga, natrium bromida mempunyai ciri -ciri fizikal yang sangat mirip dengan sebatian ionik lain logam yang sama: natrium klorida. Klorida ini diwakili sebagai NaCl, yang lebih dikenali sebagai garam atau garam meja biasa.
Ia mempunyai sejumlah besar kegunaan dalam bidang sains yang berlainan; Sebagai contoh, ia digunakan dalam pengeluaran pelbagai jenis ubat (sedatif, hipnotik, antikonvulsif, antara lain), seperti dalam sintesis organik dan juga dalam aplikasi fotografi.
Struktur kimia
Natrium bromida dibentangkan dalam fasa pepejal dan, seperti garam lain yang tidak organik, ia mempunyai penyesuaian struktur kristal.
Molekul kristal ini, yang dibentuk oleh bromin dan salah satu hidrogen, mempunyai pengesahan padu yang berpusat pada wajah, seperti garam jenis haloid logam yang sama (NAI, NAF dan NaCl).
Pengaturan molekul ini membentuk asas struktur sebatian banyak, di mana perintah itu dijalankan supaya setiap ion dikekalkan di tengah -tengah angka octahedral, seperti yang ditunjukkan dalam imej berikut.
Boleh melayani anda: asid fosforus (H3PO3)
Dalam kaca jenis ini, anda dapat melihat bagaimana setiap ion mempunyai di sekelilingnya enam ion lain - yang mempunyai caj elektrik yang bertentangan - yang terletak di hujung angka octahedral.
Begitu juga, struktur bahan ionik ini menunjukkan bahawa ia mempunyai titik lebur yang tinggi kira -kira 747 ° C, secara komersil dalam dua bentuknya: spesies anhidrat (tanpa molekul air) dan spesies dihidrasi (dengan dua molekul air dalam formula strukturnya (NABR · 2H2O)), yang mana penggabungannya berbeza.
Sintesis kimia
Natrium bromida berasal dari tindak balas kimia yang berlaku antara hidrogen bromida (BRH, halida hidrogen dalam fasa gas) dan natrium hidroksida (NaOH, asas yang kuat dalam fasa pepejal dan dengan sifat hygroscopic).
Dengan cara ini ia dihasilkan secara komersil, menambah lebihan bromin kepada penyelesaian NaOH. Oleh itu, campuran bromida/bromin terbentuk. Selanjutnya, produk yang dihasilkan tertakluk kepada penyejatan sehingga ia kering, dan dirawat dengan karbon untuk menghasilkan reaksi bromat ion (bro3-) ke ion bromida (br-).
Peneutralan
Begitu juga, garam tak organik ini juga boleh berlaku melalui tindak balas peneutralan natrium karbonat (NA2Co3) Dengan asid bromik (HBRO3), mengikuti prosedur yang sama yang dinyatakan di atas.
Melalui sintesis bahan ini dapat dihasilkan melalui tindak balas antara besi dengan bromin dan air. Sebagai produk tindak balas ini, spesies bromida ferus -pheric berasal.
Boleh melayani anda: alkoholSeterusnya, spesies ini dibentuk (diwakili sebagai Februari2/Februari3) dibubarkan di dalam air dan sejumlah natrium karbonat ditambah. Akhirnya, penyelesaian ditapis dan melalui proses penyejatan untuk mendapatkan natrium bromida akhirnya.
Sifat natrium bromida
- Biasanya dalam keadaan agregasi pepejal, dalam bentuk habuk putih.
- Ia mempunyai struktur kristal, dengan susunan molekul dalam bentuk kiub yang berpusat di wajah.
- Titik lebur bahan ini adalah kira -kira 747 ° C untuk bentuk anhydrous dan 36 ° C untuk bentuk dihydrate, menyampaikan penguraian sebelum ia cair.
- Ia terdiri daripada ion natrium (na+) dan ion bromida (br-), dengan jisim molar atau berat molekul 102.89 g/mol.
- Titik mendidihnya agak tinggi, memerhatikan 1390 ° C (bersamaan dengan 2530 ° F atau 1660 k).
- Kelarutan spesies ini sekitar 94.32 g/100 ml di dalam air pada 25 ° C, meningkat apabila suhu meningkat.
- Dengan menjalani pemanasan ke titik di mana ia rosak, bahan ini mengeluarkan gas bromin dan natrium oksida dianggap beracun.
- Ketumpatan bentuk anhydrous natrium bromida adalah 3.21 g/cm3, Walaupun sebatian dihidrasi adalah 2.18 g/cm3.
- Kelarutannya dalam alkohol dianggap sederhana, seperti pelarut lain seperti piridin, ammonia dan hidraksi.
- Ia memberikan ketidakpuasan terhadap asetonitril dan aseton.
Penggunaan/aplikasi
- Di kawasan perubatan ia digunakan sebagai ubat untuk sejumlah besar keadaan yang berasal dari sawan dan sebagai terapi untuk mencegah gambar epilepsi pada pesakit dengan sindrom Wolf-Hirschhorn, serta rawatan sedatif dan hipnosis.
Ia boleh melayani anda: asid bromik (HBRO3): sifat, risiko dan kegunaan- Dalam perubatan veterinar ia digunakan dalam anjing yang mengalami gangguan convulsif kerana kesan sampingan ubat -ubatan seperti primidone atau phenobarbital.
- Dalam bidang industri minyak, ia digunakan dalam proses penyediaan cecair tertentu kepadatan pelbagai yang digunakan dalam telaga minyak.
- Dalam bidang penyelidikan biologi, sifat mikrobiosida telah terbukti; iaitu, ia digunakan untuk mengawal pembangunan pelbagai jenis bakteria.
- Dalam sintesis jenis organik tertentu, garam tak organik ini digunakan untuk penyediaan spesies lain yang dibentuk oleh Bromo. Sebagai contoh, oleh tindak balas Finkelstein, reaktiviti alkil halogenida tertentu diperolehi, salah satunya digunakan untuk digunakan dalam fotografi.
- Di kawasan pembersihan dan pembasmian kuman, natrium bromida digunakan dalam kombinasi dengan klorin untuk sanitasi jumlah air yang besar, seperti di kolam renang dan jakuzis.