Struktur, sifat dan kegunaan butanone
- 3566
- 73
- Donnie Ryan
The Butanone Ia adalah sebatian organik, khususnya keton, yang formula kimianya adalah cho3Ch2COCH3. Penampilannya ialah cecair tanpa warna yang digunakan secara asasnya sebagai pelarut. Ia sama dengan sifat aseton, tetapi mendidih pada suhu yang lebih tinggi dan menguap lebih perlahan.
Ia dihasilkan oleh dehidrogenasi pemangkin 2-butanol (sebatian kiral). Walau bagaimanapun, ia berada dalam keadaan semula jadi dalam komposisi beberapa buah. Ia adalah sebahagian daripada emanasi paip ekzos kenderaan, dan merupakan komponen asap tembakau.
 Molekul butanone. Sumber: Pixabay.
Molekul butanone. Sumber: Pixabay. Ia adalah selepas aseton yang paling mudah dari keluarga sebatian organik ini. Butnonone menyebabkan kerengsaan di mata dan hidung. Dalam dos yang luar biasa tinggi ia boleh menyebabkan kerengsaan mukosa paru -paru. Sebaliknya, cecair ini dianggap sebagai ejen prekursor narkotik.
Butanone mempunyai kelarutan yang besar di dalam air; Tetapi ia juga sangat larut dalam pelarut organik seperti etanol, eter, aseton, benzena dan kloroform. Ini dapat dijelaskan kerana nilai log P (0.29) untuk pekali partisi oktana/air adalah rendah.
[TOC]
Struktur butanone
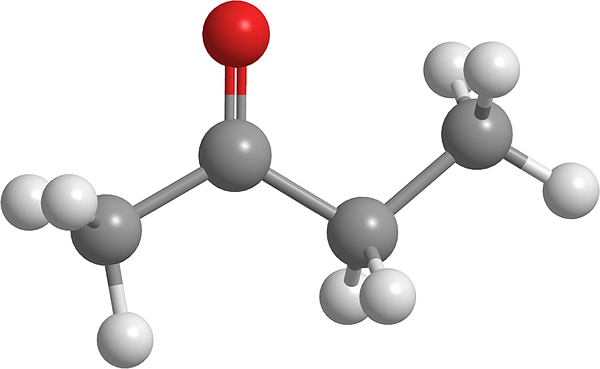
Dalam imej atas, molekul butanon ditunjukkan dengan model sfera dan bar. Atom oksigen kumpulan karbonil (sfera merah) dapat dilihat di karbon kedua. Kumpulan ini, c = o, bertanggungjawab untuk memberikan momen dipole kekal ke molekul.
Butanone, pandangan struktur, tidak lebih daripada aseton yang mana kumpulan metilena telah ditambah, ch2. Mempunyai lebih banyak karbon, momen dipole lebih kecil berbanding dengan aseton; Tetapi jisim molekul terbesarnya menyebabkan ia mendidih pada suhu yang lebih tinggi.
Molekul ini, seperti keton lain, tidak mempunyai kemungkinan membentuk jambatan hidrogen; Dan oleh itu, interaksi dipole-dipolo mereka tidak begitu kuat.
Boleh melayani anda: Pengemulsi: proses emulsi, aspek molekul, aplikasiItulah sebabnya ia adalah cecair yang tidak menentu. Apabila suhu jatuh (-86.6 ° C), dipoles lemahnya adalah mereka yang membimbing molekul mereka untuk membentuk kristal. Di samping itu, ia juga boleh dikomentari bahawa butanone tidak simetris secara struktural.
Sifat
Formula molekul
C4H8Atau ch3COCH2Ch3
Nama
- Butanone.
- 2-Butanon.
- Butan -2 -ona.
- Methyl Ethil Cetona.
Jisim molar
72,107 g/mol.
Penerangan fizikal
Cecair tanpa warna.
Bau
Wangi hingga pudina, cukup kuat.
Takat didih
79.59 ºC pada 760 mmHg.
Takat lebur
-86.6 ºC.
titik pencucuhan
-9 ºC (cawan tertutup).
Kelarutan air
29 g /100 ml pada 20 ºC. Walaupun momen dipole kurang daripada aseton, ia masih boleh berinteraksi dalam tahap yang sangat baik dengan molekul air. Dari mereka menerima jambatan hidrogen: (CH3) (Ch2Ch3) C = o-hah. Kerana ini sangat larut dalam air.
Kelarutan dalam pelarut organik
Larut dalam benzena, alkohol dan eter; Majazah dengan minyak, etanol, eter, aseton, benzena dan kloroform. Perhatikan bahawa butanone larut dalam pelbagai pelarut.
Ketumpatan
0.7997 g/cm3 pada 25 ºC.
Ketumpatan wap
2,41 (berhubung dengan air = 1).
Tekanan wap
90.6 mmhg pada 25 ºC.
Pekali partisi oktanol/air
Log p = 0.29
Suhu sendiri
505 ºC.
Penguraian
Ia terurai oleh proses fotokimia oleh pengoksidaan oleh radikal hidroksil percuma. Apabila dipanaskan hingga penguraian memancarkan asap ekar.
Goo
0.40 cpoise pada 25 ºC.
Haba pembakaran
2.444.1 kJ/mol pada 25 ° C.
Haba pengewapan
31.30 kJ/mol di titik didih; dan 34.79 kJ/mol pada 25 ° C.
Boleh melayani anda: Undang -undang gas umumKetegangan permukaan
23.97 mn/m A 25 ºC.
Potensi pengionan
0.54 eV.
Ambang bau
Bau rendah: 0.735 mg/m3.
Bau tinggi: 147.5 mg/m3.
Indeks refraktif
1,788 hingga 20 ºC.
Pemisahan pemalar
PKA = 14.70.
Kestabilan
Stabil, tetapi sangat mudah terbakar. Tidak sesuai dengan ejen pengoksidaan, pangkalan, dan ejen pengurangan yang kuat. Kelembapan harus dielakkan.
Aplikasi
Pelarut
Butanone digunakan sebagai pelarut dalam penjelasan salutan permukaan, pembuatan habuk tanpa asap, penghuraian resin berwarna, dan dalam penghapusan pengumpulan lemak yang dihasilkan oleh pelincir.
Di samping itu, ia digunakan dalam penjelasan:
- Kulit tiruan.
- Gomas.
- Lacas.
- Varnis.
- Lap.
- Pelarut.
- Cat kepentingan.
- Pelekat.
- Semen plastik.
- Pengedap.
- Pita magnet.
- Kertas telus.
- Tinta cetak.
- Kosmetik dan produk farmaseutikal.
Ia juga digunakan sebagai pelarut untuk mencelupkan permukaan logam, pembersih peralatan elektronik, dan pengekstrakan lemak. Ia berfungsi untuk pengekstrakan kayu keras dan minyak sayuran.
Ia adalah bahan lengai dalam penjelasan racun perosak, dan dalam pembuatan nitrat asetat dan selulosa.
Ia digunakan sebagai pelarut pengekstrakan dalam pemprosesan makanan dan bahan makanan; Contohnya, dalam fraksionasi lemak dan minyak, serta dalam proses decaffeinated kopi. Ia juga digunakan sebagai pelarut dalam penanda yang digunakan di papan putih.
Reagen
- Butanone digunakan sebagai photoiniciator larut air.
- Ia memendekkan formaldehid untuk menghasilkan ketone isopropenil.
- Mengalami autokodensasi untuk pengeluaran etil amilo cetona.
- Bertindak balas dengan citral untuk mendapatkan komponen minyak wangi seperti methylpseudoionone.
Boleh melayani anda: haba reaksi- Ia campur tangan sebagai pemangkin dalam pengeluaran hidrakcin.
- Di samping.
Simen plastik
Butanone mempunyai aplikasi sebagai ejen kimpalan plastik, dengan penggunaan dalam pemasangan model skala polistirena. Butnonone membubarkan polistirena, membolehkan tepi menyertai apabila pempolimeran baru berlaku. Tingkah laku ini adalah simen dan bukan gam.
Kegunaan lain
Butanone digunakan sebagai pensterilan spora bakteria dalam instrumen pembedahan, jarum, penyuntik hipodermal dan instrumen pergigian.
Ia digunakan sebagai agen perasa makanan dalam kepekatan yang sangat rendah; Sebagai contoh, dalam minuman beralkohol, kepekatan adalah 20 ppm; dalam produk bakar, 12.7 ppm; Daging mempunyai kira -kira 26.5 ppm; getah getah, 0.63 ppm; dan lemak dan minyak, 1.0 ppm.
Dan akhirnya, butanone digunakan dalam pemisahan apoprotein kumpulan hemoprotein dalam hemoprotein.
Rujukan
- Morrison, r. T. dan Boyd, R, n. (1987). Kimia organik. 5TA Edisi. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. Amina. (10thEdisi.). Wiley Plus.
- Pusat Kebangsaan Maklumat Bioteknologi. (2019). Pangkalan data pubchem metil etil ketone. CID = 6569. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Wikipedia. (2019). Butanone. Diperoleh dari: dalam.Wikipedia.org
- Persatuan Kimia Diraja. (2015). Butanone. Chemspider. Pulih dari: chemspider.com
- Arlem Cheprasov. (2019). Apa itu butanone? Formula & Penggunaan. Kajian. Pulih dari: belajar.com
- Ben Verve. (17 Mei 2017). Butanone. Dunia kimia. Pulih dari: dunia kimia.com

