Sel elektrolisis
- 3322
- 924
- Ismael Turner
 Sel elektrolisis adalah peranti elektrokimia untuk meningkatkan tindak balas oksida bukan spontan melalui elektrik
Sel elektrolisis adalah peranti elektrokimia untuk meningkatkan tindak balas oksida bukan spontan melalui elektrik Apakah sel elektrolitik?
The Sel elektrolisis Ia adalah peranti yang digunakan untuk meningkatkan tindak balas kimia pengurangan bukan -spontan dengan menggunakan elektrik. Dalam erti kata lain, mereka adalah sel di mana proses elektrolisis dijalankan, dan oleh itu namanya.
Ia adalah jenis sel elektrokimia tertentu. Ini bermakna bahawa mereka adalah peranti di mana spesies yang mengoksidakan dan yang dikurangkan tidak bersentuhan langsung, tetapi terdapat di petak yang berbeza atau bertindak balas secara fizikal secara fizikal.
Atas sebab ini, pertukaran elektron antara spesies pengoksidaan dan pengurangan tidak berlaku secara langsung, tetapi melalui konduktor luaran.
Sekiranya reaksi redoks berlaku secara spontan, iaitu, tanpa bantuan sumber tenaga luaran, kita bercakap mengenai sel galvanik.
Contohnya ialah bateri kereta. Sebaliknya, jika tindak balas memerlukan sumber tenaga luaran, ia adalah sel elektrolisis.
Operasi sel elektrolisis
Setiap sel elektrolitik dibentuk oleh beberapa elemen asas yang:
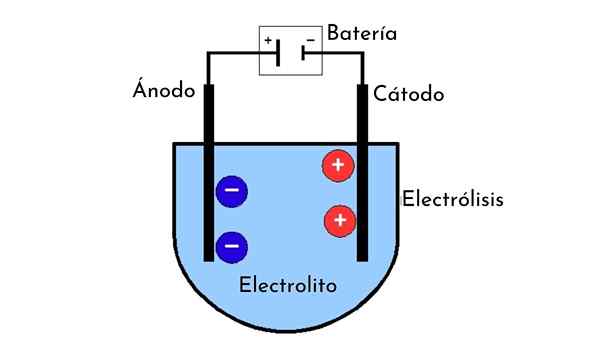
- Dua elektrod dipanggil anod dan katod.
- Penyelesaian bahan yang kami ingin serahkan kepada elektrolisis atau, gagal itu, bahan yang sama dalam keadaan cair (contohnya, garam cair).
- Konduktor elektrik.
- Sumber kuasa elektrik.
Prosesnya dijalankan untuk reaksi yang dalam keadaan normal tidak spontan. Ini bermakna bahawa mereka adalah pengurangan reaksi karat yang potensi sel, memandangkan kepekatan spesies dan keadaan suhu dan tekanan, adalah negatif.
Ini menunjukkan bahawa elektron tidak mempunyai kecenderungan untuk pergi dari spesies yang kita mahu mengoksidakan ke arah yang kita mahu mengurangkan, melainkan ke arah yang bertentangan. Dengan menggunakan voltan luaran tanda yang bertentangan, kita boleh melabur tanda potensi sel, memaksa reaksi berlaku.
Boleh melayani anda: Bahan larutSeperti sebarang tindak balas redoks, elektrolisis berlaku dalam bentuk dua separuh -reaksi yang berlaku secara berasingan dalam dua elektrod. Ini dipanggil katod dan anod.
Katod
Katod adalah elektrod yang disambungkan ke tiang negatif sumber tenaga, dan di sinilah separuh -reaksi pengurangan berlaku. Ia juga merupakan elektrod yang mana ion positif diarahkan semasa elektrolisis. Malah, di mana nama kation berasal.
Apabila mewakili proses elektrolisis dalam bentuk gambarajah sel, pengurangan separuh lampu yang berlaku di dalam katod selalu diletakkan di sebelah kanan.
Anod
Anod adalah elektrod yang menentang katod. Iaitu, ia adalah elektrod yang disambungkan kepada kuasa positif sumber tenaga dan di mana pengoksidaan separuh lampu berlaku. Ia juga merupakan tempat di mana ion dengan beban negatif (anion) diarahkan dan sentiasa diwakili di sebelah kiri rajah sel.
Aliran elektron dalam sel elektrolisis
Apabila elektrod disambungkan ke tiang yang bertentangan dengan sumber tenaga yang mempunyai potensi yang cukup, litar ditutup dan arus elektrik dihasilkan. Arus ini bermula di anod, di mana spesies pengurangan mengoksidakan dan kehilangan elektron.
Elektron ini mengalir melalui konduktor elektrik, didorong oleh perbezaan yang berpotensi sehingga sampai ke katod. Sekali di permukaan katod, elektron lulus ke spesies oksida, mengurangkannya dan menyelesaikan reaksi redoks.
Supaya aliran elektrik dapat diteruskan, ion dalam larutan atau garam cair bergerak dari satu elektrod ke yang lain. Kation mengalir ke katod dan anion ke arah anod.
Dapat melayani anda: reaksi kimia kehidupan seharianWalaupun mereka nampaknya dua arus dalam arah yang bertentangan, pada hakikatnya kedua -dua arus masuk ke arah yang sama. Ini kerana pembawa beban yang bergerak ke arah yang bertentangan juga mempunyai beban bertentangan.
Jenis sel elektrolisis
Sel -sel elektrolit larutan berair
Ini adalah sel yang paling biasa. Mereka hanya terdiri daripada dua elektrod beberapa logam lengai yang tenggelam dalam larutan garam berair yang ingin kami serahkan kepada elektrolisis.
Mereka hanya berkhidmat untuk mengurangkan spesies yang mempunyai potensi pengurangan yang lebih positif daripada hidrogen, dengan syarat pH adalah neutral.
Sebaliknya, mereka hanya berfungsi untuk mengoksidakan spesies yang mempunyai potensi pengoksidaan yang lebih besar daripada air kecuali pengganti oksigen.
Sel elektrolisis garam cair
Dalam kes di mana spesies yang kita mahukan. Ini memerlukan sel khas, seperti sel Downs.
Aplikasi sel elektrolitik
Sel elektrolisis sangat penting dalam industri. Beberapa aplikasi yang paling penting ialah:
Penyimpanan Tenaga
Elektrolisis membolehkan menukar tenaga potensi elektrik menjadi tenaga kimia yang berpotensi. Spesies yang dikurangkan dan teroksida semasa proses elektrolisis menjadi spesies baru yang mampu bertindak balas secara spontan, melepaskan tenaga yang terbalik lagi.
Pengeluaran halogen asas
Halogen sangat penting industri. Walau bagaimanapun, mereka tidak bersifat asas, kerana mereka adalah bahan pengoksidaan yang sangat reaktif. Atas sebab ini, banyak halogen hanya boleh berlaku melalui elektrolisis.
Boleh melayani anda: penyebaran fasaPengeluaran logam tulen
Sama yang boleh dikatakan mengenai halogen juga boleh dikatakan mengenai logam paling reaktif dalam jadual berkala. Unsur -unsur seperti logam alkali dan tembaga hanya boleh diperolehi oleh elektrolisis garam cair dan larutan berair.
Contoh sel elektrolisis dalam kehidupan seharian
Elektrolisis natrium fluorida
Elektrolisis natrium natrium fluorida cair digunakan secara industri untuk pengeluaran natrium dan fluorin asas. Fluorin kemudian boleh digunakan untuk mendapatkan halogen yang kurang reaktif yang lain.
Elektrolisis nitrat tembaga
Dalam pengeluaran tembaga perindustrian, ini diperolehi melalui elektrolisis penyelesaian berair garamnya. Di samping itu, tembaga juga disucikan oleh elektrolisis, pengoksidaan dan membubarkannya dari elektrod dan mendepositkannya di pihak yang lain.
Elektrolisis air
Elektrolisis larutan berair asid sulfurik mengurai oksigen dan air hidrogen dan merupakan salah satu cara paling mudah untuk mendapatkan elemen terakhir ini dalam bentuk tulen.
Rujukan
- Corinth - Kimia Umum (s. F.). Sel elektrolisis. Diambil dari Korintus.Pucp.Edu.PE.
- Ecured (s. F.). Sel elektrolitik. Diambil dari ecured.Cu.
- Luis Manuel (2014). Jenis sel elektrokimia. Diambil dari Prezi.com.
- Berhenti p., Yo. (2021). Apakah sel elektrolitik? Diambil dari yubrain.com.

