Struktur, sifat, penggunaan dan sintesis siklobutane
- 4647
- 1376
- Donnie Ryan
Dia Cyclobutane Ia adalah hidrokarbon yang terdiri daripada cyclocano empat -karbon, yang formula molekulnya adalah c4H8. Anda juga boleh dipanggil tetramethylene, memandangkan terdapat empat unit PBB2 yang membentuk cincin dengan geometri persegi, walaupun nama siklobutane lebih diterima dan dikenali.
Pada suhu bilik ia adalah gas yang tidak berwarna dan mudah terbakar yang terbakar dengan api yang cerah. Penggunaan yang paling primitif adalah sebagai sumber haba dengan membakarnya; Walau bagaimanapun, asas strukturnya (persegi) merangkumi aspek biologi dan kimia yang mendalam, dan bekerjasama dengan cara tertentu dengan sifat -sifat sebatian tersebut.
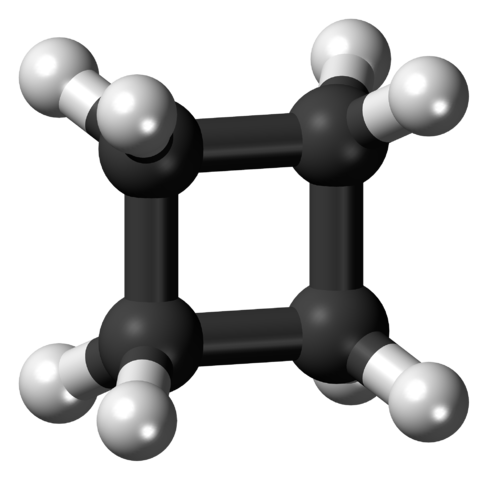 Molekul siklobutane dalam penyesuaian tegang. Sumber: Jynto [CC0].
Molekul siklobutane dalam penyesuaian tegang. Sumber: Jynto [CC0]. Dalam imej atas molekul siklobutane dengan struktur persegi ditunjukkan. Di bahagian seterusnya ia akan dijelaskan mengapa penyesuaian ini tidak stabil, kerana pautannya tegang.
Selepas cyclopropo, ia adalah sikloalcan yang paling tidak stabil, kerana saiz cincin yang lebih kecil, semakin reaktif itu akan. Menurut ini, siklobutane lebih tidak stabil daripada kitaran Pentan dan Hexano. Walau bagaimanapun, adalah ingin menyaksikan derivatifnya sebagai teras atau hati persegi, yang, seperti yang akan dilihat, adalah dinamik.
[TOC]
Struktur Cyclobutane
Dalam imej pertama struktur siklobutane ditangani sebagai karbon mudah dan dataran terhidrogenasi. Walau bagaimanapun, di kuadrat sempurna ini orbitals mengalami luka yang teruk dari sudut asalnya: mereka dipisahkan oleh sudut 90º berbanding 109.5º untuk atom karbon dengan spa hibridisasi sp sp SP3 (ketegangan sudut).
Bintik karbon kereta3 Mereka adalah tetrahedrals, dan bagi sesetengah tetrahedra, sukar untuk melengkapkan kedua -dua orbital mereka untuk mencipta sudut 90º; Tetapi lebih banyak lagi untuk karbon dengan hibridisasi SP2 (120º) dan SP (180º) mengalihkan sudut asal anda. Atas sebab ini Cyclobutane mempunyai atom karbon SP3 pada asasnya.
Boleh melayani anda: alkohol sekunder: apakah, struktur, sifat, kegunaanJuga, atom hidrogen sangat rapat antara satu sama lain, dikurangkan di ruang angkasa. Ini mengakibatkan peningkatan halangan sterik, yang melemahkan persegi yang dikatakan untuk voltan kilasan yang tinggi.
Oleh itu, ketegangan sudut dan kilasan (dikemas dalam istilah 'ketegangan anulus') menjadikan penyesuaian ini tidak stabil dalam keadaan normal.
Cyclobutan.
Rama -rama atau konformasi berkedut
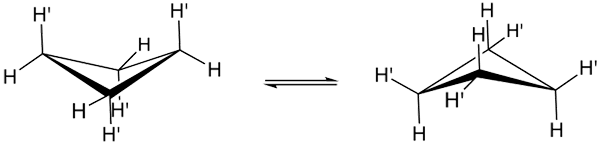 Konformasi Cyclobutane. Sumber: Smokefoot.
Konformasi Cyclobutane. Sumber: Smokefoot. Konformasi sebenar cyclobutano ditunjukkan di atas. Di dalamnya ketegangan sudut dan kilasan berkurangan; Oleh kerana, seperti yang dapat dilihat, tidak semua atom hidrogen dilepaskan. Walau bagaimanapun, terdapat kos tenaga: sudut pautannya diburukkan lagi, iaitu, rendah dari 90 hingga 88º.
Perhatikan bahawa ia boleh dibandingkan dengan rama -rama, yang sayap segi tiga dibentuk oleh tiga atom karbon; dan keempat, diposisikan pada sudut 25º berkenaan dengan setiap sayap. Anak panah rasa berganda menunjukkan bahawa terdapat keseimbangan antara kedua -dua pengubah. Seolah -olah rama -rama itu turun dan memanjat sayapnya.
Pada mereka yang berasal dari cyclobutane, sebaliknya, diharapkan bahawa kelemahan ini akan menjadi lebih lambat dan dihalang secara spasial.
Interaksi intermolecular
Katakan bahawa anda lupa selama beberapa saat di dataran, dan ganti mereka di tempat dengan rama -rama berkarbonat. Anda berada di dalam keributan mereka hanya dapat disimpan bersama dalam cecair dengan cara penyebaran London, yang berkadar dengan kawasan sayap mereka dan jisim molekulnya.
Ia boleh melayani anda: Kumpulan Carbonyl: Ciri -ciri, Harta, Tatanama, KereaktifanSifat
Penampilan fizikal
Gas tidak berwarna.
Jisim molekul
56,107 g/mol.
Takat didih
12.6ºC. Oleh itu, dalam keadaan sejuk, ia dapat dimanipulasi pada dasarnya sebagai cecair; Dengan satu -satunya terperinci, ia akan menjadi sangat tidak menentu, dan wap mereka masih akan mewakili risiko untuk mengambil kira.
Takat lebur
-91ºC.
titik pencucuhan
50ºC cawan tertutup.
Kelarutan
Tidak larut dalam air, yang tidak terkejut memandangkan sifat apolarnya; Tetapi, ia sedikit larut dalam alkohol, eter dan aseton, yang kurang pelarut kutub. Ia dijangka larut (walaupun tidak dilaporkan) secara logik dalam pelarut apolar seperti karbon tetraklorida, benzena, xilena, dll.
Ketumpatan
0.7125 hingga 5ºC (berhubung dengan 1 dari air).
Ketumpatan wap
1.93 (berhubung dengan 1 udara). Ini bermakna ia adalah padat daripada udara, dan oleh itu, melainkan jika terdapat arus, trendnya tidak akan naik.
Tekanan wap
1.180 mmHg pada 25ºC.
Indeks refraktif
1,3625 hingga 290ºC.
Entalpi pembakaran
-655.9 kJ/mol.
Haba pembentukan
6.6 kcal/mol A 25ºC.
Sintesis
Cyclobutane disintesis oleh penghidrogenan cyclobutadiene, yang strukturnya hampir sama, dengan satu -satunya perbezaan yang mempunyai ikatan berganda; Dan oleh itu, ia lebih reaktif. Ini mungkin laluan sintetik yang paling mudah untuk mendapatkannya, atau sekurang -kurangnya hanya kepadanya dan bukan derivatif.
Dalam mentah, tidak mungkin diperoleh kerana ia akan bertindak balas sedemikian rupa sehingga ia memecahkan cincin dan rantai garis terbentuk, iaitu, n-butan.
Kaedah lain untuk mendapatkan siklobutane adalah mempengaruhi sinaran ultraviolet pada molekul etilena, CH2= Ch2, yang diukur. Reaksi ini disukai fotokimia, tetapi tidak termodinamik:
Boleh melayani anda: Benchilo Benzoate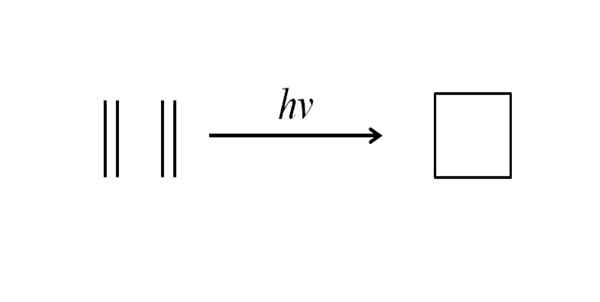 Sintesis siklobutane oleh sinaran ultraviolet. Sumber: Gabriel Bolívar.
Sintesis siklobutane oleh sinaran ultraviolet. Sumber: Gabriel Bolívar. Imej atas meringkaskan apa yang dikatakan dalam perenggan di atas. Jika bukan etilena itu, sebagai contoh, mana -mana dua alkenes, siklobutane yang diganti akan diperolehi; atau apa yang sama, derivatif sikloba. Malah, banyak derivatif dengan struktur yang menarik telah disintesis melalui kaedah ini.
Walau bagaimanapun, derivatif lain menyiratkan satu siri langkah sintetik yang rumit. Oleh itu, cyclobuta (seperti derivatif mereka dipanggil), tertakluk kepada kajian sintesis organik.
Aplikasi
Cyclobutane sahaja tidak lagi digunakan daripada berfungsi sebagai sumber haba; Tetapi, derivatifnya masuk ke tanah yang rumit dalam sintesis organik, dengan aplikasi dalam farmakologi, bioteknologi dan perubatan. Tanpa memperdalam struktur yang terlalu kompleks, Penitrems dan Grandisol adalah contoh siklobutan.
Cyclobutans umumnya mempunyai sifat yang bermanfaat untuk metabolisme bakteria, tumbuh -tumbuhan, invertebrata laut dan kulat. Mereka aktif secara biologi, dan itulah sebabnya kegunaan mereka sangat bervariasi dan sukar untuk ditentukan, kerana masing -masing mempunyai kesan khusus mereka terhadap organisma tertentu.
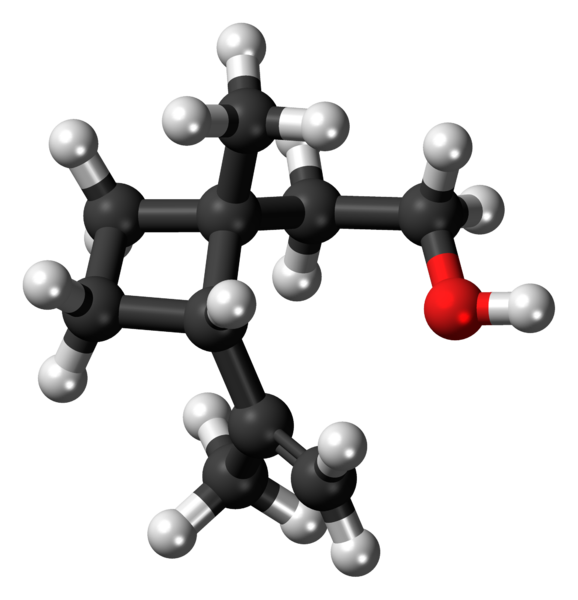
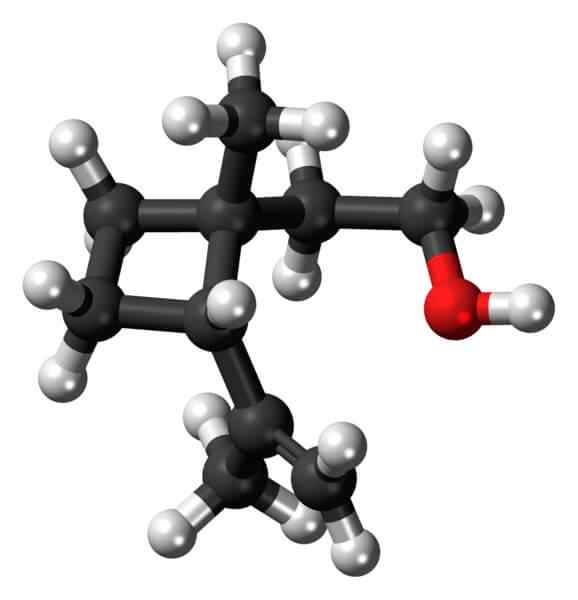 Grandisol: Contoh derivatif siklobutane. Sumber: Jynto [CC0].
Grandisol: Contoh derivatif siklobutane. Sumber: Jynto [CC0]. Grandisol, sebagai contoh, adalah pheromone Gorgjo (sejenis kumbang). Di atas, dan akhirnya, strukturnya ditunjukkan, dianggap sebagai monoterpene dengan asas persegi siklobutane.
Rujukan
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Graham Solomons, t.W.; Craig b. Fryhle. (2011). Kimia organik. (Sebelasth edisi). Wiley.
- Wikipedia. (2019). Cyclobutane. Diperoleh dari: dalam.Wikipedia.org
- Pubchem. (2019). Cyclobutane. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Peiris Nicole. (29 November 2015). Sifat fizikal sikloalkanes. Kimia Librettexts. Pulih dari: chem.Libretxts.org
- Wiberg b. Kenneth. (2005). Sifat siklobutane-fizikal dan kajian teoritis. Jabatan Kimia, Universiti Yale.
- Klement foo. (s.F.). Siklobutan dalam sintesis organik. Diperolehi dari: Scripps.Edu
- Myers. (s.F.). Sintesis Cyclobutanes. Chem 115. Pulih dari: hwpi.Harvard.Edu

