Struktur asid sulfámic, sifat, sintesis, kegunaan
- 1832
- 51
- Anthony Breitenberg
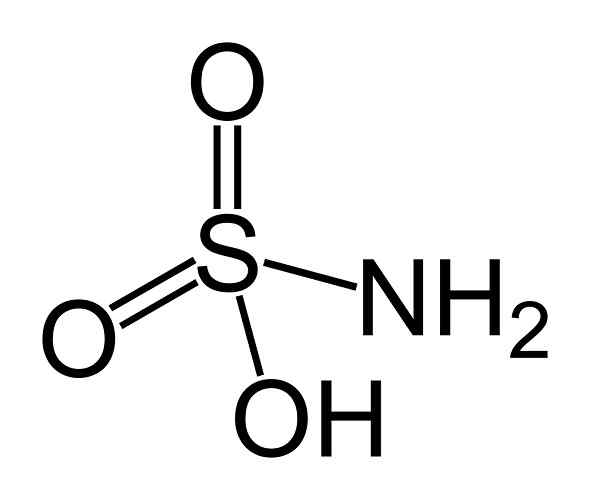
Dia Asid sulfamic Ia adalah sebatian bukan organik yang dibentuk oleh atom sulfur (s) yang dilampirkan dalam bentuk kovalen dan dengan pautan mudah ke kumpulan hidroksil (-OH) dan kumpulan amino (-NH2), dan dengan ikatan berganda kepada dua atom oksigen (O). Ia adalah pepejal kristal putih. Formula kimianya adalah NH2SW3H. Ia juga dikenali sebagai asid aminosulfonik, asid amidosulfonik, asid amidosulfurik dan asid sulfamidik.
Asid sulfámic adalah asid yang kuat. Anda boleh bertindak balas dengan logam, logam dan oksida karbonat. Garamnya biasanya larut dalam air, jadi ia adalah penghapus yang baik dalam inlays dalam peralatan proses. Ia sering digunakan dalam kilang gula untuk membersihkan inlays karbonat dalam penyejat.
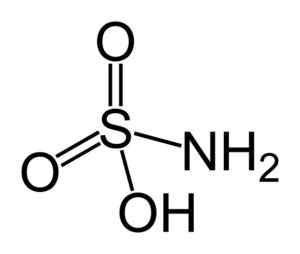 Struktur asid sulfámic. Benjah-bmm27 [domain awam]. Sumber: Wikipedia Commons.
Struktur asid sulfámic. Benjah-bmm27 [domain awam]. Sumber: Wikipedia Commons. Asid sulfámic adalah pengurangan nitrit (tidak2-) dan harta kimia ini digunakan dalam beberapa aplikasi, seperti dalam industri pewarna dan analisis nitrit.
Ia telah digunakan dalam penyamakan kulit dan dalam pemutihan pulpa untuk pembuatan kertas. Malah, ia adalah bahan pencemar makanan, seperti yang sering dijumpai di dalam kertas dan kad yang digunakan untuk membungkus kedai runcit.
Ia juga digunakan dalam elektrod logam, sebagai corak makmal dan salah satu derivatifnya adalah herba yang sangat berkesan.
[TOC]
Struktur
Asid sulfamic mengkristal dalam bentuk kristal ortorrombus bipiramidal. Bentuk prisma dan lembaran padat apabila mengkristal dari larutan sejuk, serta lembaran rhombus ketika menjadikannya larutan berair panas.
Nomenclature
- Asid sulfamic
- Asid aminosulfonic
- Asid amidosulfonik
- Asid amidosulfurik
- Sulfami -acid
Sifat
Keadaan fizikal
Pepejal kristal putih.
Berat molekul
97.1 g/mol.
Takat lebur
205 ºC, terurai pada 209 ºC.
Ketumpatan
2.15 g/cm3
Kelarutan
Larut dalam air:
- 12.8% hingga 0 ºC
- 17.57% pada 20 ºC
- 22.77% pada suhu 40 ° C
Hampir tidak larut dalam metanol, sedikit larut dalam aseton, tidak larut dalam eter.
Bebas larut dalam pangkalan nitrogen dan pelarut organik yang mengandungi nitrogen.
Tidak larut dalam disulfida karbon (CS2) dan karbon tetrachloride (CCL4).
Ph
0.41 (dalam penyelesaian 1 n, iaitu, 1 setara/l).
Pemisahan pemalar
0.101 hingga 25 ºC.
Sifat kimia
Ia adalah asid yang kuat. Hampir sama seperti asid hidroklorik (HCl), nitrik3) dan sulfur (h2SW4).
Boleh melayani anda: Sebatian oksigen: sifat, reaksi, kegunaanPenyelesaian asid sulfamik berair sangat terionisasi. PHnya lebih rendah daripada penyelesaian asid formik, fosforik dan oksalik.
Di dalam air, asid sulfamik hanya kehilangan proton yang terikat kepada oksigen. Nitrogen -Joined Hydrogens kekal kukuh bersatu.
Dalam larutan berair, perlahan -lahan dihidrolisiskan untuk memberikan asid ammonium sulfat (NH4Hso4). Stabil dalam keadaan kering.
Asid sulfámic menyerang logam, oksida logam dan karbonat untuk menghasilkan sulfamat. Contohnya, dengan kalium logam (k) kalium sulfamat (Koso2NH2) dan hidrogen (h2).
Semua garam asid sulfamik larut dalam air. Garam kalsium, plumbum dan barium sangat larut dalam air, tidak seperti asid sulfurik yang sepadan.
Asid nitrous (HNO2) bertindak balas secara kuantitatif dengan kumpulan amino asid sulfamik, melepaskan nitrogen (n2). Dianggarkan bahawa ion sulfamat berfungsi dalam tindak balas ini sebagai amida, bukan sebagai amina.
Asid sulfámic dioksidakan oleh klorin, bromin atau kalium klorat untuk mengubahnya menjadi asid sulfurik. Reaksi ini tidak berlaku dengan oksidan lain seperti asid kromik atau kalium permanganat.
Ia tidak serasi (bertindak balas) dengan alkali, klorin, asid hipoklorus, hipoklorit, sianida dan sulfida kuat.
Sifat lain
Ia bukan hygroscopic (ini bermaksud bahawa ia tidak menyerap kelembapan udara).
Apabila dipanaskan sehingga penguraian memancarkan asap sulfur oksida dan hidrogen klorida yang sangat toksik (HCL).
Salah satu derivatifnya, Ammonium Sulfamate, adalah retarder api.
Ia agak beracun.
Sintesis
Asid sulfámic diperolehi oleh tindak balas Co urea (NH2)2 Dengan asid sulfurik merokok, iaitu asid sulfurik (h2SW4) Berkonsentrasi yang mengandungi sulfur trioksida (begitu3).
Ia juga boleh disintesis dengan bertindak balas asid chlorosulfonic (HCLO3Cl) dan ammonia (NH3).
Aplikasi
Dalam industri pewarna
Asid sulfámic digunakan untuk menghilangkan nitrit yang berlebihan dengan cepat dan berkesan dalam tindak balas diazotisasi dalam sintesis pewarna. Jauh lebih praktikal daripada urea untuk tujuan ini.
Dalam pemprosesan kulit
Semasa penyamakan kulit, penggunaan asid sulfamik dan bukannya asid sulfurik memberikan tekstur yang lebih nipis dan lebih halus.
Boleh melayani anda: mineral logamDi samping itu, kerana kalsium sulfamat adalah larut air, tidak seperti kalsium sulfat, asid sulfámic boleh digunakan dalam proses yang tidak disengaja tanpa meninggalkan bintik -bintik yang kadang -kadang berlaku dalam kulit apabila digunakan asid sulfurik.
 Kasut kulit. Sumber: Pixabay.
Kasut kulit. Sumber: Pixabay. Dalam peralatan proses pembersihan
Asid sulfámic digunakan sebagai pembersih decalcifier dalam bisul, reaktor, paip, sistem penyejukan dan penukar haba.
Dalam peralatan ini, inlays untuk peredaran air atau sebatian proses dalam tumbuhan tenaga, tumbuhan kimia, pendekatan, kilang kertas, stesen mampatan dan industri lain dibentuk.
Inlays atau deposit pepejal boleh menjadi organik (alga, lumpur, kulat) atau bukan organik (oksida besi, sulfida besi, kalsium atau karbonat magnesium, sulfat, fosfat atau silikat).
Asid sulfámic sangat berkesan apabila digunakan untuk menghilangkan inlays kalsium karbonat. Ia boleh digunakan dalam peralatan tembaga, tembaga, keluli tahan karat, besi tuang dan keluli tergalvani.
Ia digunakan dalam penyelesaian 5-10% mengikut berat badan. Ia digunakan terutamanya dalam kilang gula untuk membersihkan penyejat yang diperbuat daripada besi tuang dengan penukar haba tembaga.
 Pasukan penyejat di kilang gula. Pengarang: Antiksh Kumar. Sumber: Pixabay
Pasukan penyejat di kilang gula. Pengarang: Antiksh Kumar. Sumber: Pixabay Ia harus digunakan pada suhu tidak melebihi 50-60 ºC. Suhu 70 ºC membawa kepada pembentukan sulfat yang tidak larut seperti kes4.
Apabila digunakan digabungkan dengan natrium klorida, kesan sinergi berlaku dan penyelesaiannya membolehkan oksida ferrik perlahan -lahan dibubarkan. Dalam kes ini, ia tidak boleh digunakan dengan keluli tahan karat kerana asid hidroklorik dilepaskan, yang boleh menyebabkan kakisan dalam bahan tersebut.
Dalam penapisan logam
Elektrodeposisi logam seperti tembaga, perak, kobalt, nikel, zink, kadmium, besi dan plumbum dapat dilakukan dengan jayanya dalam penyelesaian asid sulfamik. Ini boleh dikendalikan lebih mudah daripada asid asid hidrofi (h2Sif6).
Sebagai reagen corak di makmal
Memandangkan ciri-ciri tertentu asid sulfamik seperti: daya sebagai asid, kemudahannya disucikan oleh penghabluran semula dalam air, kestabilannya dan bukan hidroskopisnya, ia telah digunakan sebagai standard utama di peringkat makmal. Ini bermakna ia digunakan untuk penentuan alkali kuantitatif.
 Makmal. Publicdomainpictures. Sumber: Pixabay
Makmal. Publicdomainpictures. Sumber: Pixabay Dalam analisis nitrit
Kerana reaksi mudahnya dengan nitrit, asid sulfámic digunakan untuk penentuan ini dalam larutan.
Boleh melayani anda: asid tricloroacetic: struktur, sifat, sintesis, kegunaan, kesanDalam analisis air dibubarkan di dalam air
Oleh kerana asid sulfamik yang bertindak balas dengan nitrit air dilepaskan nitrogen, adalah mungkin untuk menentukan oksigen yang dibubarkan di dalam air, kerana gangguan yang disebabkan oleh nitrit dihapuskan.
Dalam penyediaan oksida nitrous
Asid sulfámic bertindak balas dengan asid nitrik yang menjana nitrous oksida (n2Sama ada). Tindak balas ini lebih selamat daripada ammonium nitrat untuk mendapatkan gas tersebut.
Dalam bidang pertanian
Derivatif asid sulfámic, ammonium sulfamate, adalah herbisida bukan toksik untuk haiwan.
Ia digunakan oleh embun pada lembaran spesies yang akan dihapuskan pada akhir musim panas atau permulaan musim luruh, sebaiknya dalam cuaca lembap. Apabila menggerakkan kompaun dari daun ke akar, tumbuhan mati.
 Permohonan Herbisida Rocío. Pengarang: Zefe Wu. Sumber: Pixabay
Permohonan Herbisida Rocío. Pengarang: Zefe Wu. Sumber: Pixabay Satu lagi kelebihan kompaun ini ialah tanah tidak mensterilkan secara kekal. Sesetengah nitrogen ammonium sulfamat boleh didapati di tanah untuk pertumbuhan tumbuhan pada musim depan.
Dalam kain api
Keserasiannya dengan selulosa dan ciri -ciri retarder kebakarannya menukar ammonium sulfamat menjadi ejen untuk mendapatkan kain dan kertas yang tahan api api.
10% daripada berat kain digunakan, yang penampilan dan sensasi sentuhan tetap tidak berubah. Kain ketika digunakan harus dibasuh kering, tidak pernah dibasuh dengan air agar tidak membubarkan sulfamat.
Ia berguna terutamanya di teater atau tempat yang serupa.
 Teater. Pengarang: MustangJoe Sumber: Pixabay
Teater. Pengarang: MustangJoe Sumber: Pixabay Dalam pelbagai aplikasi
Ia digunakan sebagai pemangkin dalam beberapa tindak balas kimia, seperti dalam penyediaan resin urea-formalde. Ia juga berguna sebagai bakteria dan penstabil klorin di kolam renang dan sebagai peluntur pulpa kayu di kilang pulpa dan kertas.
Rujukan
- Atau.S. Perpustakaan Perubatan Negara. (2019). Asid sulfamic. Pulih dari pubchem.NCBI.NLM.NIH.Gov
- Williams, d.L.H. (2004) Nitrosasi di Pusat Nitrogen. Dalam tindak balas nitrosasi dan kimia oksida nitrik. bab 2. Pulih dari Scientedirect.com
- Clapp, Leallyn B. (1943). Asid sulfamik dan kegunaannya. Chem. Pendidikan. 1943, 20, 4, 189. Pulih dari pub.ACS.org
- McDonald, James. (2003). Asid sulfamic. Pulih dari Veoliawatertech.com
- Sastri, v.S. (2010). Pengurusan dan kawalan kakisan. Dalam kakisan Shreir. Pulih dari Scientedirect.com
- Bajpai Pratima. (2018). Topik Pelbagai. Dalam buku panduan pulpa dan kertas Biermann. Edisi ketiga. Pulih dari Scientedirect.com

