Enantiomer
- 787
- 211
- Julius Dibbert
Kami menerangkan apa yang enantiomer dan chirtality, sifat mereka, tatanama dan beberapa contoh
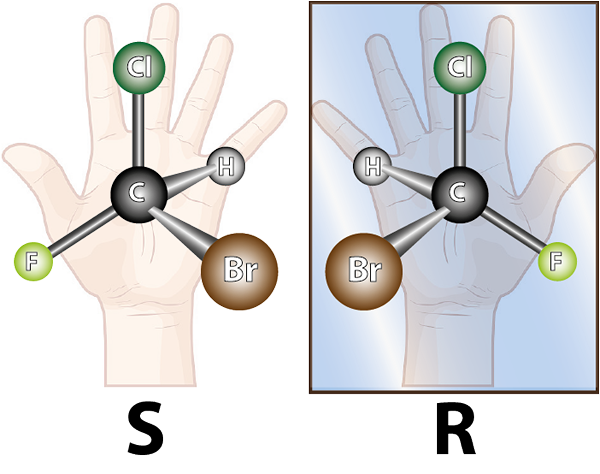
 Kedua -dua sebatian ini adalah enantiomer, kerana ia dibentuk oleh atom yang sama, bersatu dengan cara yang sama dan imej specular antara satu sama lain
Kedua -dua sebatian ini adalah enantiomer, kerana ia dibentuk oleh atom yang sama, bersatu dengan cara yang sama dan imej specular antara satu sama lain Apakah enantiomer?
The enantiomer Mereka adalah pasang sebatian yang bukan imej cermin antara satu sama lain. Pasangan sebatian ini adalah jenis isomer tertentu, iaitu, mereka adalah sebatian yang berbeza yang mempunyai formula molekul yang sama.
Terdapat pelbagai jenis isomer di antaranya adalah stereoisomer, di mana semua atom bersatu dalam susunan yang sama dan dengan jenis pautan yang sama, tetapi mereka mempunyai orientasi yang berbeza di ruang angkasa (stereo bermakna ruang).
Di dalam stereoisomer, kita dapati enantiomer, yang ciri utamanya adalah imej specular antara satu sama lain.
Enantiomer sangat biasa. Malah, hampir semua sebatian organik yang terdapat di sel -sel semua makhluk hidup adalah salah satu daripada dua enantiomer yang mungkin.
Sebagai contoh, semua asid amino yang merupakan sebahagian daripada protein semulajadi sesuai dengan enantiomer L asid amino masing -masing (isomer lain mengenal pasti dengan huruf d).
Sebaliknya, bahan -bahan aktif sebahagian besar ubat juga wujud sebagai pasang enantiomer, yang mana hanya satu yang berkesan. Kesukaran untuk memisahkan enantiomer antara satu sama lain bermaksud bahawa ubat -ubatan yang hanya mengandungi isomer berguna sangat mahal.
Enantiomer dan chirtality
Enantiomer dibentuk oleh molekul kiral. Chirtality adalah milik yang tidak dapat ditindas dengan imej cerminnya. Perkataan kiral berasal dari istilah Yunani, Kheir yang bermaksud tangan, mengingati hakikat bahawa tangan juga imej spekular antara satu sama lain, dan mereka tidak dapat bertindih.
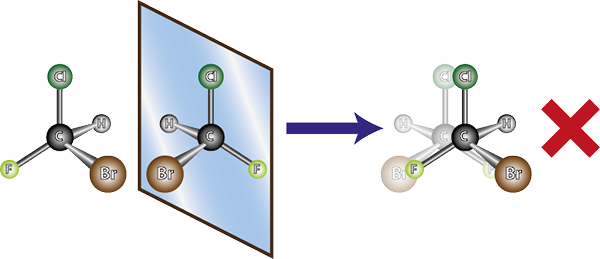 Molekul kiri adalah kiral, kerana apabila membandingkannya dengan imej cerminnya, dapat dilihat bahawa mereka tidak bertindih. Dengan kata lain, tidak ada cara untuk memutar atau mengubahnya sedemikian rupa sehingga semua atom bertepatan antara satu sama lain
Molekul kiri adalah kiral, kerana apabila membandingkannya dengan imej cerminnya, dapat dilihat bahawa mereka tidak bertindih. Dengan kata lain, tidak ada cara untuk memutar atau mengubahnya sedemikian rupa sehingga semua atom bertepatan antara satu sama lain Memandangkan perkara di atas, dapat disimpulkan bahawa bagi setiap molekul kiral, mesti ada molekul kiral lain yang tidak ada imej cermin yang bertindih, iaitu enantiomernya. Dengan kata lain, apabila molekul dikatakan.
Boleh melayani anda: Neodymium: struktur, sifat, kegunaanPusat Kiral
Banyak sebatian kiral mempunyai satu atau lebih pusat asimetrik yang bertanggungjawab untuk kreinya molekul. Ini dipanggil pusat kiral dan dalam banyak sebatian organik terdiri daripada atom karbon yang dikaitkan dengan 4 atom atau kumpulan atom yang berbeza.
Bentuk tertentu kerana empat kumpulan ini diedarkan di sekitar karbon asimetrik menentukan mana dari kedua -dua enantiomer sepadan dengan molekul kiral. Kehadiran pusat quiral tunggal memastikan bahawa molekul itu adalah kiral, tetapi jika ada lebih dari satu, ia mungkin kiral kerana tidak mungkin.
Sifat enontiomer
Sebilangan besar sifat fizikal dan kimia adalah sama
Seperti tangan kanan dan tangan kiri, enantiomer hanya berpasangan. Sebatian ini hampir sama antara satu sama lain. Malah, sebahagian besar sifat fizikal dan kimianya seperti titik gabungan, mendidih, tekanan stim dan kelarutan dalam beberapa pelarut, antara lain adalah sama.
Aktiviti optik
Semua sebatian kiral mempunyai harta yang unik yang membezakannya dari mereka yang tidak: mereka mempunyai keupayaan untuk memutar satah cahaya terpolarisasi. Harta ini dipanggil Aktiviti optik, Dan ia adalah salah satu daripada beberapa sifat yang membezakan sebatian kiral dari enantiomernya.
Yang terakhir adalah disebabkan oleh fakta bahawa satah cahaya terpolarisasi boleh diputar dalam salah satu daripada dua arah, sama ada ke arah jarum jam (dipanggil dextrogyr dan diwakili dengan simbol +) atau terhadap jarum jam (Levógiro, diwakili dengan simbol -).
Sekiranya sebatian quiral berkisar satah cahaya terpolarisasi dalam satu arah, enantiomernya akan mengubahnya ke arah yang bertentangan.
-
Contoh
Penyelesaian D-glukosa berkisar satah cahaya terpolarisasi ke arah jarum jam (ke kanan, ia adalah dextrogyral), sementara penyelesaian L-glikos menjadikannya berputar ke arah yang bertentangan.
Ia boleh melayani anda: Flask Erlenmeyer: Ciri, Kegunaan, Kaedah PenggunaanKereaktifan pembezaan
Harta lain yang membolehkan membezakan satu enantión dari yang lain, adalah kereaktifannya terhadap sebatian kiral yang lain.
Kereaktifan pembezaan boleh dibandingkan dengan cara sarung tangan hanya kelihatan baik di satu tangan, tetapi bukan yang lain, atau sebagai kasut yang betul sesuai dengan kaki kanan, tetapi tidak ke kiri.
Akibat penting kereaktifan pembezaan adalah kesan yang berbeza yang boleh menyebabkan dua enantiomer beberapa ubat. Perbezaan ini tidak berbahaya, tetapi mereka juga boleh menjadi sangat berbahaya.
-
Contoh
- Daripada dua enantimer aspartame (yang merupakan pemanis buatan), satu manis sementara yang lain tidak mempunyai rasa.
- Hanya enantiomer s omeprazole yang berkesan sebagai pelindung gastrik manakala yang lain tidak menghasilkan kesan.
- D-Penicilamine adalah ubat terhadap arthritis rheumatoid, sementara enantiomernya, l-penicilamine adalah racun berbahaya.
Penyerapan pembezaan
Enantiomer juga berbeza dengan cara mereka diserap dalam resin atau pepejal yang juga kiral. Campuran enantiomer boleh dipisahkan jika ia dilalui melalui lajur pemisahan kiral, kerana salah satu daripada dua enantiomer akan diserap lebih kuat daripada yang lain.
Nomenklatur enantiomer
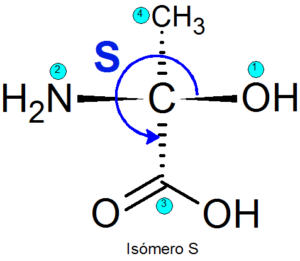
Terdapat beberapa kaedah untuk mengenal pasti satu atau enantiomer lain, tetapi yang paling banyak digunakan ialah sistem Cahn-ingold-prelog (CIP). Ini terdiri daripada langkah -langkah berikut:
- Tahap hierarki diberikan kepada empat kumpulan yang dilampirkan ke setiap pusat kiral. Keutamaan kumpulan diberikan mengikut nombor atom atom yang secara langsung dikaitkan dengan pusat quiral. Sekiranya terdapat dua atom yang sama, nombor atom atom yang dikaitkan dengan yang pertama ditambah untuk menambah nombor atom.
- Arah di mana tiga kumpulan keutamaan ditempah apabila titik keutamaan terendah ditentukan kembali.
- Sekiranya arah laluan berada di arah tangan jam, konfigurasi diberikan R, Jika tidak, konfigurasi diberikan S.
Contoh
Contoh enantiomer
D-Glyceraldehyde dan L-Glyceraldehyde
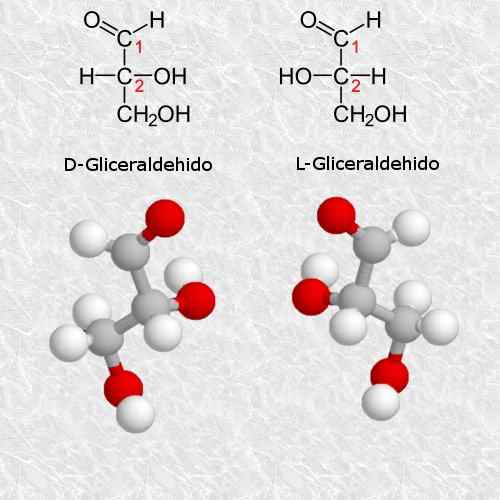
Glyceraldehyde adalah karbohidrat quiral yang paling mudah dan paling kecil yang wujud, dan sangat penting untuk kimia dan biologi.
Menurut peraturan sistem cahn-ingold-prelog, isomer d sepadan dengan isomer (r) dan isomer l sepadan dengan (s).
D-alanina dan l-alanina
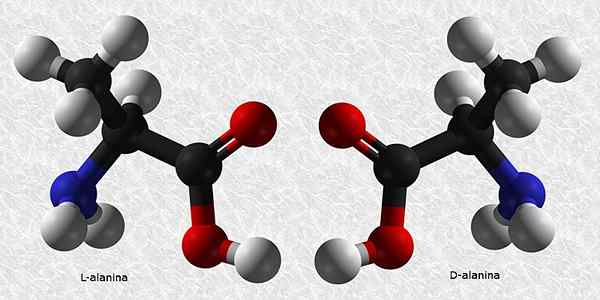
Alanine adalah salah satu asid amino penting untuk pembinaan protein. Seperti hampir semua asid amino, ia mempunyai karbon kiral sehingga ia mempunyai dua enantiomer:
Daripada kedua-dua ini, L-alanina adalah yang paling biasa dan hadir dalam semua makhluk hidup, sementara D-Alanina hanya terdapat di beberapa dinding sel bakteria.
Asid d-tartaric dan l-tartaric
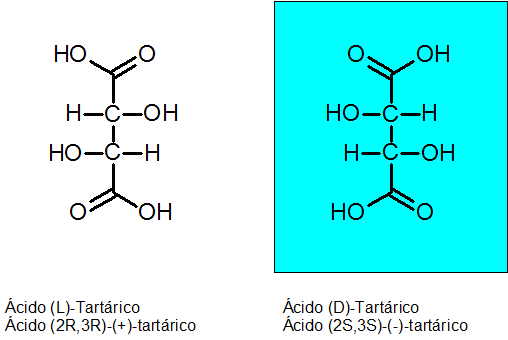
Kreiliti ditemui oleh Louis Pasteur pada tahun 1848 terima kasih kepada asid tartaric. Kompaun ini mempunyai 2 karbon asimetrik dan boleh wujud sebagai dua enantiomer ditambah isomer ketiga yang dipanggil kompa.
Konfigurasi mutlak dua karbon kiral adalah r untuk enantiómero levógiro dan s untuk enantiom dextrogyan.
2-Butanol
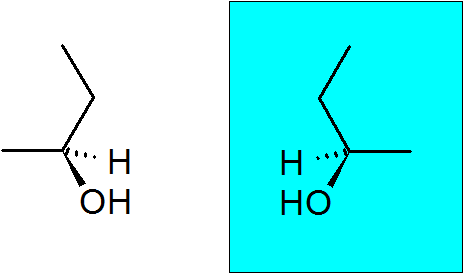
Alkohol ini juga mempunyai karbon quiral, yang menjadikan sebatian ini mempunyai dua enantiomer.
Bromocloroetan
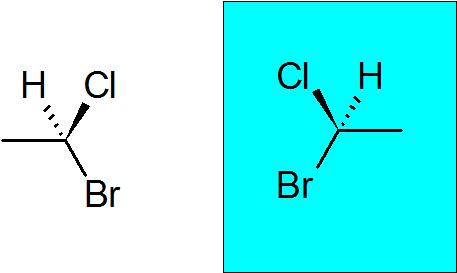
Ia adalah sebatian kiral yang sangat sederhana dengan hanya dua karbon. Quiral Carbon telah menyertai bromin, klorin, metil dan hidrogen.
Rujukan
- Chirtal (Kimia). (18 Mac, 2021), di Wikipedia.com
- Carey, f. Ke. (2008). Kimia organik. Boston: Pendidikan Tinggi McGraw-Hill.
- Smith, m., Mac, j., & Mac, J. (2001). Kimia Organik Lanjutan Mac: Reaksi, Mekanisme, dan Struptur. New York: Wiley.
- M.H. Hyun (2012). 8.13 Pemisahan dan Analisis Kromatografi: Chiral Crown Ether-berasaskan Chiral Fase. Editor: Erick m. Carreira, Hisashi Yamamoto. Memahami keahlian. Elsevier. Halaman 263-285. ISBN 9780080951683,
- Nguyen, l. Ke., Dia, h., & Pham-huy, c. (2006). Ubat Kiral: Gambaran Keseluruhan. Jurnal Antarabangsa Sains Bioperubatan: IJBS, 2(2), 85-100.

