Struktur, sifat, sifat, menggunakan, menggunakan, menggunakan, menggunakan, menggunakan,
- 3731
- 48
- Ismael Turner
Dia Ammonium fosfat Ia adalah keluarga sebatian garam yang berasal dari tindak balas antara asid fosforik dan ammonia. Menurut tatanama bukan organik, nama ini sesuai dengan garam yang formula kimianya (NH4)3PO4, Terdiri daripada kation ammonium, NH4+, dan anion fosfat, po43-.
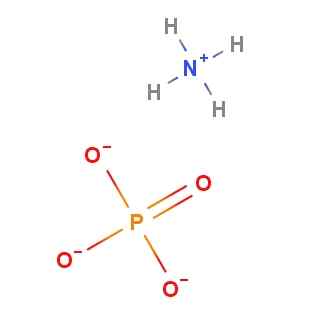
Dalam imej yang lebih rendah, perwakilan ion -ion ini ditunjukkan. The (nh4)3PO4 Ia juga dikenali sebagai fosfat tribasic ammonium atau fosfat triamonik. Nama -nama ini disebabkan oleh hakikat bahawa, seperti yang diperhatikan, PO43- Ia mempunyai tiga oksigen negatif yang mampu menerima proton, h+, asid sekitar.
 Ion ammonium fosfat. Sumber: Gabriel Bolívar melalui Molview.
Ion ammonium fosfat. Sumber: Gabriel Bolívar melalui Molview. Dan tepatnya inilah yang berlaku dengan NH4+ strukturnya sendiri. Oleh itu, ammonium fosfat tidak stabil, decomposing dalam NH4H2PO4 dan NH3. Itulah sebabnya garam ini menolak bau ammonia yang kuat.
Garam fosfat ammonium yang lain lebih stabil dan berguna. Contohnya, mereka digunakan dalam bidang pertanian sebagai bahan baja, dan kristal beberapa dari mereka bahkan mempunyai aplikasi optik dan fizikal.
Keluarga garam ini mudah tetapi pelbagai apabila keasidan medium diubah di mana ia berada.
[TOC]
Struktur
Ammonium fosfat terdiri daripada ion NH4+ dan po43-, Kedua -dua geometri tetrahedral. Elektron po43- Mereka diedarkan di antara tiga atom oksigen ikatan P-O-, beban negatif yang sangat menarik NH4+. Oleh itu, boleh dianggap bahawa struktur kristal (NH4)3PO4 adalah kuat.
Di dalamnya, ion NH4+ dan po43- Mereka ditemui dalam perkadaran 3: 1, yang bermaksud bahawa dalam kristal mereka terdapat ion triple nh4+ Bagaimana dengan ion po43-. Oleh itu, interaksi elektrostatiknya akhirnya menentukan kristal tetragonal.
Boleh melayani anda: radio: struktur, sifat, kegunaan, mendapatkanPerkara yang sama berlaku sebahagian dengan garam lain fosfat ini: (NH4)2HPO4 dan NH4H2PO4, di mana PO43- telah memenangi satu atau dua jam+, masing -masing. Dalam kristal tetragonalnya, interaksi elektrostatik lebih lemah kerana beban ionik kecil mereka.
Walau bagaimanapun, mereka lebih stabil, terutamanya NH4H2PO4, Nah, ia membentangkan titik lebur terbesar.
Sebaliknya, garam fosfat ammonium juga boleh membentuk hidrat, menggabungkan molekul air ke dalam struktur kristal mereka.
Sifat aminonium fosfat
Nama
(NH4)3PO4
Formula ini, dengan ketat mengikuti tatanama bukan organik, sepadan dengan garam garam garam. Nama lain yang diterima ialah:
-Ammonium fosfat tribasic
-Triammonium atau fosfat triamonik
(NH4)2HPO4
Garam ini membentangkan beberapa nama mengikut tatanama pilihan. Yang paling biasa, selain daripada fosfat diammonik, adalah:
-Asid ammonium fosfat
-Dibasic ammonium fosfat
Tidak seperti (NH4)3PO4, Ia terdiri daripada ion NH4+ dan HPO42- Dalam perkadaran 2: 1.
NH4H2PO4
Garam ini sepadan dengan "versi paling berasid" ammonium fosfat. Di dalamnya, PO43- telah memenangi dua h+, dengan itu mengurangkan beban ionnya ke h2PO4-. Oleh itu, nama mereka yang paling biasa adalah:
-Monobasic Ammonium Phosphate (kerana ia hampir tidak mempunyai oksigen yang mampu menerima proton)
-Ammonium diácido fosfat
Beberapa nama sebelumnya juga boleh diubah oleh:
-Dihydrogen ammonium fosfat
-Monoammonium fosfat
Seperti yang dapat dilihat, terdapat banyak nama yang mungkin. Yang penting adalah untuk mengetahui bagaimana untuk menghubungkannya secara langsung dengan formula mana -mana tiga garam yang sepadan dengan keluarga ammonium fosfat.
Massa molar
(NH4)3PO4: 149.09 g/mol
(NH4)2HPO4: 132.06 g/mol
NH4H2PO4: 115.025 g/mol
Penampilan fizikal
Garam fosfat ammonium berkongsi sama bahawa mereka semua putih. Dengan pengecualian triamonic atau tribasic fosfat ammonium, garam lain tidak menolak bau ammonia dalam keadaan biasa.
Boleh melayani anda: penggantian nukleofilik aromatik: kesan, contohMata Fusion
The (nh4)3PO4 Ia hancur sebelum ia dapat mencairkan. Sementara itu, (NH4)2HPO4 cair pada 155 ºC, dan NH4H2PO4 pada 190 ºC. Titik gabungan terbesar NH4H2PO4 menunjukkan kestabilan yang lebih besar dan ikatan ionik yang lebih kuat.
Mata mendidih
Fail, ketika mereka rosak ketika lebur.
Kelarutan
Garam fosfat ammonium sangat larut dalam air, (NH4)3PO4 Pepejal hygroscopic. Walau bagaimanapun, mereka tidak larut dalam etanol, aseton dan ammonia cecair.
Penguraian
Semua garam fosfat ammonium berpotensi untuk melepaskan ammonia semasa menguraikan. Juga, bergantung kepada intensiti haba, ia dipecah menjadi asid fosforik untuk akhirnya melepaskan gas berbahaya dari nitrogen dan fosforus oksida.
Memperoleh
Garam fosfat ammonium diperolehi oleh tindak balas peneutralan yang berlaku antara asid fosforik dan ammonia:
H3PO4 + 3 nh3 → (NH4)3PO4
Seperti yang dapat dilihat, jika dikehendaki. Umumnya, fosforik oksida digunakan, p2Sama ada5, Sebagai sumber fosforus untuk asid masing -masing.
Semakin banyak h3PO4 berada di sana, yang paling besar akan pengeluaran NH4H2PO4 atau (NH4)2HPO4 (lebih banyak asid) daripada (NH4)3PO4 (lebih asas).
Malah, mereka adalah NH4H2PO4 (Peta, untuk akronim dalam bahasa Inggeris: Monoammonium fosfat) dan (NH4)2HPO4 (DAP) garam fosfat ammonium yang mempunyai nilai komersial yang lebih besar. Sementara itu, (NH4)3PO4 Ia adalah yang kurang dijual, tepat kerana ia adalah yang paling tidak stabil dan, mungkin, yang paling mahal untuk disediakan.
Ia boleh melayani anda: Nombor Avogadro: Sejarah, Unit, Bagaimana Ia Dikira, KegunaanAplikasi
Salah satu kesan segera dari perenggan sebelumnya ialah kebanyakan penggunaan garam fosfat ammonium adalah disebabkan oleh NH4H2PO4 dan (nh4)2HPO4. The (nh4)3PO4, Sebaliknya, ia hampir tidak digunakan, kerana ia terurai dengan cepat.
Baja
 Ammonium fosfat digunakan sebagai baja. Sumber: Pxhere.
Ammonium fosfat digunakan sebagai baja. Sumber: Pxhere. Garam fosfat ammonium adalah baja yang baik, kerana mereka menyediakan dua nutrien penting untuk pembangunan tumbuhan: nitrogen dan fosforus. Di samping itu, mereka larut dalam air, jadi mereka dengan cepat boleh didapati di tanah untuk penyerapan yang sewajarnya melalui akar.
Mereka disimpan tanpa sebarang masalah, dan melainkan jika ada api, mereka tidak melepaskan ammonia, gas yang boleh merosakkan tisu tumbuhan.
Retarders api
 Ammonium fosfat adalah sebahagian daripada beberapa retardan api. Sumber: Hutan Nasional Coconino/CC BY-S (https: // creativeCommons.Org/lesen/by-sa/2.0)
Ammonium fosfat adalah sebahagian daripada beberapa retardan api. Sumber: Hutan Nasional Coconino/CC BY-S (https: // creativeCommons.Org/lesen/by-sa/2.0) Garam fosfat ammonium ketika mengurai melepaskan beberapa gas yang, walaupun berbahaya, menggantikan oksigen dari udara dengan kebakaran penuh. Itulah sebabnya mereka digunakan sebagai retardan kebakaran. Dengan cara ini, kemajuan api diperlahankan atau ditangguhkan.
Optik dan fizikal
NH4H2PO4 Ia digunakan dalam aplikasi optik kerana kristal mereka menunjukkan birefrigance, iaitu, mereka mempunyai pembiasan berganda. Mereka juga mempunyai sifat piezoelektrik, itulah sebabnya mereka digunakan dalam transduser.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2020). Ammonium fosfat. Diperoleh dari: dalam.Wikipedia.org
- Elsevier b.V. (2020). Ammonium fosfat. Scientedirect. Diperoleh dari: Scientedirect.com
- Diane Milner. (4 Februari 2019). Banyak kegunaan ammonium fosfat. Noah Technologies. Pulih dari: maklumat.Noahtech.com
- Pusat Kebangsaan Maklumat Bioteknologi. (2020). Ammonium fosfat tribasic. Pangkalan data PUBCHEM., CID = 57517680. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Milek J.T., Neuberger m. (1972) Ammonium dihydrogen fosfat (ADP). Dalam: Bahan modular elektrooptik linear. Springer, Boston, MA.
- Syarikat Mosaic. (2020). Monoammonium fosfat (peta). Pulih dari: Cropnutrition.com

