Struktur natrium fosfat, sifat, sintesis, kegunaan

- 1035
- 31
- Horace Gulgowski
Dia Natrium fosfat Ia adalah garam bukan organik yang formula kimianya adalah na3PO4. Ia juga menerima nama fosfat yang trisodious (TSP untuk akronim dalam bahasa Inggeris: Trisodium fosfat), atau natrium fosfat tribasic, kerana ia tidak mempunyai keupayaan untuk menderma ion hidrogen h+.
Apabila merujuk kepadanya dengan cara jamak, natrium fosfat, terdapat perbincangan mengenai keseluruhan kompendium garam, terhidrasi atau tidak, berasal dari interaksi elektrostatik antara NA+ dan po43-. Sebahagian daripada garam ini terdiri daripada natrium pirofosfat, atau polimer bukan organik yang mempunyai PO43- sebagai monomer.
 Kaca jam dengan kristal natrium fosfat. Sumber: Ondřej Mangl [Domain Awam]
Kaca jam dengan kristal natrium fosfat. Sumber: Ondřej Mangl [Domain Awam] Itulah sebabnya, melainkan jika spesifikasi dibuat, ia akan selalu merujuk kepada NA3PO4, Dan tidak kepada nah2Po4, na2HPO4, Na4P2Sama ada7 Bukan garam lain.
Imej atas menunjukkan penampilan natrium fosfat, yang kelihatan kristal putih serupa dengan garam atau meja biasa, atau dibeli sebagai serbuk amorf putih. Na3PO4 mampu membentuk beberapa hidrat, menjadi NA3PO4· 12h2Atau yang paling dipasarkan.
Ia dapat digunakan terutamanya dalam industri makanan, dalam detergen, suplemen sukan, dan berfungsi sebagai julap hiperosmotik.
[TOC]
Struktur kimia
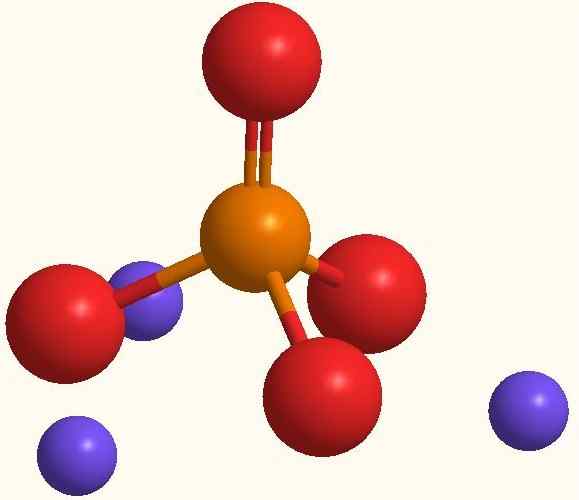 Ion utama natrium fosfat. Sumber: Smolamj melalui Wikipedia.
Ion utama natrium fosfat. Sumber: Smolamj melalui Wikipedia. Formula NA yang sama3PO4 menunjukkan bahawa untuk setiap anion po43- Terdapat tiga kation na+. Ion -ion ini dapat dilihat dalam imej yang unggul. Perhatikan bahawa PO43- Ia mempunyai geometri tetrahedral, dengan atom oksigennya membawa beban negatif resonan, yang menarik NA+ persekitaran.
Juga, formula NA3PO4 Dia menyatakan bahawa ia adalah garam anhydrous, jadi tidak ada molekul air yang termasuk dalam kristal mereka. Tarikan elektrostatik antara NA+ dan po43- Mereka akhirnya menentukan kristal putih trigonal. Pautan ioniknya sedemikian rupa sehingga na3PO4 Ia mempunyai titik gabungan 1583 ºC, jauh lebih tinggi daripada beberapa garam.
Boleh melayani anda: Reaksi Cannizzaro: Ciri, Mekanisme, ContohKedua -dua Na+ Seperti po43- Mereka adalah ion yang boleh dihidrasi pada tahap yang tinggi, tanpa memberi kesan negatif terhadap kestabilan kristal.
Oleh sebab itu, hidrat juga boleh mengkristal; Walau bagaimanapun, titik leburnya lebih rendah daripada garam anhidrat, kerana jambatan hidrogen intermolecular air memisahkan ion dan melemahkan interaksi mereka. Di na3PO4· 12h2Atau, sebagai contoh, titik leburnya ialah 73.4 ºC, jauh lebih rendah daripada NA3PO4.
Sifat
Penampilan fizikal
Ia boleh berlaku seperti kristal putih yang ditakrifkan atau sebagai habuk atau butiran warna yang sama. Semua magnitud fizikal yang dinyatakan di bawah hanya merujuk kepada garam naif3PO4.
Takat lebur
1583 ºC
Takat didih
100 ºC
Kelarutan air
14.5 g/100 ml pada 25 ° C, jadi dianggap sebagai fosfat air yang agak larut. Walau bagaimanapun, ia tidak larut dalam pelarut organik seperti etanol dan karbon disulfida.
Ketumpatan
2,536 g/cm3 pada 17.5 ºC.
Kestabilan
Ia adalah pepejal hygroscopic. Oleh itu, ia mesti disimpan sedemikian rupa sehingga tidak dapat didedahkan kepada kelembapan.
Ph
Ia adalah garam alkali yang kuat. Sebagai contoh, penyelesaian berair 0.1% sudah mempunyai pH 11.5. Harta ini berfungsi untuk digunakan sebagai bahan tambahan dalam detergen.
Sintesis
Bagaimana natrium fosfat dihasilkan atau disintesis? Untuk melakukan ini, ia berdasarkan asid fosforik, h3PO4, atau dari natrium garam fosfat garam, nah2PO4.
Dalam kebanyakan sintesis, H lebih disukai3PO4. Oleh itu, H bertindak balas3PO4 Dengan pangkalan yang meneutralkan tiga kumpulan OH, dengan mengambil kira bahawa asid ini juga boleh ditulis sebagai PO (OH)3.
Boleh melayani anda: keseimbangan subjek: apakah, persamaan umum, jenisAsas dengan keutamaan adalah natrium hidroksida, NaOH (di Jerman), tetapi ia juga berdaya maju (dan lebih murah) untuk menggunakan natrium karbonat atau abu Sosa, Na2Co3 (di Amerika Syarikat). Persamaan untuk kedua -dua tindak balas peneutralan adalah:
Na2Co3 + H3PO4 → NA2HPO4 + Co2 + H2Sama ada
Na2HPO4 + NaOH → NA3PO4 + H2Sama ada
Perhatikan bahawa semasa menggunakan NA2Co3 Na tidak diperoleh3PO4 tetapi na2HPO4, yang memerlukan peneutralan berikutnya. Menjadi reaksi berair, mengkristalisasi NA3PO4· 12h2Atau, jadi ia mesti dikira untuk menghapuskan kandungan airnya dan menyebabkan garam anhydrous.
Na3PO4· 12h2O Ia dicirikan dengan "menggabungkan" kristal mereka dalam jisim padat yang sukar. Semakin kecil saiz kristal mereka, semakin cepat pengiraannya.
Aplikasi
Makanan
 Natrium fosfat digunakan sebagai ejen effervescent untuk mengembangkan peranan atau kek kayu manis. Sumber: Pixabay.
Natrium fosfat digunakan sebagai ejen effervescent untuk mengembangkan peranan atau kek kayu manis. Sumber: Pixabay. Dalam natrium fosfat menggunakannya tidak dapat dielakkan untuk mencampurkan NA3PO4 atau na3PO4· 12h2Atau, kerana yang terakhir adalah hidrat yang paling dipasarkan. Sebagai contoh, kedua -dua daripada kedua -dua mereka memberikan ion -ion yang tidak berbahaya (teori) kepada makanan yang mereka tambah, memperkayakan mereka fosfat dan pada masa yang sama meningkatkan kemasinan mereka.
Dalam salar daging, NA3PO4· 12h2Atau dimasukkan untuk memastikan mereka segar lebih lama semasa simpanan mereka. Ia juga ditambah sebagai ejen pengemulsi supaya campuran air minyak tidak "dipotong", tetapi tetap bersatu; Dan sebagai pengawal selia pH, kerana ia membantu mengurangkan keasidan makanan (termasuk bijirin).
Boleh melayani anda: kalsium silikat: sifat, struktur, mendapatkan, menggunakanDi samping itu, ia digunakan untuk menebal beberapa sos tomato, dan untuk baking kek atau roti (imej unggul). Yang terakhir adalah kerana na3PO4· 12h2Atau cenderung melepaskan wap air, yang meningkatkan saiz liang -liang jisim tepung dan jumlah yang sama.
Detergen
Natrium fosfat cukup asas untuk menghidupkan beberapa lemak atau minyak yang anda hubungi. Kealkaliannya kemudiannya digunakan untuk meningkatkan tindakan detergen, selagi permukaan kepada penderitaan bukan logam, kerana mereka dapat merosotnya.
Walau bagaimanapun, pengeluaran detergen yang diperkaya dengan fosfat telah dikurangkan kerana mereka menghasilkan eutrophication tasik dan sungai dan, dengan itu, percambahan alga yang meliputi permukaan mereka.
Ia juga telah digunakan untuk penjelasan disinfektan: na3PO4· 1/4Naocl · 11h2Atau, yang disediakan menggunakan natrium hypochlorite, naocl, bukan naOH atau na2Co3 Untuk meneutralkan h3PO4.
Ubat
Na3PO4 Ia mendorong pembuangan air dengan bertindak sebagai pencahayaan hiperosmotik, perlu membersihkan kolon sebelum pesakit menjalani kolonoskopi. Sebaliknya, ia juga telah digunakan (ditambah) dalam suplemen tenaga.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Pusat Kebangsaan Maklumat Bioteknologi. (2019). Trisodium fosfat. Pangkalan data PUBCHEM. CID = 24243. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Wikipedia. (2019). Trisodium fosfat. Diperoleh dari: dalam.Wikipedia.org
- Curran m.P. & Plosker g.L. (2004). Penyelesaian natrium fosfat oral: Kajian semula kegunaannya kepada pembersih kolorektal. Doi: 10.2165/00003495-200464150-00009
- Corey Whelan. (22 Disember 2017). Natrium fosfat. Pulih dari: kesihatan.com
- Jacobs, Joel B. Taborosi, Steve. (2019). Proses untuk pengeluaran trisodium fosfat. Diperolehi dari: freepatentssonline.com
- Maryann Marks. (2018). Mengapa trisodium fosfat (TSP) ditambah kepada makanan kita? Pulih dari: Theingredientguru.com

