Galvanplasty

- 938
- 192
- Ms. Santos Fritsch
Kami menerangkan apa yang terdiri daripada galvanoplasti, juga dipanggil elektrodeposisi, bagaimana prosesnya, contoh praktikal dan aplikasinya.
 Galvanoplasti sudu
Galvanoplasti sudu Apa itu galvanoplasti?
Galvanoplasti atau elektrodeposisi adalah teknik elektrokimia yang terdiri daripada namanya, dalam mendepositkan lapisan logam pada objek menerima; Iaitu, meliputi mereka dari penutup logam, yang ketebalannya berkisar antara 5-20 μm.
Teknik ini juga dikenali sebagai elektrochapado atau bersalut elektrolitik, sebagai medium elektrolitik yang terdiri daripada ion logam logam yang dikehendaki untuk disimpan sangat diperlukan untuk pelaksanaannya. Oleh itu, jika kita mahukan tembaga bersalut (tembaga), kita akan memerlukan garam larut tembaga, seperti tembaga sulfat, dibubarkan di dalam air.
Penalaran sebelumnya digunakan untuk logam lain: bersalut elektrolitik emas akan memerlukan garam emas, biasanya sianida emas, yang boleh menjadi sangat toksik. Oleh itu, beberapa objek, seperti peralatan makan, boleh dilapisi dengan emas untuk memberikan nilai dan bangsawan yang lebih besar.
Tetapi galvanoplasti melampaui estetika: mereka dianugerahkan. Ia juga membolehkan penjimatan sumber semula jadi, kerana tidak perlu menghabiskan banyak logam untuk lapisan.
Proses galvanoplasti
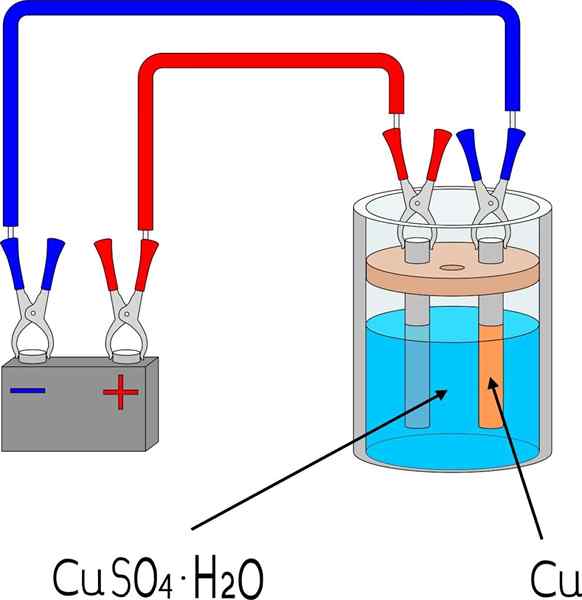 Elektrodeposisi tembaga di bilik mandi sulfat tembaga
Elektrodeposisi tembaga di bilik mandi sulfat tembaga Item
Untuk elektrodepose logam di permukaan, beberapa elemen asas diperlukan, yang dimensi dan modnya akan berbeza -beza bergantung kepada kumpulan objek yang akan ditutup.
Di bahagian atas, contohnya, elektrod tembaga kecil -skala ditunjukkan, boleh dihasilkan semula di mana -mana makmal atau ruang.
Medium elektrolitik
Pertama, medium elektrolit logam ke elektrodeposit diperlukan. Garam sulfat tembaga, CUO4, Ia sangat larut dalam air, jadi ia membawa ion cu2+ yang kemudiannya akan dikurangkan ke atom CU0. Atom ini adalah yang akan dipasang di permukaan penerimaan untuk menimbulkan kristal logam.
Medium elektrolitik sangat diperlukan untuk litar berfungsi dan beban ionik boleh bergerak atau menggerakkan ke arah rantau di mana elektrodeposisi berlaku.
Elektrod
Elektrod adalah permukaan di mana elektrodeposisi berlaku dari pangkalan kimianya. Secara ringkas terdapat dua elektrod: katod, di mana logam adalah elektrodepos; Dan anod, di mana tindak balas kimia berlaku yang menyumbangkan elektron kepada ion logam yang akan meliputi katod.
Ia boleh melayani anda: urethane: struktur, sifat, mendapatkan, menggunakanIaitu, katod menjadi bahagian yang dikehendaki. Sementara itu, anod adalah permukaan di mana spesies mengoksidakan dan menyumbangkan elektronnya ke katod. Banyak kali anod diperbuat daripada logam yang sama yang dibubarkan dalam persekitaran elektrolitik. Sekiranya terdapat ionik tembaga di tengah, dalam hal ini anod akan menjadi tembaga logam.
Litar luaran
Litar luaran adalah bateri yang menyediakan elektron awal yang mempromosikan elektrodeposisi. Kehadirannya bermaksud bahawa tindak balas tidak spontan: elektrik diperlukan untuk menghasilkan perubahan kimia, iaitu pengurangan ion logam terlarut.
Pembersihan elektrod
Bahagian yang akan dilindungi mesti bersih sepenuhnya. Jika tidak, pelapisan atau salutan akan rosak.
Untuk melakukan ini, anda perlu memastikan bahawa permukaannya sepenuhnya hidrofilik, iaitu, ia tidak mempunyai lemak atau kotoran. Salah satu cara untuk memastikan ini, selepas mencuci bahan kimia, adalah membasahi sekeping dengan air, dan jika pembentukan air jatuh atau penurunan cecair yang tidak berwarna tidak diperhatikan, ini bermakna elektrod belum bersih.
Reaksi dan makna elektron
Galvanoplasti adalah reaksi redoks. Oleh itu: satu spesies mesti dikurangkan, sementara yang lain dioksidakan, atau sebaliknya. Dalam tembaga, kita mempunyai anod yang diperbuat daripada tembaga, dan katod yang diperbuat daripada logam saya (besi, zink, timah, dll.).
Apabila kita menghidupkan bateri, mereka akan mengalir elektron ke katod, yang mula mengecas secara negatif.
Beban negatif katod menarik Cation Cu2+ persekitaran elektrolitik, berlaku pengurangan:
Cu2+(Ac) +2e- → Cu (s)
Ia dapat melayani anda: Reaksi MaillardBateri perlu memulihkan elektron yang disumbangkan, dan juga ion Cu mesti pulih2+ dikurangkan untuk mengekalkan berkecuali persekitaran elektrolisis. Ini adalah apabila anod datang dalam fungsi: atom tembaga mengoksidakan:
Cu (s) → Cu2+(Ac) +2e-
Dan elektron yang dikeluarkan diarahkan kembali ke bateri, yang seterusnya menggerakkannya ke arah katod untuk meneruskan elektrodeposisi.
Anod mendapat beban positif, yang menarik ion SO42- dari medium elektrolitik (lihat gambar sekali lagi).
Iaitu, tindak balas yang berlaku adalah pengurangan dan pengoksidaan tembaga, logam yang elektrodepos:
Cu2+(Ac) +2e- → Cu (s)
Cu (s) → Cu2+(Ac) +2e-
Anod, tembaga, kehilangan adunan sementara katod, logam lain, ditutup dengan lapisan coppery halus.
Contoh galvanoplasti
Perak
Logam boleh menjadi "elektroplat", yang secara elektrik meliputi mereka dari lapisan perak. Ini amat bermanfaat dalam komponen elektronik yang mesti menjalankan elektrik. Perak boleh menjadi elektrodeposita pada keluli, tembaga, nikel dan logam lain.
Tinned
Tinner adalah elektrodeposisi timah. Ia sangat berguna dalam pengeluaran tin besi, yang ditutup dengan timah untuk menjadikannya tahan terhadap kakisan, dan dengan itu tidak merosakkan makanan atau produk yang disimpan.
Latin atau tan
Walaupun sedikit lebih rumit, tembaga dan gangsa juga boleh menjadi elektrodepos pada beberapa logam untuk meningkatkan penampilan mereka.
Zincado
Zink atau zink galvanoplasti (tidak mengelirukan dengan termal tergalvani) kebanyakannya digunakan untuk memberikan ketahanan besi kepada kakisan dan permukaan yang lebih cerah dan lebih menarik. Oleh itu, fungsinya adalah estetika dan pada masa yang sama berfungsi, dan terdapat di bahagian badan seperti roda.
Plastik logam
Plastik, sebelum ini dirawat untuk mempunyai permukaan konduktif, juga boleh ditutup dengan logam, yang seolah -olah mereka dipatuhi selimut aluminium.
Boleh melayani anda: Kitasato FlaskAplikasi galvanoplasti
Aplikasi galvanplasti atau elektrodeposisi boleh dibahagikan kepada fungsi atau estetik.
Berfungsi
 Elektrodepos emas nipis dalam penonton kes -kes angkasawan membolehkan mereka melindungi mata mereka dari cahaya matahari
Elektrodepos emas nipis dalam penonton kes -kes angkasawan membolehkan mereka melindungi mata mereka dari cahaya matahari Salutan sekeping atau objek adalah untuk menyediakan permukaannya dengan sifat -sifat yang semata -mata kekurangan. Sebagai contoh, elektrik tembaga atau emas membuat kepingan yang mereka ada, jadi ia sesuai dengan litar elektronik untuk memanfaatkan sifat -sifat logam ini, tanpa perlu menghabiskan banyak emas pada pembuatan keseluruhan dan pepejal.
Emas, sebaliknya, melindungi permukaan haba dan radiasi. Oleh sebab itu, ia digunakan secara meluas dalam satelit dan di topi keledar angkasawan, kerana ia mencerminkan cahaya matahari sehingga memusnahkan mata mereka, atau dengan cepat panas.
Keluli krom atau nicken sangat tahan terhadap kakisan terima kasih tepat pada lapisan logam ini. Itulah sebabnya galvanoplasti digunakan dalam industri untuk melindungi logam yang sensitif terhadap koroden.
Estetika
Venir logam bersinar. Zink, nikel dan kromium banyak digunakan untuk tujuan ini. Juga, emas dan perak adalah elektrodepos dalam cincin, rantai, gelang, chokers, cerun, dll., Dan oleh itu galvanoplasti beliau mendapati banyak aplikasi di kedai perhiasan dan hiasan, untuk meningkatkan imej dan prestij pakaian ini.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Wikipedia. (2021). Electroplating. Diperoleh dari: dalam.Wikipedia.org
- Chris Woodford. (28 Julai 2020). Bagaimana kerja elektroplating. Diperolehi dari: jelas.com
- Rob Snyder. (s.F.). Electrodeposition nanoscale. Institut Pendidikan STEM. [Pdf]. Pulih dari: nanoscale.UNL.Edu
- Elsevier b.V. (2021). Electrodeposition. Scientedirect. Diperoleh dari: Scientedirect.com
- Vaishali Mittal. (10 Disember 2020). Electroplating. Kimia Librettexts. Pulih dari: chem.Libretxts.org
- Singh Davneet. (9 Jun, 2020). Pelbagai jenis elektropling. Pulih dari: Teachoo.com
- Helmestine, Anne Marie, Ph.D. (26 Ogos, 2020). Apa itu elektroplating dan bagaimana ia berfungsi? Pulih dari: Thoughtco.com

