Sifat hidrokarbon alifatik, tatanama, reaksi, jenis

- 3570
- 718
- Kerry Schmitt
The Hidrokarbon alifatik Mereka semua adalah mereka yang kurang aromatik, bukan dalam erti kata penciuman, tetapi berkenaan dengan kestabilan kimia. Mengklasifikasikan hidrokarbon dengan cara ini hari ini terlalu samar -samar dan tidak tepat, kerana ia tidak mendiskriminasi antara pelbagai jenis hidrokarbon yang tidak aromatik.
Oleh itu, kita mempunyai hidrokarbon alifatik dan hidrokarbon aromatik. Yang terakhir diiktiraf oleh unit asas mereka: cincin benncénico. Yang lain, sebaliknya, boleh mengguna pakai struktur molekul: linear, bercabang, kitaran, tak tepu, polycyclical; selagi mereka tidak mempunyai sistem konjugasi seperti benzena.
 Bahan api cecair pemetik api terdiri daripada campuran hidrokarbon alifatik. Sumber: Pixnio.
Bahan api cecair pemetik api terdiri daripada campuran hidrokarbon alifatik. Sumber: Pixnio. Istilah 'alifatik' dilahirkan dari perkataan Yunani 'aleiphar', yang bermaksud lemak, juga digunakan untuk merujuk kepada minyak. Oleh itu, pada abad kesembilan belas klasifikasi ini diberikan kepada hidrokarbon yang diperoleh dari ekstrak berminyak; Walaupun hidrokarbon aromatik diekstrak dari pokok dan resin wangi.
Walau bagaimanapun, sebagai asas kimia organik yang disatukan, didapati bahawa terdapat harta kimia yang membezakan hidrokarbon, bahkan lebih penting daripada sumber semula jadi mereka: aromatik (dan bukan wangian).
Dengan cara ini, hidrokarbon alifatik tidak lagi menjadi yang diperolehi daripada lemak, untuk menjadi semua aromatik yang kurang. Di dalam keluarga ini kita mempunyai alkenes dan alkynes, tanpa mengira sama ada mereka linear atau kitaran. Itulah sebabnya 'alifatik' dianggap tidak tepat; Walaupun berguna untuk menangani beberapa aspek umum.
Contohnya, apabila dikatakan 'ekstrem' atau 'rantai' rantaian, kawasan molekul disebutkan di mana cincin aromatik tidak hadir. Dari semua hidrokarbon alifatik, definisi paling mudah adalah metana, CHO4; Walaupun benzena adalah hidrokarbon aromatik yang paling mudah.
[TOC]
Sifat hidrokarbon alifatik
Sifat -sifat hidrokarbon alifatik berayun dalam darjah yang berbeza bergantung pada mana yang dipertimbangkan. Terdapat massa molekul yang rendah dan tinggi, serta linear, bercabang, kitaran atau polycyclical, bahkan struktur tiga dimensi yang menakjubkan; Seperti Kuba, dalam bentuk kiub.
Walau bagaimanapun, terdapat beberapa umum yang boleh disebutkan. Sebilangan besar hidrokarbon alifatik adalah gas hidrofobik dan apolar atau cecair, mempunyai lebih banyak apolar daripada yang lain, kerana walaupun mereka yang rantai karbonnya mempunyai halogen, oksigen, nitrogen atau atom sulfur dimasukkan ke dalam senarai.
Boleh melayani anda: boron: sejarah, sifat, struktur, kegunaanMereka juga boleh terbakar, kerana mereka terdedah kepada pengoksidaan di udara sebelum sumber haba minimum. Ciri ini menjadi lebih berbahaya jika kita menambah turun naik yang tinggi, disebabkan oleh interaksi penyebaran yang lemah yang mengekalkan molekul alifatik.
Contohnya kita melihatnya di butana, gas yang boleh dicairkan dengan kemudahan relatif serta propana. Kedua -duanya sangat tidak menentu dan mudah terbakar, jadi mereka adalah komponen aktif gas dapur atau pemetik poket.
Sudah tentu, turun naik sedemikian cenderung berkurangan kerana jisim molekul dan hidrokarbon menyebabkan lebih banyak cecair likat.
Nomenclature
Nomenklatur hidrokarbon berbeza lebih daripada sifatnya. Sekiranya mereka adalah alko atau alkina, piawaian yang sama yang ditetapkan oleh IUPAC diikuti: pilih rantai terpanjang, memberikan petunjuk terendah ke hujung yang paling diganti atau ke heteroatomes atau lebih banyak kumpulan reaktif.
Dengan cara ini anda tahu di mana karbon setiap substituen dijumpai, atau bahkan tidak tepu (pautan berganda atau tiga). Dalam kes hidrokarbon kitaran, nama itu didahului oleh substituen yang disenaraikan dalam susunan abjad, diikuti dengan perkataan 'kitaran', mengira nombor karbon yang mengintegrasikannya.
Sebagai contoh, pertimbangkan dua siklohexans berikut:
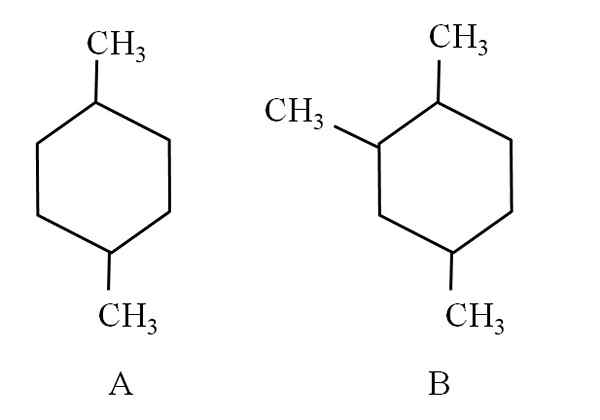 Dua siklohexans, yang diklasifikasikan sebagai hidrokarbon alifatik. Sumber: Gabriel Bolívar.
Dua siklohexans, yang diklasifikasikan sebagai hidrokarbon alifatik. Sumber: Gabriel Bolívar. Cyclohexan A, dipanggil 1.4-dimetilciclohexan. Sekiranya cincin itu adalah lima karbon, ia akan menjadi 1.4-dimetilciclopentano. Sementara itu, Cyclohexan B dipanggil 1,2,4-Trimethylcyclohexan, dan bukan 1,4,6-Cyclohexan, kerana ia bertujuan untuk menggunakan petunjuk terendah.
Sekarang, tatanama boleh menjadi sangat rumit untuk struktur operabotik hidrokarbon. Bagi mereka terdapat peraturan yang lebih spesifik, yang mesti dijelaskan secara berasingan dan berhati -hati; Seperti matlamat, terpenes, dasar, dan sebatian polycyclic.
Reaksi
Pembakaran
Nasib baik, reaksi kurang bervariasi untuk hidrokarbon ini. Salah seorang daripada mereka telah disebutkan: mereka mudah membakar, menghasilkan karbon dioksida dan air, sebagai tambahan kepada oksida atau gas lain bergantung kepada kehadiran heteroatomes (Cl, N, P, O, dll.). Walau bagaimanapun, CO2 dan h2Atau merupakan produk pembakaran utama.
Tambahan
Sekiranya mereka tidak mempunyai restri, mereka mungkin mengalami tindak balas tambahan; iaitu, mereka menggabungkan molekul kecil ke dalam kerangka mereka sebagai substituen mengikuti mekanisme tertentu. Di antara molekul -molekul ini kita mempunyai air, hidrogen dan halogen (f2, Cl2, Br2 dan saya2).
Halogenasi
Sebaliknya, hidrokarbon alifatik di bawah kejadian radiasi ultraviolet (Hv) dan haba boleh memecahkan pautan C-H untuk mengubahnya dengan pautan C-X (C-F, C-CL, dll.). Ini adalah tindak balas halogenasi, yang diperhatikan dalam alkana rantai yang sangat pendek, seperti metana atau pentan.
Boleh melayani anda: nitrit: sifat, struktur, tatanama, pembentukanCraqueo
Reaksi lain yang boleh diderita oleh alifatik, terutamanya alkana rantai panjang, adalah retak haba. Ia terdiri daripada bekalan haba yang sengit supaya tenaga terma memecahkan ikatan C-C, dan dengan itu molekul kecil, lebih banyak disebutkan dalam pasaran bahan bakar, dari molekul besar dibentuk.
Empat reaksi di atas adalah yang utama yang mungkin mengalami hidrokarbon alifatik, pembakaran menjadi yang paling penting dari semua, kerana ia tidak mendiskriminasi terhadap mana -mana sebatian; Semua akan terbakar dengan kehadiran oksigen, tetapi tidak semua orang akan menambah molekul atau memecah masuk ke molekul kecil.
Lelaki
Kumpulan hidrokarbon alifatik Kumpulan tidak berkesudahan, yang seterusnya diklasifikasikan lebih spesifik, menunjukkan tahap ketidakpatuhan mereka, serta jenis struktur yang mereka ada.
Mengikut bagaimana mereka tidak tepu, kita mempunyai alkana (tepu), alkenes dan alkynes (tak tepu).
Alkanes dicirikan dengan mempunyai pautan C-C yang mudah, manakala dalam alkena dan alkina kita melihat pautan c = c dan c≡C, masing-masing. Cara yang sangat umum untuk memvisualisasikannya adalah memikirkan kerangka karbon alkana sebagai zigzagen dan rantai dilipat, menjadi "persegi" untuk alkenes, dan "garis lurus" untuk alkina.
Ini kerana ikatan berganda dan tiga mempunyai tenaga dan sekatan stenrik dalam putaran mereka, "mengeraskan" struktur mereka.
Alkitos dan Alkin boleh bercabang, kitaran atau poliklik. Itulah sebabnya cycloalcanos, cycloalquenos, sikloalquinos, dan sebatian seperti decalin (struktur basikal), adamantano (serupa dengan topi besbol), heptalena, gonano, antara lain, hidrokarbon alifatik juga dianggap.
Dari Alkenes jenis hidrokarbon lain timbul, seperti matlamat (dengan dua ikatan berganda), polienous (dengan banyak bon alternatif berganda), dan terpenes (sebatian yang diperoleh dari isoprena, diena).
Aplikasi
Sekali lagi, kegunaan untuk hidrokarbon ini boleh berbeza -beza bergantung pada mana yang dipertimbangkan. Walau bagaimanapun, di bahagian sifat dan reaksi telah dijelaskan bahawa semua pembakaran, bukan sahaja untuk melepaskan molekul gas, tetapi juga cahaya dan panas. Oleh itu, mereka adalah takungan tenaga, berguna untuk berfungsi sebagai bahan api atau sumber haba.
Itulah sebabnya mereka digunakan sebagai sebahagian daripada komposisi petrol, untuk gas asli, dalam pemetik api bunsen, dan secara umum dapat berasal dari api.
Boleh melayani anda: peraturan oktetSalah satu contoh yang paling luar biasa ialah acetylene, HC≡CH, yang pembakarannya membolehkan untuk merangsang ion logam sampel dalam spektrometri penyerapan atom yang dilakukan pada ujian analisis. Begitu juga, api yang dihasilkan dapat digunakan untuk kimpalan.
Hidrokarbon alifatik cecair, seperti parafinik, sering digunakan sebagai pelarut pengekstrakan lemak. Di samping itu, tindakan pelarutnya boleh digunakan untuk menghilangkan bintik -bintik, enamel, lukisan, atau hanya untuk menyediakan penyelesaian sebatian organik tertentu.
Jisim molekul terbesar, sudah likat atau pepejal, ditakdirkan untuk penjelasan resin, polimer atau ubat.
Berkenaan dengan istilah 'alifatik', biasanya digunakan untuk merujuk kepada kawasan tersebut, dalam makromolekul, yang kekurangan aromatik. Sebagai contoh, asfalten digambarkan secara dangkal sebagai nukleus aromatik dengan rantai alifatik.
Contoh
Pada mulanya dikatakan bahawa metana adalah yang paling mudah dari hidrokarbon alifatik. Mereka diikuti oleh propana, cho3Ch2Ch3, Butano, ch3Ch2Ch2Ch3, Pentano, Ch3Ch2Ch2Ch2Ch3, oktana, nonano, dekan, dan sebagainya, mempunyai alkana yang semakin panjang.
Perkara yang sama berlaku untuk etilena, CHO2= Ch2, Propeno, ch3CH = CH2, Buteno, ch3Ch2CH = CH3, Dan untuk seluruh Alkin. Sekiranya terdapat dua ikatan berganda, mereka adalah oley, dan jika terdapat lebih daripada dua, polienas. Begitu juga, mungkin terdapat pautan berganda dan tiga dalam kerangka yang sama, meningkatkan kerumitan struktur.
Di antara sikloalcanos kita boleh menyebutkan siklopropane, siklobutane, cyclopentano, siklohexan, cycloheptano, cyclooctane, serta cyclohexen dan cyclohexin. Dari semua hidrokarbon ini, derivatif bercabang diperolehi, mengalikan contoh yang ada (seperti 1.4-dimetilciclohexano).
Daripada terpenes yang paling mewakili kita mempunyai limonene, mentol, pinene, vitamin A, escualeno, dll. Polietilena adalah polimer tepu dengan unit -ch2-Ch2-, Oleh itu, ia juga merupakan contoh hidrokarbon ini. Contoh lain telah disebutkan di bahagian sebelumnya.
Rujukan
- Morrison, r. T. dan Boyd, R, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. Amina. (Edisi ke -10.). Wiley Plus.
- Helmestine, Anne Marie, Ph.D. (22 Ogos 2019). Definisi hidrokarbon alifatik. Pulih dari: Thoughtco.com
- Wikipedia. (2019). Sebatian alifatik. Diperoleh dari: dalam.Wikipedia.org
- Kimia Librettexts. (20 Ogos 2019). Hidrokarbon alifatik. Pulih dari: chem.Libretxts.org
- Elizabeth Wyman. (2019). Hidrokarbon alifatik: Definisi & sifat. Kajian. Pulih dari: belajar.com
- « Dimensi Sosial Menjadi Manusia, Pendidikan, Pengetahuan, Kanan, Kesihatan
- 100 data haiwan yang ingin tahu »

