Molekul apolar
- 4921
- 724
- Clarence Greenholt DDS
The Molekul apolar Mereka adalah yang hadir dalam struktur mereka pengagihan simetri elektron mereka. Ini mungkin jika perbezaan elektronegativiti atomnya kecil, atau jika atom atau kumpulan elektronegatif membatalkan kesannya pada molekul.
Tidak selalunya "apolariti" adalah mutlak. Atas sebab itu, molekul polariti yang lemah dianggap sebagai apolar; iaitu, ia mempunyai momen dipole μ hampir 0. Di sini anda memasuki medan relatif: berapa rendah harus μ supaya molekul atau sebatian dianggap apolar?
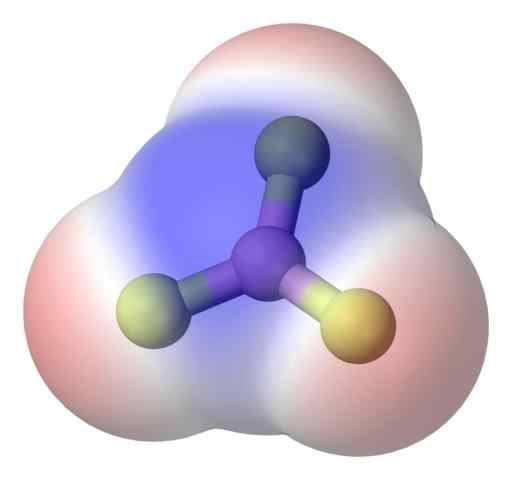
 BF3 Apolar Molekul. Sumber: Benjah-bmm27 melalui Commons Wikimedia.
BF3 Apolar Molekul. Sumber: Benjah-bmm27 melalui Commons Wikimedia. Untuk menangani masalah ini, anda mempunyai molekul boron trifluoride, bf3 (gambar atas).
Atom fluorin jauh lebih elektronegatif daripada Boro, dan oleh itu pautan B-F adalah kutub. Walau bagaimanapun, molekul BF3 Ia adalah simetri (satah trigonal) dan melibatkan pembatalan vektor tiga momen b-f.
Oleh itu, molekul apolar juga dihasilkan, walaupun dengan kewujudan pautan kutub. Polariti yang dihasilkan boleh seimbang dengan kewujudan pautan kutub yang lain, magnitud yang sama seperti yang sebelumnya, tetapi berorientasikan ke arah yang bertentangan; seperti yang berlaku di bf3.
Ciri -ciri molekul apolar
Simetri
Agar kesan pautan kutub untuk membatalkan satu sama lain, molekul mesti mempunyai struktur geometri tertentu; Contohnya, linear, yang paling mudah difahami pada pandangan pertama.
Ini adalah kes karbon dioksida (CO2), yang mempunyai dua pautan kutub (o = c = o). Ini kerana kedua -dua momen dipole pautan c = o dibatalkan apabila seseorang berorientasikan ke satu sisi, dan yang kedua ke arah yang lain, pada sudut 180 °.
Boleh melayani anda: transaminasiOleh itu, salah satu ciri pertama yang perlu diambil kira apabila "apolariti" molekul dinilai oleh penerbangan burung, adalah untuk memerhatikan bagaimana simetri itu.
Katakan bahawa bukan co2 Anda mempunyai molekul cos (o = c = s), yang dipanggil karbonil sulfida.
Kini ia tidak lagi molekul apolar, kerana elektronegativiti sulfur kurang daripada oksigen; Dan oleh itu, momen dipole c = s adalah berbeza dari c = o. Akibatnya, COS adalah molekul kutub (kutub adalah tepung karung lain).
Imej yang lebih rendah secara grafik meringkaskan semua yang baru diterangkan:
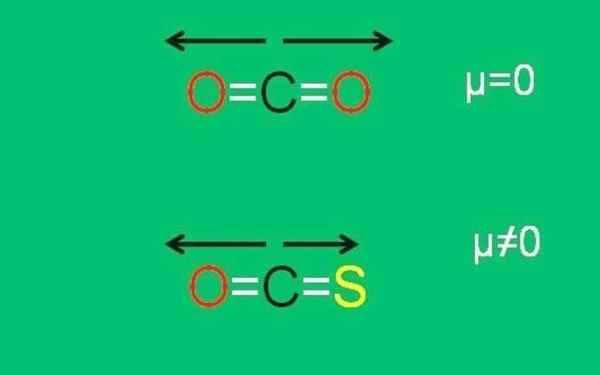 XXX Dipolar Moments of the CO2 dan COS molekul. Sumber: Gabriel Bolívar.
XXX Dipolar Moments of the CO2 dan COS molekul. Sumber: Gabriel Bolívar. Perhatikan bahawa momen dipole pautan c = s kurang daripada pautan c = o dalam molekul cos.
Elektronegativiti
Electronegativity pada skala Pauling mempunyai nilai antara 0.65 (untuk Francio), dan 4.0 (untuk fluorida). Secara umum, halogen mempunyai elektronegativiti yang tinggi.
Apabila perbezaan elektronegativiti unsur -unsur yang membentuk ikatan kovalen kurang dari 0.4, dikatakan bahawa ia adalah apolar atau tidak kutub. Walau bagaimanapun, satu-satunya molekul yang benar-benar apolar adalah yang dibentuk oleh hubungan antara atom yang sama (seperti hidrogen, H-H).
Kuasa intermolecular
Untuk bahan untuk membubarkan di dalam air, ia mesti berinteraksi secara elektrostatik dengan molekul; interaksi yang tidak dapat melakukan molekul apolar.
Dalam molekul apolar, caj elektrik mereka tidak terkurung pada satu hujung molekul, tetapi diedarkan secara simetri (atau homogen). Oleh itu, dia tidak dapat berinteraksi melalui pasukan dipole-dipolo.
Boleh melayani anda: volume atomSebaliknya, molekul apolar berinteraksi antara satu sama lain melalui daya penyebaran London; Ini adalah, dipole segera yang memolarisasi awan elektronik atom molekul jiran. Di sini jisim molekul adalah faktor utama dalam sifat fizikal molekul ini.
Cara mengenal pasti molekul apolar?
-Mungkin salah satu kaedah terbaik untuk mengenal pasti molekul apolar adalah kelarutannya dalam pelarut kutub yang berbeza, secara amnya sedikit larut di dalamnya.
-Secara umum, molekul apolar adalah sifat gas. Mereka juga boleh menjadi cecair yang tidak dapat dilepaskan dengan air.
-Pepejal apolar dicirikan dengan lembut.
-Daya penyebaran yang menyatukan mereka biasanya lemah. Kerana ini, titik lebur atau mendidih cenderung lebih rendah daripada sebatian kutub.
-Molekul apolar, terutamanya dalam bentuk cecair, adalah konduktor elektrik yang buruk, kerana mereka tidak mempunyai caj elektrik bersih.
Contoh molekul apolar
Gas mulia
Walaupun mereka bukan molekul, gas mulia dianggap apolar. Jika diandaikan bahawa dua atomnya berinteraksi untuk tempoh masa yang singkat, interaksi ini boleh dipertimbangkan (separuh) sebagai molekul; molekul yang akan menjadi sifat apolar.
Molekul diatomik
Molekul diatomik, seperti h2, br2, i2, Cl2, o2, dan f2, Mereka adalah apolar. Ini secara amnya2, A-a.
Hydrocarbons
Bagaimana jika ia adalah sekumpulan atom? Ia akan berlaku sebelum sebatian apolar lain; Contohnya, Ethane, Cho3-Ch3, Kerangka karbon yang linear, C-C.
Metano, Ch4, dan etana, c2H6, Mereka adalah molekul apolar. Karbon mempunyai elektronegativiti sebanyak 2.55; Walaupun elektronegativiti hidrogen adalah 2.2. Oleh itu, terdapat vektor dipole intensiti rendah, berorientasikan dari hidrogen ke karbon.
Ia boleh melayani anda: Kaedah Mohr: Asas, Reaksi, Prosedur, KegunaanTetapi, disebabkan oleh simetri geometri molekul metana dan etana, jumlah vektor dipole atau momen dipole dalam molekul mereka tidak sah, jadi tidak ada beban bersih dalam molekul.
Secara umum, perkara yang sama berlaku dengan semua hidrokarbon, dan walaupun terdapat ketidakpastian di dalamnya (ikatan berganda dan tiga), mereka dianggap apolar atau sebatian polariti rendah. Juga, hidrokarbon siklik adalah molekul apolar, seperti siklohexan atau siklobutane.
Yang lain
Molekul Karbon Dioksida (CO2) dan disulfida karbon (CS2) Mereka adalah molekul apolar, kedua -duanya dengan geometri linear.
Dalam karbon disulfida, elektronegativiti karbon adalah 2.55, manakala elektronegativiti sulfur adalah 2.58; Oleh itu, kedua -dua elemen mempunyai, praktikal, elektronegativiti yang sama. Tidak ada generasi vektor dipole dan oleh itu, beban bersih adalah sifar.
Juga, molekul CCL berikut tersedia4 dan albr3, kedua -dua apolar:
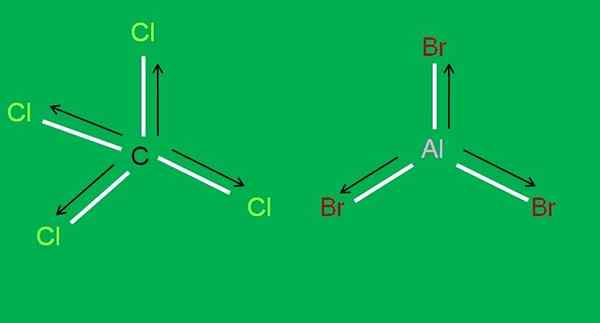 Molekul CCL4 dan ALBR3. Sumber: Gabriel Bolívar.
Molekul CCL4 dan ALBR3. Sumber: Gabriel Bolívar. Dalam tribromida aluminium, albb3 Perkara yang sama berlaku dengan bf3, Pada permulaan artikel. Sementara itu, untuk karbon tetraklorida, CCL4, Geometri tetrahedral dan simetri, kerana semua pautan C-CL adalah sama.
Begitu juga, molekul dengan formula cx umum4 (Cf4, Ci4 dan CBR4), mereka juga apolar.
Dan akhirnya, molekul apolar bahkan boleh mempunyai geometri octahedral, seperti halnya dengan sulfur hexafluoride, SF6. Malah, anda boleh mempunyai sebarang geometri atau struktur, selagi ia simetri dan pengedaran elektroniknya adalah homogen.
Rujukan
- Molekul nonpolar. Pulih dari: kimia.Tutorvista.com
- Contoh molekul kutub dan nonpolar. Pulih dari: Thoughtco.com
- « Keseimbangan perkara apa, persamaan umum, jenis
- Daniel Servitje Montull Biografi, Kepimpinan dan Sumbangan »

