Struktur pepejal kristal, sifat, jenis, contoh

- 793
- 75
- Erick Krajcik
The pepejal kristal Mereka adalah mereka yang struktur mikroskopik diperintahkan dan mematuhi corak tersendiri untuk rangkaian kristal tertentu; Contohnya: kubik, heksagon, triclinic, rhomboédrica, antara lain.
Dikatakan bahawa pepejal ini wujud sebagai kristal, yang menunjukkan aspek dan reka bentuk geometri yang mencerminkan bagaimana diperintahkan di dalamnya. Contoh lain pepejal kristal adalah berlian, kuarza, anthracene, ais kering, kalium klorida atau magnesium oksida.
 Bar kristal jenayah. Sumber: Pixabay.
Bar kristal jenayah. Sumber: Pixabay. Sepasang pepejal kristal yang sangat terkenal ialah gula dan garam (NaCl). Pada pandangan pertama, kedua -duanya memakai kristal putih; Tetapi sifatnya sangat berbeza. Gula adalah pepejal kristal molekul, manakala garam adalah pepejal kristal ionik. Yang pertama terdiri daripada molekul sukrosa; Dan yang kedua, dari ion+ dan Cl-.
Imej atas membolehkan anda melihat bagaimana kristal gula terang. Kristal garam namun mereka tidak jauh di belakang. Walaupun gula dan garam kelihatan seperti saudara -saudara, struktur mereka berbeza: gula, yang menjadi sukrosa, mempunyai struktur monoklinik; Semasa garam, struktur padu.
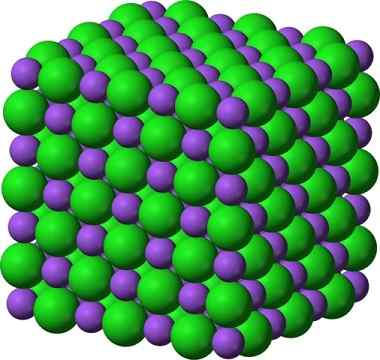 Struktur kristal natrium klorida, NaCl
Struktur kristal natrium klorida, NaCl Disembur gula dan garam (glas) kekal kristal; Kristalnya hanya menjadi lebih kecil untuk mata kita. Oleh itu, kristal pepejal ditakrifkan lebih banyak oleh struktur dalamannya, daripada penampilan luarannya atau kilauannya.
[TOC]
Struktur pepejal kristal
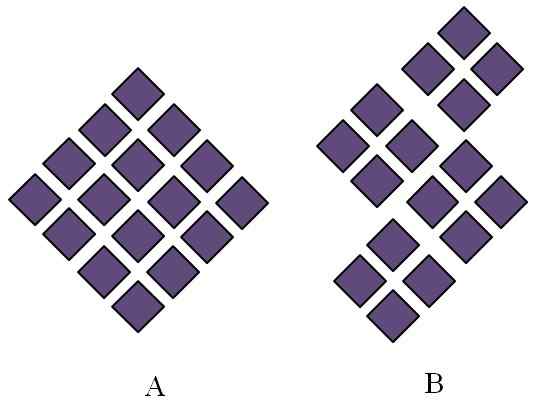 Struktur pepejal kristal yang diperintahkan. Sumber: Gabriel Bolívar.
Struktur pepejal kristal yang diperintahkan. Sumber: Gabriel Bolívar. Pepejal kristal telah mengarahkan struktur. Ciri -ciri geometriknya bergantung kepada jenis rangkaian kristal yang mana mereka berada, yang seterusnya diproyeksikan secara luaran dalam bentuk kristal (sistem kristal). Imej unggul menggambarkan dua konsep penting struktur tersebut: berkala dan bijirin kristal.
Boleh melayani anda: penyebaran fasaSistem spatial zarah pepejal kristal adalah akhbar; iaitu, ia diulang lagi dan lagi ke semua arah. Ini menyebabkan corak strukturnya sendiri untuk setiap rangkaian pepejal dan kristal; Sebagai contoh, ini adalah di mana garam dan gula mula membezakan di luar sifat kimianya.
Di dalam rombus mereka diperintahkan untuk menimbulkan rhombus yang lebih besar. Setiap rhombus ungu mewakili zarah atau satu set mereka (atom, ion atau molekul). Oleh itu, dapat dijangkakan bahawa kristal makroskopik A mempunyai penampilan rhomboédica.
Sementara itu, dalam b rombus diperintahkan sedemikian rupa sehingga mereka berasal dari bijirin kristal; Ini, kristal yang sangat kecil (kristal). Ia kemudian dikatakan bahawa B adalah pepejal polyristal; iaitu, ia dibentuk oleh pelbagai kristal aglomerasi.
Kesimpulannya, pepejal boleh menjadi kristal (a), atau polyristaline (b); Dalam bentuk kristal, sementara polyristales b.
Sifat
Sifat pepejal kristal bergantung pada jenis gelasnya. Adalah diketahui bahawa struktur mereka diperintahkan, dan mereka juga biasanya mempersembahkan puak -puak cemerlang yang jatuh cinta dengan pencinta mineral. Walau bagaimanapun, sebutan dibuat bahawa berdebu pepejal, termasuk "off", juga boleh diklasifikasikan sebagai kristal.
Cara di mana zarah mereka berorientasikan spasial membolehkan mereka mempunyai beberapa sifat penting untuk pencirian mereka. Sebagai contoh, pepejal kristal mampu mengubah x -rays, mewujudkan spektrum difraksi dari mana struktur mikroskopik kristal dapat ditentukan.
Begitu juga, kerana strukturnya berkala, haba disebarkan dengan cara yang sama sepanjang pepejal; selagi tidak ada kekotoran di antara. Oleh itu, titik lebur untuk pepejal kristal adalah malar, dan tidak berubah tanpa mengira bagaimana ia diukur.
Ia boleh melayani anda: Gallium: sifat, struktur, mendapatkan, menggunakanJenis pepejal kristal
Jenis pepejal kristal berdasarkan jenis zarah yang mengarangnya dan apakah interaksi atau pautan mereka. Terdapat empat jenis: rangkaian ionik, logam, molekul dan kovalen.
Walaupun mereka menunjukkan tahap kekotoran tertentu, mereka terus menjadi kristal, walaupun sifatnya terjejas dan tidak menunjukkan nilai yang sama untuk pepejal murni.
Ionik
Garam adalah contoh pepejal kristal ionik, kerana ia terdiri daripada ion na+ dan Cl-. Oleh itu, dalam jenis pepejal ini, ikatan ionik mengawal: ia adalah kuasa elektrostatik yang mengawal urutan struktur.
Logam
Semua atom logam membentuk kristal logam. Ini bermaksud bahawa, sebagai contoh, garpu perak adalah konglomerat kristal perak yang bersatu. Struktur dalaman atau mikroskopik adalah sama di setiap telapak objek, dan tetap tidak berubah dari pemegang garpu ke ujung giginya.
Molekul
Gula adalah contoh pepejal kristal molekul, kerana ia terbentuk daripada molekul sukrosa. Oleh itu, jenis pepejal ini terdiri daripada molekul, yang melalui interaksi intermolecularnya (dan ikatan bukan kovalen) berjaya menubuhkan struktur yang teratur.
Rangkaian kovalen
Akhirnya, kami mempunyai pepejal kristal rangkaian kovalen. Mereka mendominasi ikatan kovalen, kerana mereka bertanggungjawab untuk menubuhkan perintah dan mengekalkan atom -atom yang sangat ditetapkan dalam kedudukan ruang masing -masing. Tidak ada perbincangan mengenai ion, atom atau molekul, tetapi rangkaian tiga dimensi.
Contoh
Seterusnya, dan akhirnya, beberapa contoh akan disebutkan untuk setiap jenis pepejal kristal.
Boleh melayani anda: ElektronegativitiIonik
Semua garam adalah pepejal ionik. Terdapat juga sulfida, hidroksida, oksida, halida, dan sebatian lain yang juga dibentuk oleh ion, atau interaksi mereka dalam intipati ionik. Kami ada:
-KCl
-Kes4
-BA (oh)2
-Cuso4
-FECL3
-Na2S
-Mgo
-Caf2
-Nahco3
-(NH4)2Cro4
Sebagai tambahan kepada contoh -contoh ini, sebahagian besar mineral dianggap pepejal kristal ionik.
Logam
Sebarang elemen logam secara semulajadi dibentangkan sebagai kristal logam. Sebahagian daripada mereka adalah:
-Tembaga
-Besi
-Aluminium
-Chrome
-Hidrogen logam (di bawah tekanan yang tidak dapat dibayangkan)
-Tungsten
-Zirkonium
-Titanium
-Magnesium
-Natrium
Molekul
Terdapat pelbagai pepejal kristal molekul. Hampir mana -mana sebatian organik yang menguatkan berjaya menubuhkan kristal jika kesuciannya tinggi, atau jika strukturnya tidak terlalu rumit. Jadi kita ada:
-Ais (h2Sama ada)
-Ais kering (CO2)
-Yo2
-P4
-S8 (dan polimorfnya)
-Anthracene
-Oksigen pepejal
-Ammonia pepejal
-Phenolphthalein
-Asid benzoik
Rangkaian kovalen
Dan akhirnya, di antara beberapa pepejal kristal rangkaian kovalen yang kita ada:
-Berlian
-Grafit
-Nanotube karbon
-Fullerenos
-Kuarza
-Silikon
-Germanium
-Boron Nitride
Dari senarai ini, nanotube karbon dan fullerene juga boleh dianggap sebagai pepejal kristal molekul. Ini kerana, walaupun mereka terdiri daripada atom karbon bersatu kovalen, mereka menentukan unit yang boleh digambarkan sebagai makromolekul (bola bola sepak dan tiub).
Rujukan
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2020). Kristal. Diperoleh dari: dalam.Wikipedia.org
- Kimia Librettexts. (16 Jun, 2019). Pepejal kristal dan amorf. Pulih dari: chem.Libretxts.org
- Rachel Bernstein & Anthony Carpi. (2020). Sifat pepejal. Pulih dari: penglihatan.com

