Komposisi, Jenis dan Contoh Penyelesaian Crystalloid
- 865
- 230
- Ismael Turner
The Penyelesaian Crystalloid Mereka adalah yang dibentuk oleh pembubaran molekul larut air kecil dan lain. Dalam istilah kimia yang mudah: penyelesaian ini tidak lebih daripada penyelesaian perlombongan berair dan dicairkan.
Penyelesaian Crystalloid memainkan peranan penting dalam terapi klinikal seperti cecair infus intravena untuk kes -kes pendarahan, dehidrasi, hipovolemia dan jangkitan. Biasanya, kepekatan garamnya adalah isotonik, yang bermaksud bahawa bilangan ion yang dibubarkannya adalah setanding dengan plasma darah.
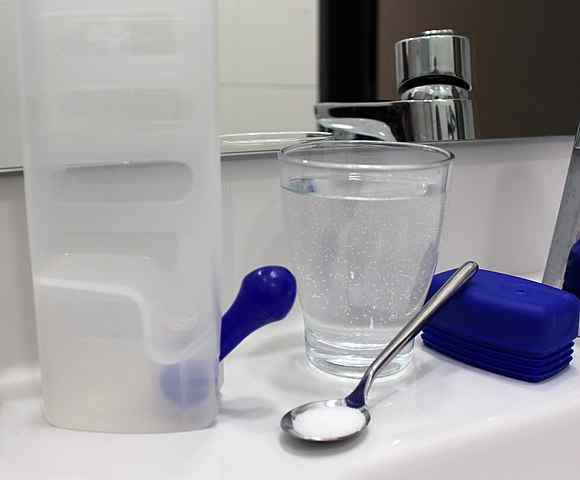
 Penyelesaian kristal boleh disediakan hanya dengan membubarkan garam dan larutan lain di dalam air pada kepekatan sederhana. Sumber: Rillke/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/3.0)
Penyelesaian kristal boleh disediakan hanya dengan membubarkan garam dan larutan lain di dalam air pada kepekatan sederhana. Sumber: Rillke/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/3.0) Oleh itu, penyelesaian crystalloid tidak menyebabkan perubahan osmotik, tetapi memberikan jumlah cecair yang betul supaya darah terus mengairi oleh sistem peredaran darah. Dengan cara ini, dicapai bahawa jantung mengepam darah yang dicairkan dan boleh membekalkan oksigen ke tisu.
Contoh penyelesaian kristal adalah penyelesaian garam biasa, yang mengandungi NaCl pada kepekatan 0.9%. Walau bagaimanapun, bergantung kepada kes klinikal, penyelesaian lain boleh dipilih, dengan komponen, kepekatan dan jenis tonik yang berbeza.
[TOC]
Komposisi penyelesaian kristal
Semua penyelesaian crystalloid didasarkan pada disterilkan atau mikroorganisma percuma, jadi ini adalah pelarut kegemarannya. Jika tidak, mereka tidak dapat mengintegrasikan sihat ke dalam badan kita dan menyebabkan reaksi yang tidak diingini. Sebagai penyelesaian atau penyelesaiannya, ia juga mempunyai larutan, yang pada dasarnya adalah garam mineral atau elektrolit yang kuat.
Jualan boleh beberapa, selagi mereka menyumbang dalam kepekatan sederhana ion na+, Ac2+, K+ dan Cl-. Sebagai tambahan kepada garam bukan organik, mereka juga boleh mempunyai larutan organik yang sangat larut dalam air seperti asetat, glukonat dan laktat. Juga, beberapa penyelesaian ini mengandungi glukosa (dextrose).
Boleh melayani anda: hydroxyapatiteKepekatan garam atau larutan ini sangat bervariasi, dan dinyatakan sama ada dalam peratusan, miligram oleh desiliter (mg/dl), molariti atau osmolarities. Pilihan satu atau yang lain bergantung kepada kriteria klinikal.
Lelaki
Dikatakan pada mulanya penyelesaian kristal sering digunakan untuk memberikan jumlah cecair ke sistem peredaran darah. Dalam proses itu, bergantung kepada toniknya, plasma darah menderita atau perubahan bukan -osmotik, yang mempromosikan atau memihak kepada negara -negara tertentu yang dikehendaki dalam pesakit.
Oleh itu, satu -satunya perkara yang membezakan penyelesaian kristal dari yang lain bukanlah sifat kimia larutnya, tetapi toniknya; iaitu, jika penyelesaian hipertonik, isotonik atau hipotonik.
Hypertonic
Penyelesaian kristal hipertonik ialah kepekatan garam yang lebih tinggi daripada yang terdapat dalam plasma darah. Oleh itu, air berhijrah dari dalam sel ke plasma yang telah meningkatkan toniknya kerana kehadiran larutan kristal hipertonik. Contoh penyelesaian jenis ini ialah 3% NaCl, terutamanya lebih tertumpu daripada penyelesaian salin 0.9% normal.
Penyelesaian ini dikontraindikasikan untuk kebanyakan kes klinikal, kecuali bagi mereka yang membentangkan sekuel neurologi.
Isotonik
Penyelesaian kristal isotonik ialah kepekatan garamnya adalah setanding atau sama dengan plasma darah dan bahagian selular. Oleh itu, tidak ada pertukaran air antara kedua -dua media. Contoh penyelesaian jenis ini ialah 0.9%NaCl, yang telah disebutkan di atas.
Hypotonic
Dan akhirnya, penyelesaian kristal hipotonik ialah kepekatan garam yang lebih rendah daripada plasma darah dan ruang atau ruang intraselular. Kali ini air bergerak ke dalam sel sel sehingga mencapai keseimbangan. Contoh penyelesaian jenis ini ialah 0.45% NaCl.
Ia boleh melayani anda: logam alkaliSeperti penyelesaian kristal hipertonik, hipotonik dikontraindikasikan untuk kebanyakan kes klinikal, terutama bagi mereka di mana terdapat risiko edema cerebral.
Contoh penyelesaian kristal
Beberapa contoh penyelesaian kristal akan disebutkan dan diterangkan di bawah. Perbezaan antara satu dan yang lain akan terletak pada identiti elektrolitnya atau garam terlarut.
Penyelesaian Saline Normal
Penyelesaian salin biasa mempunyai komposisi NaCl 0.9%, adalah isotonik dan juga penyelesaian kristal yang paling berulang, kerana ia berfungsi untuk merawat infiniti kes dehidrasi biasa; seperti yang disebabkan oleh cirit -birit, kejutan, muntah, pendarahan, antara lain. Walau bagaimanapun, gunakan pada pesakit dengan masalah buah pinggang atau jantung dielakkan.
Penyelesaian laktat
Juga dikenali sebagai penyelesaian Ringer atau Hartmann (walaupun mereka berbeza sedikit dalam kepekatan ionik mereka), ia adalah satu yang terdiri daripada campuran natrium klorida, natrium laktat, kalsium klorida dan kalium klorida.
Komposisi garamnya adalah yang menyerupai plasma darah, jadi jenis isotonik. Ia digunakan sebagai cecair atau cecair adjuster untuk kes -kes luka bakar, trauma, ketidakseimbangan elektrolitik, asidosis metabolik. Walau bagaimanapun, ia adalah kontraindikasi untuk pesakit yang mengalami hiperkalkemia.
Laktat dimetabolisme di dalam badan kita dan akhirnya berubah menjadi bikarbonat. Penyelesaian ini juga boleh mengandungi anion glukonat, serta jumlah magnesium tertentu, mg2+.
Penyelesaian glukosa
Juga dikenali sebagai penyelesaian dextrose crystalloid, ia datang dalam dua kepekatan: 5 dan 10% (D5 atau D10, masing -masing). Ini pada mulanya hipotonik, tetapi ia berubah menjadi isotonik apabila glukosa diserap, memberikan air ke buah pinggang. Walaupun ia memberikan sejumlah besar kalori, ia adalah kontraindikasi untuk pesakit yang menderita hiperglikemia.
Boleh melayani anda: asid elagik: struktur, sifat, mendapatkan, lokasi, kegunaanTidak seperti penyelesaian kristal lain, ini manis. Yang paling manis mempunyai kepekatan lebih besar daripada 10% (D20, D30, D50, dll.), Dan mereka ditakdirkan untuk pesakit dengan edema pulmonari dan otak. Sebaliknya, mereka mengurangkan katabolisme protein, melindungi hati, dan membantu melawan runtuh peredaran darah.
Penyelesaian salin hipertonik dan hipotonik
Penyelesaian salin hipertonik (3 dan 5% NaCl) digunakan untuk membekalkan cecair untuk membakar pesakit, mendorong hiperosmolariti, dan melegakan kekurangan buah pinggang. Sebaliknya, penyelesaian salin hipotonik (0.45% NaCl atau kepekatan yang lebih rendah), mengawal hipernatremia, dan dikontraindikasikan untuk membakar pesakit.
Oleh itu, seseorang membekalkan kesan yang bertentangan dengan yang lain; Apabila penyelesaian hipertonik sangat diperlukan, hipotonik tidak disetujui, dan sebaliknya.
Mekanisme di sebalik semua penyelesaian kristal adalah berdasarkan keseimbangan osmotik dan air antara cecair intra dan ekstraselular.
Rujukan
- Lewis Sr et al. (3 Ogos 2018). Koloid atau kristal untuk penggantian cecair pada orang kritikal. Kerjasama Cochrane. Pulih dari: Cochrane.org
- Epstein em, Waseem m. (29 November 2019). Cecair crystalloid. Dalam: Statpearls. Treasure Island (FL): Statpearls Publishing 2020 -. Pulih dari: NCBI.NLM.NIH.Gov
- Wikipedia. (2020). Ekspander Volume. Diperoleh dari: dalam.Wikipedia.org
- Elsevier b.V. (2020). Crystalloid. Scientedirect. Diperoleh dari: Scientedirect.com
- Sheila Bouie. (2020). Crystalloids: Definisi & Contoh. Kajian. Pulih dari: belajar.com

