Volatilisasi

- 2968
- 684
- Clarence Greenholt DDS
 Apabila air dipanaskan di pinggan sehingga wap berlaku, volatilisasi berlaku. Dengan lesen
Apabila air dipanaskan di pinggan sehingga wap berlaku, volatilisasi berlaku. Dengan lesen Apa itu volatilisasi?
The volatilisasi Ia adalah proses menukar bahan kimia keadaan cecair atau pepejal ke gas atau stim. Istilah lain yang digunakan untuk menggambarkan proses yang sama adalah pengewapan, penyulingan dan sublimasi.
Bahan sering boleh dipisahkan dari yang lain dengan volatilisasi, dan boleh dipulihkan oleh pemeluwapan stim.
Bahan ini boleh dikurangkan dengan lebih cepat, sama ada memanaskannya untuk meningkatkan tekanan stim atau dengan mengukus, menggunakan aliran gas lengai atau pam vakum.
Prosedur pemanasan termasuk volatilisasi air, merkuri atau trichloride arsenik untuk memisahkan bahan -bahan ini dari unsur -unsur interferensi.
Kadang -kadang tindak balas kimia digunakan untuk menghasilkan produk yang tidak menentu, seperti dalam pembebasan karbon dioksida dari karbonat, ammonia dalam kaedah kjeldahl untuk penentuan nitrogen dan sulfur dioksida dalam penentuan keluli sulfur.
Kaedah volatilisasi biasanya dicirikan oleh kesederhanaan dan kemudahan operasi yang hebat, kecuali apabila tahan terhadap tahan kakisan atau bahan diperlukan.
Volatilisasi tekanan wap
Mengetahui bahawa suhu mendidih air berada pada suhu 100 ° C, adalah penting untuk bertanya mengapa air hujan menguap. Sekiranya berada di 100 ° C, ia harus memberi kita haba.
Ia juga bernilai bertanya apa aroma ciri yang diberikan kepada alkohol, cuka, kayu atau plastik.
Orang yang bertanggungjawab untuk semua ini adalah harta yang dikenali sebagai tekanan stim, yang merupakan tekanan yang dikenakan oleh stim dalam keseimbangan dengan fasa pepejal atau cecair dari bahan yang sama. Juga, tekanan separa bahan di atmosfera pada pepejal atau cecair.
Tekanan stim adalah ukuran kecenderungan bahan yang akan ditukar kepada keadaan gas atau stim, iaitu ukuran volatiliti bahan.
Ia boleh melayani anda: karbon disulfida (cs2): struktur, sifat, kegunaan, risikoApabila tekanan stim meningkat, semakin besar kapasiti cecair atau pepejal untuk menguap, sehingga menjadi lebih tidak menentu.
Tekanan stim akan meningkat dengan suhu. Suhu di mana tekanan stim pada permukaan cecair adalah sama dengan tekanan yang dikenakan oleh persekitaran dipanggil titik mendidih cecair.
Tekanan stim bergantung kepada larutan larut dalam larutan (ia adalah harta koligatif). Di permukaan penyelesaian (antara muka rendah udara), molekul yang paling cetek cenderung menguap, bertukar antara fasa dan menghasilkan tekanan stim.
Kehadiran larut mengurangkan bilangan molekul pelarut di antara muka, mengurangkan tekanan stim.
Perubahan dalam tekanan stim boleh dikira dengan undang -undang Raault untuk larutan yang tidak menonjol, yang diberikan oleh:
(1) Di mana P1 adalah tekanan stim selepas menambahkan larutan, x1 adalah pecahan molar yang disebutkan larut dan p ° adalah tekanan wap pelarut tulen.
Di mana P1 adalah tekanan stim selepas menambahkan larutan, x1 adalah pecahan molar yang disebutkan larut dan p ° adalah tekanan wap pelarut tulen.
Jika jumlah pecahan molar larut dan pelarut adalah sama dengan 1 maka kita ada:
(2)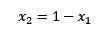
Di mana x2 adalah pecahan molar pelarut. Sekiranya kita melipatgandakan kedua -dua belah persamaan dengan P ° maka ia tetap:
(3)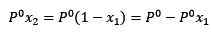
Menggantikan (1) dalam (3) kekal:
(4)
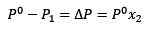
Ini adalah variasi tekanan stim apabila larut larut.
Analisis gravimetrik
Analisis gravimetrik adalah kelas teknik makmal yang digunakan untuk menentukan jisim atau kepekatan bahan dengan mengukur perubahan jisim.
Ahli kimia yang kita cuba kuantiti kadang -kadang dipanggil analit. Kita boleh menggunakan analisis gravimetrik untuk menjawab soalan seperti:
Boleh melayani anda: mineral logam- Apakah kepekatan analit dalam penyelesaian?
- Betapa murni sampel kami? Sampel di sini boleh menjadi pepejal atau penyelesaian.
Terdapat dua jenis analisis gravimetrik yang biasa. Kedua -duanya melibatkan perubahan fasa analit untuk memisahkannya dari seluruh campuran, menimbulkan perubahan dalam adunan.
Salah satu daripada kaedah ini adalah gravimetri hujan, tetapi yang benar -benar menarik minat kami ialah gravimetri volatilisasi.
Volatilisasi gravimetri didasarkan pada termal atau kimia sampel dan mengukur perubahan yang terhasil dalam jisimnya.
Sebagai alternatif, kita dapat menangkap dan menimbang produk penguraian yang tidak menentu. Kerana pembebasan spesies yang tidak menentu adalah bahagian penting dari kaedah ini, kami secara kolektif mengklasifikasikannya sebagai kaedah analisis volatilisasi gravimetrik.
Masalah analisis gravimetrik hanyalah masalah stoikiometri dengan beberapa langkah tambahan.
Untuk melakukan pengiraan stoikiometrik, kita memerlukan pekali persamaan kimia yang seimbang.
Sebagai contoh, jika sampel mengandungi kekotoran barium dihidrasi (BACL2● H₂o), anda boleh mendapatkan jumlah kekotoran yang memanaskan sampel untuk menguap air.
Perbezaan jisim antara sampel asal dan sampel yang dipanaskan akan memberi kita, dalam gram, jumlah air yang terkandung dalam barium klorida.
Dengan pengiraan stoikiometrik yang mudah, jumlah kekotoran sampel akan diperolehi.
Penyulingan berperingkat
Penyulingan pecahan adalah proses di mana komponen campuran cecair dipisahkan ke bahagian yang berlainan (dipanggil pecahan) mengikut titik mendidih yang berbeza.
Perbezaan turun naik sebatian campuran memainkan peranan penting dalam pemisahannya.
Boleh melayani anda: peraturan oktetPenyulingan pecahan digunakan untuk membersihkan bahan kimia dan juga untuk memisahkan campuran dan mendapatkan komponen mereka. Ia digunakan sebagai teknik makmal dan dalam industri, di mana prosesnya mempunyai kepentingan komersial yang hebat.
Wap penyelesaian mendidih diluluskan di sepanjang lajur yang tinggi, yang dipanggil lajur subdivision.
Lajur ini dibungkus dengan mutiara plastik atau kaca untuk meningkatkan pemisahan, memberikan lebih banyak kawasan permukaan untuk pemeluwapan dan penyejatan.
Suhu lajur secara beransur -ansur berkurangan sepanjang panjangnya. Komponen dengan titik mendidih yang lebih tinggi dipendekkan dalam lajur dan kembali ke penyelesaian.
Komponen titik mendidih yang lebih rendah (lebih tidak menentu) melewati lajur dan dikumpulkan berhampiran bahagian atas.
Secara teorinya, mempunyai lebih banyak mutiara atau plat meningkatkan pemisahan, tetapi penambahan plat juga meningkatkan masa dan tenaga yang diperlukan untuk menyelesaikan penyulingan.
Contoh volatilisasi
- Blok ais kering bersentuhan dengan pecah udara. Udara memulakan proses volatilisasi dan ais menguap: ia berlalu dari keadaan pepejal ke soda.
- Apabila air atau bahan lain direbus: haba menjana stim, dan dengan itu air berlalu dari keadaan cecair ke gas.
- Pil naphthalin, yang secara beransur -ansur merendahkan dan lulus dari keadaan pepejal ke soda.
- Apabila sulfur pepejal tertakluk kepada suhu tinggi, ia menjadi gas toksik. Iaitu, ia bergerak dari pepejal ke gas.
- Pil Aromatizing: Mereka mempunyai proses yang sama seperti pil naphthalin, secara beransur -ansur merendahkan dan menjadi gas, berbau dan tidak berbahaya.
Rujukan
- Steam definisi tekanan. Pulih dari pemikiran.com.
- Tekanan wap. Pulih dari Britannica.com.

