Struktur, sifat, pengeluaran, penggunaan acrilonitrile

- 878
- 6
- Erick Krajcik
Dia Acrilonitrile Ia adalah sebatian organik yang formula pekatnya adalah cho2CHCN. Ia adalah salah satu nitril paling mudah yang wujud. Kimia dan strukturnya tidak lebih daripada produk kesatuan antara kumpulan vinil, CHO2= Ch-, dan kumpulan nitril, sianida, C≡N. Ia adalah bahan yang mempunyai kesan perindustrian yang hebat terhadap dunia plastik.
Secara fizikal, ia adalah cecair yang tidak berwarna, dengan bau bawang tertentu, dan dalam keadaan tidak suci memberikan nada kekuningan. Ia sangat mudah terbakar, toksik, dan mungkin karsinogenik, jadi ia diklasifikasikan sebagai bahan yang sangat berbahaya. Ironinya, dengan itu mereka dihasilkan plastik dan mainan kehidupan seharian, seperti tupperware dan blok LEGO.
 Polimer Acrilonitril terdapat di plastik Tupperware. Sumber: Stebulus melalui Wikipedia.
Polimer Acrilonitril terdapat di plastik Tupperware. Sumber: Stebulus melalui Wikipedia. Di Skala Perindustrian, Acrilonitril. Hampir semua jumlah yang dihasilkan bertujuan untuk pembuatan plastik, berdasarkan homopolimer, seperti polyacrylonitrile, atau kopolimer, seperti acrilonitrile-butadiene-styrene.
[TOC]
Struktur Acrilonitrile
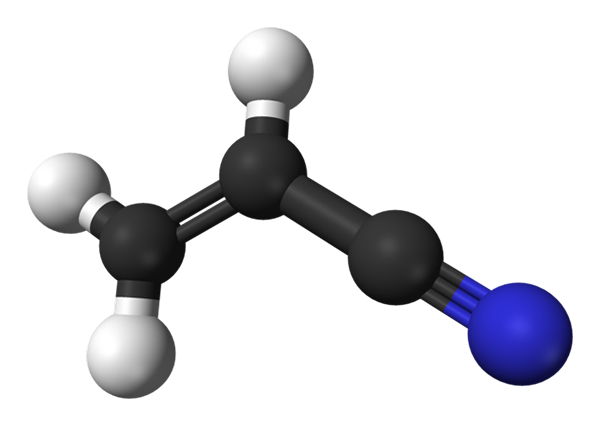 Struktur molekul acrilonitrile. Sumber: Benjah-bmm27 / domain awam
Struktur molekul acrilonitrile. Sumber: Benjah-bmm27 / domain awam Di bahagian atas, kita mempunyai molekul Acrilonitrile yang diwakili dengan model sfera dan bar. Sfera hitam sesuai dengan atom karbon, manakala putih dan biru ke atom hidrogen dan nitrogen. Kiri, CH2= CH- sepadan dengan kumpulan vinil, dan hak, kepada kumpulan cyano, C≡N.
Keseluruhan molekul adalah rata, kerana karbon kumpulan vinil mempunyai hibridisasi SP2. Sementara itu, karbon kumpulan ciano mempunyai hibridisasi SP, bersebelahan dengan atom nitrogen dalam garis yang terletak pada satah yang sama dengan seluruh molekul.
Kumpulan CN menyumbang polariti kepada molekul, jadi molekul CHO2CHCN menetapkan dipole kekal di mana ketumpatan elektronik tertinggi diarahkan ke atom nitrogen. Oleh itu, dipole-dipol.
Boleh melayani anda: Apakah periodik kimia?Molekul Ch2CHCN rata, dapat mengharapkan bahawa dalam kristal mereka (dipenuhi pada -84 ºC) mereka boleh didapati di antara satu sama lain seperti lembaran atau lembaran kertas, sehingga dipoles mereka tidak menolak.
Sifat
Penampilan fizikal
Cecair tanpa warna tetapi dengan nada kekuningan apabila ia membentangkan beberapa kekotoran. Apabila demikian, mereka mengesyorkan penyulingannya sebelum penggunaannya. Ia tidak menentu dan juga mempunyai bau yang sengit yang serupa dengan bawang.
Jisim molar
53,064 g/mol
Takat lebur
-84 ºC
Takat didih
77 ºC
Titik kilat
-5 ºC (cawan tertutup)
0 ºC (cawan terbuka)
Suhu sendiri
481 ºC
Ketumpatan
0.81 g/cm3
Ketumpatan wap
1.83 dalam hubungan udara.
Tekanan wap
109 mmHg pada 25 ºC
Kelarutan
Di dalam air ia mempunyai kelarutan 74 g/l hingga 25 ºC. Acrilonitril juga larut dalam aseton, minyak, etanol, etil asetat dan etanil benzena.
Penguraian
Apabila termal melepaskan sianida hidrogen toksik, oksida karbon dan oksida nitrogen.
Pengeluaran
Proses Sohio
Acryonitrile boleh berlaku kepada skala besar melalui pelbagai reaksi dan proses kimia. Daripada mereka semua, proses Sohio adalah yang paling banyak digunakan, yang terdiri daripada amixidation pemangkin propylene. Dalam reaktor katil fluidized, propylene dicampur dengan udara dan ammonia pada suhu sekitar 400 dan 510 ºC, di mana mereka bertindak balas terhadap pemangkin pepejal.
Reaktan memasuki reaktor sekali, mengambil reaksi berikut:
2ch3-CH = CH2 + 2 nh3 + 3 o2 → 2 ch2= CH-C≡N + 6 jam2Sama ada
Perhatikan bahawa oksigen dikurangkan menjadi air, sementara propilena mengoksidakan acrilonitrile. Oleh itu nama 'amoxidation', kerana ia adalah pengoksidaan yang melibatkan penyertaan ammonia.
Boleh melayani anda: mendidih: konsep, jenis dan contohProses alternatif
Sebagai tambahan kepada proses SOHIO, tindak balas lain dapat disebutkan yang membolehkan memperoleh acrilonitrile. Jelas sekali, tidak semuanya berskala, atau sekurang -kurangnya dengan cara yang mencukupi, atau menjana produk dengan prestasi tinggi atau kesucian.
Acrylonitrile disintesis, sekali lagi dari propylene, tetapi menjadikannya bertindak balas dengan oksida nitrik pada pemangkin PBO2-Zro2 Airgel -shaped. Reaksi adalah seperti berikut:
4 ch3-CH = CH2 + 6 Tidak → 4 Cho2= CH-C≡N + 6 jam2Atau + n2
Reaksi yang tidak melibatkan propilena adalah yang bermula dengan etilena oksida, yang bertindak balas dengan sianida hidrogen untuk berubah menjadi etilena cyanohydrin; Dan kemudian, ia menjadi dehidrasi pada suhu 200 ºC dalam acrilonitrile:
Eto + HCN → CH2Oh2CN
Ch2Oh2CN + Q (200 ºC) → CH2= CH-C≡N +H2Sama ada
Satu lagi tindak balas langsung adalah penambahan sianida hidrogen pada asetilena:
HC≡CH + HCN → CH2= CH-C≡N
Walau bagaimanapun, banyak produk menengah dibentuk, jadi kualiti acrilonitrile lebih rendah berbanding proses Sohio.
Sebagai tambahan kepada bahan yang disebutkan di atas, lactonitrile, propionitril.
Aplikasi
 Legos terutamanya dihasilkan dengan plastik abs, kopolimer di mana acrilonitrile adalah sebahagian. Sumber: Pxhere.
Legos terutamanya dihasilkan dengan plastik abs, kopolimer di mana acrilonitrile adalah sebahagian. Sumber: Pxhere. Acrilonitrile adalah bahan yang sangat diperlukan untuk industri plastik. Beberapa plastik yang diperolehnya sangat terkenal. Demikianlah kes kopolimer acrilonitrilo-butadiene-styrene (ABS), yang mana kepingan orang awam dihasilkan. Kami juga mempunyai serat akrilik, dihuraikan dengan homopolimer polyacrylonitril (PAN).
Boleh melayani anda: saponifikasiAntara plastik lain yang mengandungi acrilonitrile sebagai monomer, atau yang bergantung kepadanya untuk pembuatannya, kita mempunyai: acrylene stretch (san), butadiene acrylonitrile (NBR), acrilonitrile stretch acrylate (ASA), polyacrylamide, dan sintetik retin dan nitrile resin dan nitril.
Secara praktiknya, polimer semulajadi, seperti kapas, boleh diubah suai dengan memasukkan struktur molekulnya ke acrilonitrile. Oleh itu, derivatif nitril diperolehi, yang menjadikan kimia acrylonitril yang sangat luas.
Salah satu kegunaannya di luar dunia plastik adalah seperti racun perosak bercampur dengan karbon tetraklorida. Walau bagaimanapun, disebabkan kesannya yang mengerikan terhadap ekosistem laut, racun perosak tersebut telah melarang diri mereka atau tertakluk kepada sekatan yang kuat.
Risiko
Acrilonitrile adalah bahan berbahaya, jadi ia mesti dimanipulasi dengan penjagaan yang melampau. Sebarang pendedahan yang tidak sesuai atau berlebihan berpanjangan ke sebatian ini boleh mematikan, sama ada dengan penyedutan, pengambilan atau hubungan fizikal.
Ia harus dikekalkan sejauh mungkin dari sumber haba, kerana ia adalah cecair yang tidak menentu dan sangat mudah terbakar. Dia juga tidak harus bersentuhan dengan air, kerana dia bertindak balas dengan ganas dengannya.
Di samping itu, ia adalah bahan karsinogenik yang mungkin, yang telah dikaitkan dengan kanser hati dan paru -paru. Mereka yang telah terdedah kepada bahan ini telah meningkat dalam tahap tiosianat yang dikeluarkan dalam air kencing, dan sianida darah.
Rujukan
- Morrison, r. T. dan Boyd, R, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2020). Acrylonitrile. Diperoleh dari: dalam.Wikipedia.org
- Pusat Kebangsaan Maklumat Bioteknologi. (2020). Acrylonitrile. Pangkalan data PUBCHEM., CID = 7855. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Elsevier b.V. (2020). Acrylonitrile. Scientedirect. Diperoleh dari: Scientedirect.com
- Korry Barnes. (2020). Apa itu acrylonitrile? - Penggunaan & Properties. Kajian. Pulih dari: belajar.com
- Pajonk, g.M., Manzalji, t. (1993). Sintesis acrylonitril dari campuran propilena dan nitrik oksida pada PBO2-Zro2 Pemangkin Airgel. Catal Lett dua puluh satu, 361-369. doi.org/10.1007/BF00769488
- « Ciri -ciri pengaturcaraan dinamik, contoh, kelebihan, kelemahan
- Apakah proses isoterma? (Contoh, latihan) »

