Apakah proses isoterma? (Contoh, latihan)

- 4412
- 1300
- Anthony Breitenberg
Dia proses isoterma atau isotherm adalah proses termodinamik yang boleh diterbalikkan di mana suhu tetap tetap. Dalam gas, terdapat situasi di mana perubahan dalam sistem tidak menghasilkan variasi suhu, tetapi dalam ciri -ciri fizikal.
Perubahan ini adalah perubahan fasa, apabila bahan berubah dari pepejal ke cecair, cecair gas atau sebaliknya. Dalam kes sedemikian, molekul bahan menyesuaikan kedudukan mereka, menambah atau mengekstrak tenaga terma.
 Rajah 1. Carambans yang mencairkan adalah contoh proses isoterma. Sumber: Pixabay.
Rajah 1. Carambans yang mencairkan adalah contoh proses isoterma. Sumber: Pixabay. Tenaga terma yang diperlukan untuk perubahan fasa berlaku dalam bahan dipanggil haba laten atau haba transformasi.
Salah satu cara untuk mendapatkan proses isoterma adalah untuk menghubungi bahan yang akan menjadi sistem yang sedang dikaji dengan deposit terma luaran, yang merupakan satu lagi sistem kapasiti kalori besar. Dengan cara ini, pertukaran haba yang perlahan berlaku, bahawa suhu tetap berterusan.
Jenis proses ini sering diberikan. Sebagai contoh, pada manusia apabila suhu badan meningkat atau turun, kita berasa sakit, kerana dalam badan kita banyak tindak balas kimia yang mengekalkan kehidupan diberikan pada suhu tetap. Ini sah untuk darah panas secara umum.
Contoh lain ialah ais yang cair dengan haba ketika kiub musim bunga dan ais tiba.
[TOC]
Contoh proses isoterma
-Metabolisme haiwan panas yang panas dijalankan pada suhu malar.
 Rajah 2. Haiwan yang berwarna panas mempunyai mekanisme untuk menjaga suhu tetap. Sumber: Wikimedia Commons.
Rajah 2. Haiwan yang berwarna panas mempunyai mekanisme untuk menjaga suhu tetap. Sumber: Wikimedia Commons. -Apabila air mendidih perubahan fasa, cecair gas, dan suhu tetap malar pada kira -kira 100 º C, kerana faktor lain dapat mempengaruhi nilai.
-Es yang cair adalah satu lagi proses isoterma yang kerap, serta meletakkan air di dalam peti sejuk untuk membuat kiub ais.
Boleh melayani anda: optik geometri: apa kajian, undang -undang, aplikasi, latihan-Enjin kereta, peti sejuk, serta banyak jenis jentera, beroperasi dengan betul dalam julat suhu tertentu. Untuk mengekalkan suhu yang sesuai, peranti yang dipanggil Termostat. Dalam reka bentuknya, pelbagai prinsip operasi digunakan.
Kitaran Carnot
Enjin Carnot adalah mesin yang ideal dari mana kerja diperolehi terima kasih kepada proses yang boleh diterbalikkan sepenuhnya. Ia adalah mesin yang ideal kerana ia tidak menganggap proses yang menghilangkan tenaga, sebagai kelikatan bahan yang melakukan pekerjaan, atau geseran.
Siklus Carnot terdiri daripada empat peringkat, dua daripadanya adalah sejenis isoterma dan dua lagi adiabatik. Tahap isoterma adalah mampatan dan pengembangan gas yang bertanggungjawab untuk menghasilkan kerja yang berguna.
Enjin kereta beroperasi dengan prinsip yang serupa. Pergerakan omboh di dalam silinder dihantar ke bahagian lain kereta dan menghasilkan pergerakan. Ia tidak mempunyai tingkah laku sistem yang ideal seperti enjin Carnot, tetapi prinsip termodinamik adalah perkara biasa.
Pengiraan kerja yang dilakukan dalam proses isoterma
Untuk mengira kerja yang dilakukan oleh sistem apabila suhu tetap, undang -undang termodinamik pertama mesti digunakan, yang menyatakan:
Δu = q - w
Ini adalah satu lagi cara untuk menyatakan pemuliharaan tenaga dalam sistem, yang dibentangkan melalui ΔU atau perubahan tenaga, Q Apabila panas dibekalkan dan akhirnya W, yang mana kerja yang dilakukan oleh sistem tersebut.
Katakan sistem yang dimaksudkan adalah gas ideal yang terkandung dalam silinder dari omboh kawasan mudah alih Ke, Apa yang berfungsi ketika jumlahnya V perubahan V1 ke V2.
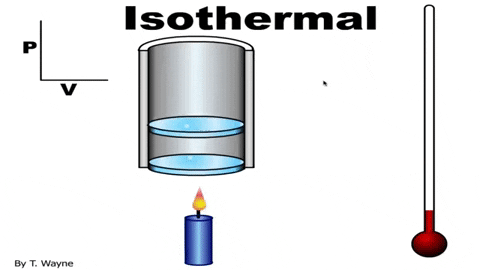 Rajah 3. Dalam proses isoterma, gas berkembang di omboh tanpa mengubah suhu. Sumber: YouTube.
Rajah 3. Dalam proses isoterma, gas berkembang di omboh tanpa mengubah suhu. Sumber: YouTube. Persamaan status gas ideal adalah Pv = nrt, yang berkaitan dengan jumlah tekanan P dan suhu T. Nilai n dan r adalah malar: n adalah bilangan tahi lalat gas dan r pemalar gas. Sekiranya berlaku proses isoterma produk Pv ia tetap.
Boleh melayani anda: pemalar antoin: formula, persamaan, contohNah, kerja yang dilakukan dikira dengan mengintegrasikan kerja pembezaan kecil, di mana kekuatan F menghasilkan anjakan dx kecil:
Dw = fdx = padx
Sebagai ADX tepatnya variasi kelantangan Dv, Jadi:
DW = PDV
Untuk mendapatkan jumlah kerja dalam proses isoterma, ungkapan DW disepadukan:
Tekanan P dan jumlahnya V Mereka adalah graf dalam rajah P-v Seperti yang ditunjukkan dalam angka dan kerja yang dilakukan bersamaan dengan kawasan di bawah lengkung:
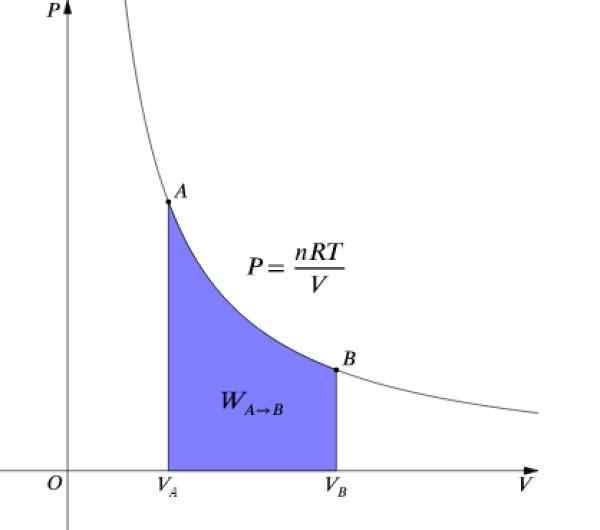 Rajah 4. Gambar rajah P-V proses isoterma. Sumber: Wikimedia Commons.
Rajah 4. Gambar rajah P-V proses isoterma. Sumber: Wikimedia Commons. Sebagai ΔU = 0 Oleh kerana suhu tetap malar, dalam proses isoterma ia harus:
Q = w
- Latihan 1
Silinder yang disediakan dengan omboh mudah alih mengandungi gas ideal pada 127 ºC. Jika omboh bergerak sehingga isipadu awal dikurangkan 10 kali, menjaga pemalar suhu, cari jumlah tahi lalat yang terkandung dalam silinder, jika kerja yang dilakukan pada gas adalah 38.180 J.
Fakta: R = 8.3 J/mol. K
Penyelesaian
Kenyataan itu menegaskan bahawa suhu tetap malar, maka kita berada di hadapan proses isoterma. Untuk kerja yang dilakukan pada gas, anda mempunyai persamaan yang ditolak sebelum ini:

127 º C = 127 + 273 k = 400 k
N Jelas, bilangan tahi lalat:
N = w / rt ln (v2 / v1) = -38180 J / 8.3 J/mol.K x 400 k x ln (v2/10v2) = 5 mol
Tanda negatif adalah sebelum bekerja. Pembaca yang prihatin akan perasan di bahagian sebelumnya bahawa W ditakrifkan sebagai "kerja yang dilakukan oleh sistem" dan mempunyai tanda +. Jadi "kerja yang dilakukan pada sistem" mempunyai tanda negatif.
Ia boleh melayani anda: Keadaan Keseimbangan Kedua: Penjelasan, Contoh, Latihan- Latihan 2
Anda mempunyai udara dalam silinder yang disediakan dengan pelocok. Pada mulanya terdapat 0.4 m3 tekanan pada suhu 100 kPa dan 80 º c. Udara dimampatkan pada 0.1 m3 Memastikan suhu di dalam silinder tetap berterusan semasa proses.
Tentukan berapa banyak kerja yang dilakukan semasa proses ini.
Penyelesaian
Kami menggunakan persamaan untuk kerja yang ditolak sebelumnya, tetapi bilangan tahi lalat tidak diketahui, yang boleh dikira dengan persamaan gas ideal:
80 º C = 80 + 273 k = 353 k.
P1V1 = n.R.T → n = p1V1 /RT = 100000 PA x 0.4 m3 /8.3 J/mol. K x 353 k = 13.65 mol
W = n.R.T ln (v2/V1) = 13.65 mol x 8.3 J/mol. K x 353 k x ln (0.1/0.4) = -55.442.26 J
Sekali lagi tanda negatif menunjukkan bahawa kerja dilakukan pada sistem, yang selalu berlaku ketika gas dimampatkan.
Rujukan
- Bauer, w. 2011. Fizik untuk Kejuruteraan dan Sains. Jilid 1. MC Graw Hill.
- Cengel, dan. 2012. Thermodynamics. 7ma Edisi. McGraw Hill.
- Figueroa, d. (2005). Siri: Fizik untuk Sains dan Kejuruteraan. Jilid 4. Cecair dan termodinamik. Diedit oleh Douglas Figueroa (USB).
- Knight, r. 2017. Fizik untuk saintis dan kejuruteraan: Pendekatan Strategi.
- Serway, r., Vulle, c. 2011. Asas Fizik. 9na Pembelajaran Cengage.
- Wikipedia. Proses isoterma. Diperoleh dari: dalam.Wikipedia.org.


