Alkynes
- 969
- 262
- Ms. Micheal Rippin
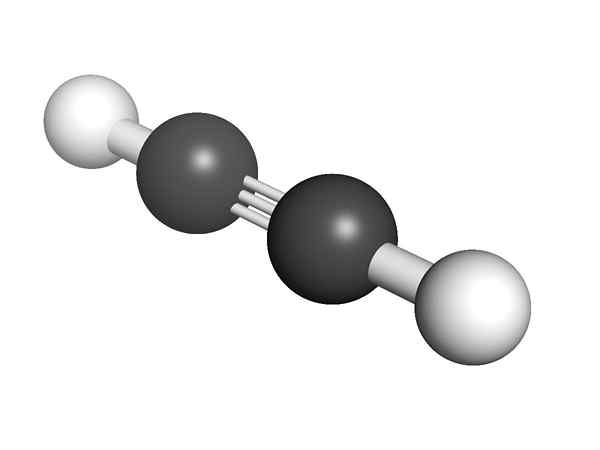
 Struktur Alvento, dengan pautan tiga
Struktur Alvento, dengan pautan tiga Apa itu Alkines?
The Alkynes Mereka adalah hidrokarbon atau sebatian organik yang terdapat dalam struktur mereka hubungan tiga antara dua karbon. Pautan triple (≡) ini dianggap sebagai kumpulan berfungsi apabila mewakili tapak aktif molekul, dan oleh itu bertanggungjawab untuk kereaktifan mereka.
Walaupun alkynes tidak banyak membezakan dari Alko atau Alkenes, mereka mempamerkan keasidan dan kutub yang lebih besar kerana sifat hubungan mereka. Istilah yang tepat untuk menggambarkan sedikit perbezaan ini adalah apa yang dikenali sebagai tidak tepu.
Alkanes adalah hidrokarbon tepu, sementara alkina adalah yang paling tidak tepu berkenaan dengan struktur asal. Apakah maksud ini? Bahawa alkane h3C-ch3 (etana) boleh menjadi dehidrogen ke h2C = ch2 (Etene) dan seterusnya HC≡CH (etino, atau lebih dikenali sebagai asetilena).
Perhatikan bagaimana pautan tambahan dibentuk di kalangan karbon mengurangkan bilangan hidrogen yang dikaitkan dengan mereka. Karbon, kerana ciri -ciri elektroniknya, bertujuan untuk membentuk empat pautan mudah, jadi semakin besar kecenderungan untuk bertindak balas (kecuali sebatian aromatik).
Sebaliknya, pautan triple jauh lebih kuat daripada ikatan dua (=) atau sederhana (-), tetapi pada kos tenaga yang tinggi. Oleh itu, kebanyakan hidrokarbon (alken dan alkena) boleh membentuk ikatan tiga pada suhu tinggi.
Akibat daripada tenaga yang tinggi, ketika melanggar mereka melepaskan sangat panas. Contoh fenomena ini dapat dilihat apabila acetylene terbakar dengan oksigen dan panas api api untuk mengimpal atau mencairkan logam digunakan.
Acetylene adalah alkyne yang paling mudah dan paling kecil dari semua. Hidrokarbon lain boleh dinyatakan dari formula kimia mereka dengan menggantikan H dengan kumpulan alquilical (RC≡CR '). Perkara yang sama berlaku di dunia sintesis organik melalui sebilangan besar reaksi.
Alkyne ini berlaku dari reaksi kalsium oksida batu kapur dan bahan mentah, bahan mentah yang menyediakan karbon yang diperlukan di dalam ketuhar elektrik:
Cao + 3c => cac2 + Co
CAC2 Ia adalah kalsium karbida, sebatian bukan organik yang akhirnya bertindak balas dengan air untuk membentuk asetilena:
CAC2 + 2h2O => ca (oh)2 + HC≡CH
Sifat fizikal dan kimia Alkin
Polariti
Pautan triple membezakan alkina dari alken dan alkenes. Tiga jenis hidrokarbon adalah apolar, tidak larut dalam air dan asid yang sangat lemah. Walau bagaimanapun, elektronegativiti karbon ikatan berganda dan tiga lebih besar daripada karbon mudah.
Menurut ini, karbon bersebelahan dengan hasil ikatan tiga ke kesan induktif ketumpatan beban negatif. Atas sebab ini, di manakah pautan c≡C atau c = c akan ada ketumpatan elektronik yang lebih besar daripada di seluruh kerangka berkarbonat. Akibatnya, terdapat momen dipol kecil di mana molekul berinteraksi dengan pasukan dipole-dipolo.
Interaksi ini sangat lemah jika momen dipole mereka dibandingkan dengan molekul air atau sebarang alkohol. Ini dicerminkan dalam sifat fizikal mereka: Alkin umumnya mempunyai titik gabungan dan mendidih yang lebih tinggi berbanding dengan hidrokarbon mereka yang kurang tepu.
Boleh melayani anda: 7 aplikasi biokimia yang paling pentingBegitu juga, disebabkan oleh polaritas yang rendah, mereka kurang larut dalam air, tetapi larut dalam pelarut organik apolar, seperti benzena.
Keasidan
Juga, elektronegativiti ini menyebabkan hidrogen HC≡CR lebih berasid daripada sesiapa yang hadir dalam hidrokarbon lain. Oleh itu, alkina adalah spesies yang lebih berasid daripada alkena dan lebih banyak daripada alkana. Walau bagaimanapun, keasidannya tetap hina jika dibandingkan dengan asid karboksilik.
Oleh kerana alkina adalah asid yang sangat lemah, mereka hanya bertindak balas dengan pangkalan yang sangat kuat, seperti natrium amiden:
HC≡CR + NANH2 => HC≡CNA + NH3
Dari tindak balas ini, larutan natrium asetilur diperoleh, bahan mentah untuk sintesis alkynes lain.
Reaktiviti Alquinos
Kereaktifan alkynes dijelaskan dengan penambahan molekul kecil ke pautan triple mereka, mengurangkan ketidakpastiannya. Ini boleh menjadi molekul hidrogen, hallogenida hidrogen, air atau halogen.
Hidrogenasi
Molekul kecil h2 Ia sangat sukar difahami dan cepat, jadi untuk meningkatkan peluang ditambah ke pautan tiga alkina.
Ini biasanya logam (Pd, Pt, Rh atau Ni) dibahagikan dengan baik untuk meningkatkan kawasan permukaan; Dan dengan cara ini, hubungan antara hidrogen dan alquino:
RC≡CR ' + 2H2 => Rch2Ch2R '
Hasilnya ialah hidrogen adalah "sauh" kepada karbon yang memecahkan ikatan, dan sebagainya sehingga alkane yang sepadan menghasilkan, RCH2Ch2R '. Ini bukan sahaja menembusi hidrokarbon awal, tetapi juga mengubah struktur molekulnya.
Penambahan halogenuros hidrogen
Di sini molekul bukan organik HX ditambah, di mana x boleh menjadi mana -mana halogen (f, cl, br atau i):
Rc≡Cr ' + hx => rch = cxr'
Penghidratan
Penghidratan alkina adalah apabila mereka menambah molekul air untuk membentuk aldehid atau keton:
Rc≡Cr ' + h2O => rch2Cor '
Jika R 'adalah H, ia adalah aldehid; Sekiranya ia sewa, maka itu adalah cetona. Dalam tindak balas sebatian yang dikenali sebagai enol (rch = c (oh) r ') dibentuk sebagai perantara.
Ini menderita penukaran bentuk enol (c-oh) ke keton (c = o) dalam keseimbangan yang disebut tautomerisasi.
Penambahan halogen
Dan berkenaan dengan penambahan, molekul diatomik halogen juga boleh berlabuh dengan karbon (x x2= F2, Cl2, Br2 saya dengar2):
Rc≡Cr ' + 2x2 => Rcx2-Cx2R '
Alkilasi acetylene
Dari larutan natrium asetilur, alkina lain boleh disediakan dengan menggunakan halida sewa:
HC≡CNA + rx => HC≡CR + NAX
Sebagai contoh, jika ia adalah metil iodida, maka alkyne yang dihasilkan akan menjadi:
HC≡CNA + CH3I => HC≡CCH3 + Nax
HC≡CCH3 adalah yang betul, juga dikenali sebagai Metilacetylene.
Struktur kimia alkina
 Struktur Kimia Alquino
Struktur Kimia Alquino Apakah struktur alkynes? Dalam imej atas molekul asetilena ditunjukkan. Geometri linear pautan c≡C dapat jelas daripadanya.
Oleh itu, di mana terdapat ikatan tiga, struktur molekul mestilah linear. Ini adalah satu lagi perbezaan yang ketara antara mereka dan selebihnya hidrokarbon.
Ia boleh melayani anda: sikopropana (c3h6)Alkanes biasanya diwakili sebagai zigzag, kerana mereka mempunyai hibridisasi SP3 dan pautan mereka dipisahkan 109º. Mereka sebenarnya rantai tetrahedra bersatu kovalen. Sementara alkena rata oleh hibridisasi SP2 karbonnya, membentuk lebih khusus satah trigonal dengan pautan yang dipisahkan sebanyak 120º.
Dalam alkynes, hibridisasi orbital adalah SP, iaitu, mereka mempunyai 50% daripada S dan 50% daripada P. Terdapat dua orbital hibrid SP yang dikaitkan dengan atom H dalam kumpulan asetilena atau alkyne di Alkines.
Jarak kedua H atau R adalah 180º, sebagai tambahan kepada fakta bahawa hanya dengan cara ini orbital karbon tulen dapat membentuk ikatan tiga. Atas sebab ini pautan -c≡C- linear. Melihat struktur mana -mana molekul yang -caring- sorotan di kawasan -kawasan di mana rangka itu sangat linear.
Jarak dari pautan dan sedekah terminal
Karbon dalam ikatan triple berada pada jarak yang lebih kecil daripada dua kali ganda atau pautan mudah. Dalam erti kata lain, c≡C lebih pendek daripada c = c dan c-c. Akibatnya, pautan lebih kuat kerana kedua -dua pautan π menyumbang untuk menstabilkan pautan mudah σ.
Sekiranya ikatan triple berada di hujung rantai, maka ia adalah alkyne terminal. Oleh itu formula sebatian tersebut mestilah HC≡CR, di mana H menyatakan akhir atau permulaan rantai.
Jika sebaliknya ia adalah pautan dalaman triple, formula adalah rc≡Cr ', di mana r dan r' adalah sebelah kanan dan kiri rantai.
Nomenklatur Alquinos
Bagaimana Alkin Dilantik mengikut peraturan yang ditentukan oleh IUPAC? Dengan cara yang sama seperti Alquenos dan Alkenes telah dilantik. Untuk melakukan ini, akhiran -o atau -eno untuk akhiran -ino diubah.
Contohnya: HC≡CCH3 Ia dilantik tip, kerana ia mempunyai tiga karbon, seperti propana (CHO3Ch2Ch3). HC≡CCH2Ch3 Ia adalah 1-butino, yang merupakan alkyne terminal. Tetapi dalam hal Cho3C≡CCH3 Ini adalah 2-butino, dan dalam hal ini pautan triple bukan terminal tetapi dalaman.
Ch3C≡CCH2Ch2(Ch3)2 Ia adalah 5-methyl-2-hexine. Karbon bermula dari sisi yang paling dekat dengan pautan tiga.
Satu lagi jenis alkina adalah sikloalquins. Bagi mereka sudah cukup untuk menggantikan akhiran -o oleh -ino cycloalcan yang sepadan. Oleh itu, siklopropane yang mempunyai ikatan triple dinamakan sebagai siklopropin (yang tidak wujud).
Apabila terdapat dua pautan tiga, awalan DI ditambah ke nama-. Ia mempunyai contoh untuk HC≡C-C≡H, diacetylene atau propadine; Dan kepada HC≡C-C-C≡H, Butadiino.
Alquinos menggunakan
Acetylene atau etino
Yang terkecil dari alkynes menebal jumlah penggunaan yang mungkin untuk hidrokarbon ini. Dari situ melalui Alks, sebatian organik lain boleh disintesis. Ia juga menjalani tindak balas oksidatif untuk mendapatkan etanol, asid asetik, asid akrilik, antara lain.
Boleh melayani anda: lithium hidrida: struktur, sifat, mendapatkan, kegunaanLain -lain kegunaannya terdiri daripada menyediakan sumber haba untuk merangsang elektron atom; Lebih spesifik, e kation logam dalam penentuan oleh pelepasan penyerapan atom, teknik spektroskopi yang digunakan secara meluas.
Alkin semulajadi
Satu -satunya kaedah yang sedia ada untuk menyediakan alkynes bukan sahaja sintetik atau dengan aplikasi haba tanpa ketiadaan oksigen, tetapi juga biologi.
Dalam enzim ini dipanggil Acetylese, yang boleh menafikan ikatan berganda. Terima kasih kepada ini, banyak sumber alkynes semula jadi yang dicapai.
Berikutan itu, sumber -sumber ini boleh diekstrak racun, antidot, ubat -ubatan atau sebatian lain yang memberikan manfaat; Terutama apabila ia menyangkut kesihatan. Alternatifnya banyak ketika mengubah struktur asal mereka dan menjadikannya sebagai sokongan untuk alkina baru.
Contoh Alkynes
Sejauh ini banyak contoh alkina telah disebutkan. Walau bagaimanapun, ada yang berasal dari sumber yang sangat spesifik atau mempunyai struktur molekul tertentu: mereka adalah polyacetyle.
Ini bermakna terdapat lebih daripada satu pautan tiga yang merupakan sebahagian daripada struktur yang sangat besar, dan bukan hanya rantai berkarbonat yang mudah.
Asid tariric
 Struktur asid taryric
Struktur asid taryric Asid tariric berasal dari tumbuhan yang terletak di Guatemala yang dipanggil Picramnia Tariri. Ia secara khusus diekstrak dari minyak dari benihnya.
Dalam struktur molekulnya satu pautan triple tunggal dapat diperhatikan yang memisahkan ekor apolar dari kepala kutub; Oleh itu ia boleh dianggap sebagai molekul amphipatic.
Histrionicotoxin
 Struktur Histrionicotoxin
Struktur Histrionicotoxin Histrionicotoxin adalah racun yang dipisahkan oleh kulit penduduk Colombia, Brazil dan negara -negara Amerika Latin yang lain. Ia mempunyai dua pautan konjugasi tiga kali dengan ikatan berganda. Kedua -duanya adalah terminal dan dipisahkan oleh cincin enam -karbon dan amina kitaran.
Cicutoxin
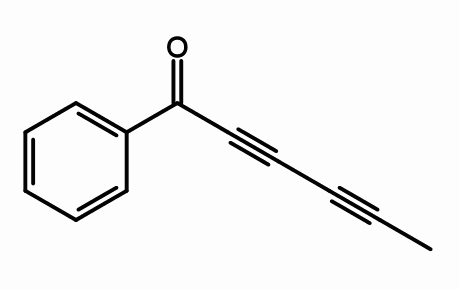 Struktur cicutoxin. Oleh giorgiogp2 [cc by-sa 3.0 (https: // creativeCommons.Org/lesen/by-sa/3.0) atau GFDL (http: // www.gnu.Org/copyleft/fdl.html)], dari Wikimedia Commons
Struktur cicutoxin. Oleh giorgiogp2 [cc by-sa 3.0 (https: // creativeCommons.Org/lesen/by-sa/3.0) atau GFDL (http: // www.gnu.Org/copyleft/fdl.html)], dari Wikimedia Commons Dari struktur molekul cicutoxin, di mana pautan tiga? Sekiranya ikatan berganda rata, kerana ia dilihat betul, dan pautan mudah adalah tetrahedrals, seperti di hujungnya, triple adalah linear dan berada di cerun (\).
Kompaun ini terdiri daripada neurotoksin yang terdapat terutamanya di kilang penyembuhan akuatik.
Capillina
 Struktur Capillina. Oleh Klever [CC0], dari Wikimedia Commons
Struktur Capillina. Oleh Klever [CC0], dari Wikimedia Commons Ia adalah alkyne yang hadir di minyak pati tumbuhan Artemis yang digunakan sebagai agen antikulat. Dua pautan tiga kali berturut -turut dapat diperhatikan, lebih banyak dikonfirmasi dengan betul.
Apakah maksudnya? Bahawa ikatan triple bergema sepanjang rantaian karbon keseluruhan dan melibatkan ikatan ganda c = o dibuka kepada c-o-.
Pargilin
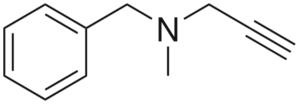 Struktur Pargilin
Struktur Pargilin Ia adalah satu -satunya aktiviti antihipertensi. Menganalisis strukturnya di bahagian adalah: kumpulan benchilo di sebelah kiri, amina tertiari di tengah, dan kanan -wing; iaitu kumpulan harta terminal.
Rujukan
- Francis a. Tortoiseshell. Kimia organik. Asid karboksilik. (Edisi Keenam., Halaman 368-397). MC Graw Hill.
- Brennan, John. (10 Mac, 2018). Contoh Alkynes. Saintifik. Diambil dari: saintifik.com
- Byju's. (2018). Ikatan tiga dalam alkynes. Diambil dari: Byjus.com
- Ensiklopedia Contoh (2017). Alkynes. Pulih dari: contoh.co
- Kevin a. Boudreaux. Alkynes. Diambil dari: Angelo.Edu
- Robert c. Neuman, jr. Alkenes dan Alkynes. [Pdf]. Diambil dari: chem.UCR.Edu

