Watak logam
- 1163
- 182
- Clarence Greenholt DDS
Apakah watak logam?
Dia Watak logam elemen Jadual berkala merujuk kepada semua pembolehubah, kimia dan fizikal, yang menentukan logam atau membezakannya dari bahan -bahan lain yang lain. Mereka biasanya cerah, padat, keras, tinggi terma dan elektrik, boleh dibentuk dan dikeluarkan.
Walau bagaimanapun, tidak semua logam mempamerkan ciri -ciri tersebut; Contohnya, dalam hal merkuri, ini adalah cecair hitam terang. Juga, pembolehubah ini bergantung pada tekanan terestrial dan keadaan suhu. Contohnya, hidrogen yang tidak dapat dipertahankan secara fizikal dapat bertindak secara fizikal sebagai logam dalam keadaan yang melampau.
Syarat -syarat ini boleh: di bawah tekanan buruk atau suhu yang sangat sejuk di sekitar sifar mutlak. Untuk menentukan sama ada elemen adalah logam atau tidak, perlu mempertimbangkan corak tersembunyi di mata pemerhati: corak atom.
Ini mendiskriminasi lebih ketepatan dan kebolehpercayaan apa unsur -unsur logam, dan bahkan elemen apa yang lebih logam daripada yang lain.
Dengan cara ini, watak logam sebenar duit syiling emas terletak lebih banyak mengenai sifat -sifat atomnya daripada yang ditentukan oleh jisim emasnya, malah kedua -duanya berkait rapat.
Antara syiling yang manakah lebih logam: salah satu emas, satu tembaga atau platinum? Jawapannya adalah platinum, dan penjelasannya terletak pada atomnya.
Bagaimana berbeza sifat logam unsur -unsur dalam jadual berkala?
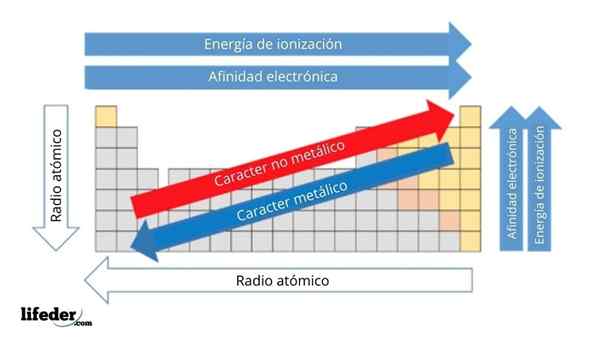
Di bahagian atas, anda mempunyai sifat berkala unsur -unsur. Baris sesuai dengan tempoh dan lajur kepada kumpulan.
Karakter logam berkurangan dari kiri ke kanan jadual berkala, dan meningkat ke arah yang bertentangan. Begitu juga, watak logam meningkat dari atas ke bawah dan berkurangan kerana tempoh dikunjungi ke kepala kumpulan.
Ia boleh melayani anda: asas: ciri dan contohDengan cara ini, unsur -unsur yang dekat dengan arah yang mana titik anak panah, mempunyai watak logam yang lebih besar daripada yang terletak di arah yang bertentangan (blok kuning).
Di samping itu, anak panah yang lain sesuai dengan sifat berkala yang lain, yang menentukan dalam erti kata mereka meningkat atau berkurangan kerana elemen itu "logam". Sebagai contoh, unsur -unsur blok kuning, walaupun mereka mempunyai watak logam yang rendah, pertalian elektronik dan tenaga pengionan mereka tinggi.
Dalam kes radio atom, semakin besar, lebih banyak metalik elemen adalah; Ini ditunjukkan oleh anak panah biru.
Sifat elemen logam
Dalam jadual berkala diperhatikan bahawa logam mempunyai radio atom yang besar, tenaga pengionan yang rendah, afinitas elektronik yang rendah dan elektronegativiti yang rendah. Cara menghafal semua sifat ini?
Titik yang mereka mengalir adalah kereaktifan (electropositivity) yang mentakrifkan logam, yang mengoksidakan; iaitu, mereka kehilangan elektron dengan mudah.
Apabila mereka kehilangan elektron, logam membentuk kation (m+). Oleh itu, unsur -unsur dengan kation bentuk watak metalik tertinggi lebih mudah daripada watak logam yang lebih rendah.
Contoh di atas adalah untuk mempertimbangkan kereaktifan unsur -unsur kumpulan 2, logam alkalinoterapi. Beryllium kurang logam daripada magnesium, dan ini seterusnya kurang logam daripada kalsium.
Jadi sehingga sampai ke Bario Metal, yang paling reaktif kumpulan (selepas radius, elemen radioaktif).
Bagaimana jejari atom pada kereaktifan logam mempengaruhi?
Apabila jejari atom meningkat, elektron Valencia jauh dari nukleus, sehingga mereka dikekalkan dengan kekuatan yang kurang dalam atom.
Boleh melayani anda: Natrium hidroksida (NaOH): Struktur, sifat, kegunaan, sintesisWalau bagaimanapun, jika tempoh dilalui ke sebelah kanan jadual berkala, nukleus menambah proton ke tubuhnya, kini lebih positif, yang menarik elektron valensi lebih kuat, mengurangkan saiz jejari atom. Ini mengakibatkan penurunan watak logam.
Oleh itu, atom yang sangat kecil dan dengan nukleus yang sangat positif cenderung untuk mendapatkan elektron dan bukannya kehilangannya (unsur -unsur bukan logam), dan mereka yang boleh menang dan kehilangan elektron, dianggap metalloides. Boron, Silicon, Germanio dan Arsenic adalah beberapa metalloid ini.
Sebaliknya, jejari atom juga meningkat jika terdapat ketersediaan tenaga baru untuk orbital lain, yang berlaku ketika turun dalam satu kumpulan.
Atas sebab ini, apabila turun dalam jadual berkala, radio menjadi besar dan teras menjadi tidak dapat menghalang spesies lain daripada merebut elektron dari lapisan luar mereka.
Di makmal, dengan ejen pengoksidaan yang kuat seperti asid nitrik yang dicairkan (HNO3)- reaktiviti logam dalam menghadapi pengoksidaan dapat dikaji.
Begitu juga, proses pembentukan halida logam mereka (NaCl, misalnya) juga merupakan eksperimen demonstrasi kereaktifan ini.
Elemen watak logam yang lebih besar
 Cesium
Cesium Arah anak panah biru dalam imej jadual berkala membawa kepada unsur -unsur Francio dan Cesio. Francio lebih logam daripada cesium, tetapi tidak seperti yang terakhir, Francio adalah buatan dan radioaktif. Atas sebab ini, cesium menduduki tempat unsur semula jadi watak logam yang lebih besar.
Boleh melayani anda: Besi oksidaMalah, salah satu tindak balas yang paling terkenal (dan letupan) yang diketahui adalah yang berlaku apabila sekeping (atau titisan) cesium bersentuhan dengan air.
Kereaktifan yang tinggi dari cesium, juga diterjemahkan ke dalam pembentukan sebatian yang lebih stabil, bertanggungjawab untuk melepaskan tenaga secara tiba -tiba:
2cs (s) + 2h2O → 2csoh (aq) + h2(g)
Persamaan kimia membolehkan melihat pengoksidaan cesium dan pengurangan hidrogen air ke hidrogen gas.
Elemen watak logam yang lebih rendah
 Model fluorin 3D
Model fluorin 3D Di dalam pepenjuru yang bertentangan, di sudut kanan atas jadual berkala, fluorida (F2, Imej unggul) Memimpin senarai unsur bukan logam. Kerana? Kerana ia adalah elemen dalam sifat elektronegatif yang paling banyak dan yang mempunyai tenaga pengionan terendah.
Dalam erti kata lain, ia bertindak balas dengan semua elemen jadual berkala untuk membentuk ion f- dan bukan f+.
Fluorin sangat tidak mungkin kehilangan elektron dalam tindak balas kimia, agak bertentangan dengan logam. Oleh sebab itu, ia adalah unsur watak logam yang lebih rendah.
Rujukan
- Lumen, kimia untuk bukan major. Watak logam dan nonmetalllic. Pulih dari kursus.Lumenning.com
- Tugasan Kimia. (2018). Elektropostiviti atau watak logam. Pulih dari penyerahan kimia.com
- Juan Ramos. Senarai lengkap logam dan bukan logam. Pulih dari sciencetrends.com
- Anne Marie Helmestine, Ph.D. Sifat dan trend watak logam. Pulih dari pemikiran.com

