Beban nuklear yang berkesan
- 1620
- 349
- Kerry Schmitt
Apa beban nuklear yang berkesan?
The Beban nuklear yang berkesan (diwakili sebagai zEff Dan dalam beberapa kes seperti z*) Ia adalah beban nuklear bersih yang pengalaman elektron ketika berada dalam atom polyhelectronic (iaitu, ia mempunyai lebih dari satu elektron).
Dengan cara yang lebih tepat, ia adalah caj elektrik yang akan mempunyai teras atom hipotesis yang mampu menarik satu -satunya elektron dengan daya yang sama dengan inti atom sebenar menarik elektron yang sama dengan kehadiran semua elektron lain.
Ia adalah beban nuklear yang diperbetulkan yang mengambil kira kesan kehadiran elektron lain pada atom polilekronic. Beban yang dikurangkan ini menerangkan mengapa elektron paling luar dalam atom polyhelectronic dikaitkan dengan nukleus daripada elektron dalaman.
Beban nuklear yang berkesan adalah konsep yang sangat penting dalam kimia, kerana ia membolehkan kita memahami kecenderungan berkala banyak sifat seperti jejari atom, jejari ion, elektronegativiti, tenaga pengionan dan banyak lagi.
Mengapa beban nuklear yang berkesan wujud?
Beban nuklear yang berkesan timbul dari dua fenomena:
- Kesan perisai elektron pada atom polyhelectronic.
- Penolakan elektrostatik di kalangan elektron kerana setiap orang mempunyai cas elektrik yang sama.
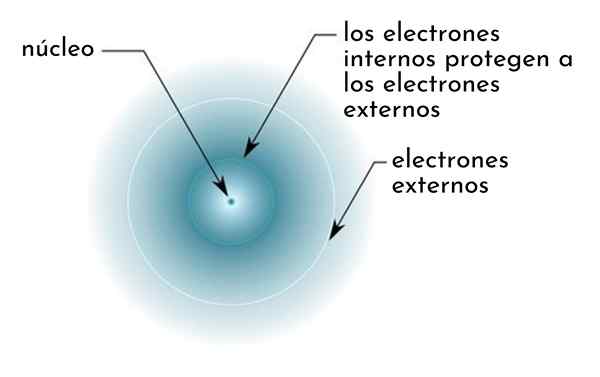
Dia kesan perisai Ia terdiri daripada sejenis perisai yang dibentuk oleh elektron dalaman atom yang meliputi nukleus. Ini menjadikan elektron paling luar "merasakan" tarikan yang lebih rendah di bahagian nukleus daripada yang mereka rasakan jika elektron lain tidak hadir.
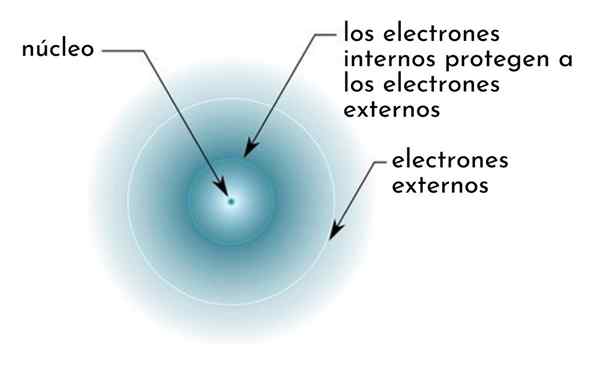 Rajah secara skematik menunjukkan elektron dalaman bertindak sebagai skrin yang melindungi elektron luaran tarikan nukleus
Rajah secara skematik menunjukkan elektron dalaman bertindak sebagai skrin yang melindungi elektron luaran tarikan nukleus Sebagai contoh, beban nuklear atom natrium ialah +11 (nombor atomnya adalah z = 11), tetapi, satu -satunya elektron valencia yang dimiliki, sebenarnya merasakan daya tarikan beban hanya +2,2.
Boleh melayani anda: Natrium benzoat: struktur, sifat, kegunaan dan risikoDalam erti kata lain, pelindung 10 elektron dalaman yang lain menyebabkan elektron valencia natrium merasakan daya tarikan nuklear hanya kelima dari apa yang sepatutnya.
Sebagai tambahan kepada kesan perisai, penolakan antara elektron (yang mempunyai caj elektrik yang sama) juga menyumbang untuk mengatasi kapasiti teras untuk menarik elektron luaran. Iaitu, penolakan ini juga membantu mengurangkan beban nuklear yang berkesan.
Ciri -ciri penting beban nuklear yang berkesan
Harus diingat bahawa kesan perisai yang bertanggungjawab untuk mengurangkan beban nuklear yang berkesan hanya mempengaruhi elektron yang berada dalam tahap tenaga yang sama atau di lapisan atas, tetapi bukan elektron paling dalaman. Di samping itu, kesannya tidak sama untuk elektron yang terdapat dalam orbital atom S dan P daripada yang terdapat dalam orbital D dan F F dan F.
Atas sebab ini, setiap set elektron setiap lapisan atau tahap tenaga merasakan beban nuklear yang berbeza. Ini mempunyai implikasi penting mengenai sifat kimia unsur -unsur yang berbeza.
Trend berkala beban nuklear yang berkesan
Dalam tempoh
Elektron yang terletak di tahap tenaga yang sama kurang melindungi daripada yang terdapat di tahap tenaga yang lebih rendah.
Oleh sebab itu, kesan perisai tidak meningkat dengan ketara ketika kita bergerak dalam tempoh, tetapi beban nuklear sebenar. Atas sebab ini, beban nuklear yang berkesan kenaikan dari kiri ke kanan dalam jadual berkala.
Sepanjang satu kumpulan
Sebaliknya, ketika berlalu dari satu tempoh ke kumpulan yang sama (ia. Ini menjadikan beban nuklear yang berkesan berkurangan dari atas ke bawah atau, apa yang sama, meningkat dari bawah ke atas.
Boleh melayani anda: AyaroínaFormula beban nuklear yang berkesan
Beban nuklear yang berkesan boleh dikira dengan cara persamaan separuh masa yang sangat mudah yang mengambil kira nilai sebenar beban nuklear (diberikan oleh nombor atom, z) dan istilah yang dipanggil perisai malar. Yang terakhir merangkumi kesan kehadiran elektron lain dalam satu.
Persamaan diberikan oleh:
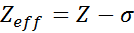
di mana z ialah nombor atom dan σ (sigma huruf Yunani) mewakili pemalar perisai, yang bergantung kepada konfigurasi elektronik.
Peraturan Slater
Pemalar perisai boleh dianggarkan dari sistem yang dikenali sebagai peraturan Slater. Peraturan ini membolehkan mengira pemalar perisai elektron dengan menambahkan sumbangan elektron lain untuk mengatakan perisai pemalar. Peraturan ini boleh diringkaskan seperti berikut:
- Mana -mana elektron yang berada pada tahap tenaga yang sama (tahap n0) Menyediakan jumlah 0.35 kepada pemalar perisai, melainkan kedua -duanya berada pada tahap 1, di mana ia menyediakan 0.30.
- Setiap elektron yang berada di tahap terdahulu (pada tahap n0-1) dalam orbital s atau p, ia membawa 0.85; Sebaliknya, jika ia berada di orbital d atau f ia menyumbang 1.
- Semua elektron lain yang berada pada tahap tenaga yang lebih rendah (n0-2, n0-3, dll.), menyumbang 1 kepada pemalar perisai.
Contoh pengiraan beban nuklear yang berkesan
Valencia Electron of the Natrium Atom
Konfigurasi elektronik atom natrium adalah 1s22s22 p63s1. Iaitu jika kita mahu mengira beban nuklear yang berkesan yang dirasakan oleh elektron Valencia (elektron 3s1), kita mesti menambah sumbangan 10 elektron yang lain mengikut peraturan Slater.
Boleh melayani anda: Besi oksida (ii): struktur, nomenclature, sifat, kegunaanBagaimana kita mengira pemalar perisai elektron 3s1 (n0= 3) Dan ini bersendirian di lapisan Valencia, tidak ada elektron lain pada tahap tenaga yang sama.
Tahap terdahulu adalah n0-1 = 2, di mana terdapat 8 elektron dalam orbital s atau p yang menyumbang 0.85 setiap satu, dan tidak ada elektron dalam orbital d atau f.
Akhirnya, satu -satunya tahap yang lebih rendah daripada 2 adalah n = 1, di mana terdapat hanya 2 elektron. Semua ini diringkaskan dalam jadual berikut:
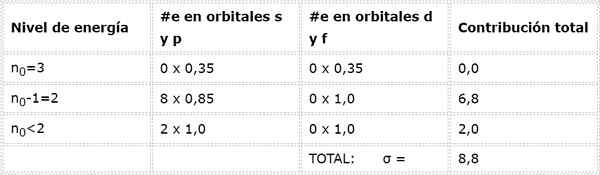
Seperti yang dapat dilihat, elektron dalaman natrium menyediakan pemalar perisai 8.8, jadi beban nuklear yang berkesan yang dirasakan oleh elektron 3s1 adalah:
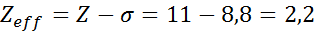
Elektron Arsenik Valencia
Konfigurasi elektronik arsenik adalah 1s22s22 p63s23p63d104s24p3. Lapisan Valencia adalah lapisan 4 (n0= 4) yang mempunyai 5 elektron: (4s24p3). Dalam kes ini, setiap 5 elektron ini akan merasakan kesan 4 yang lain yang berada dalam lapisan yang sama dan yang lain 28 elektron dalaman seperti yang ditunjukkan dalam jadual:
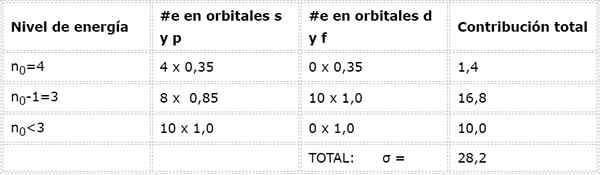
Oleh itu, beban nuklear yang berkesan yang dirasakan oleh elektron arsenik adalah: