Asid hyposulfurous
- 3421
- 234
- Ms. Santos Fritsch
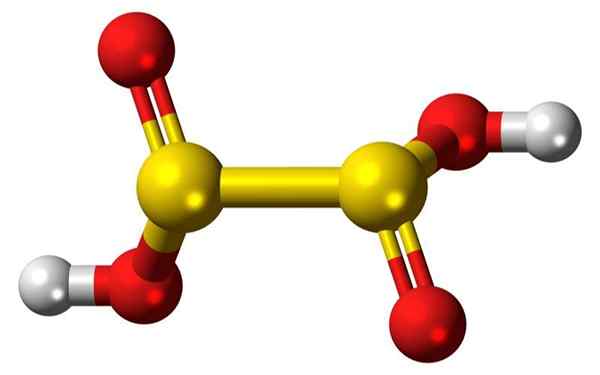
 Bar 3d bar dan belon molekul asid hiposulfur. Sumber: Jynto
Bar 3d bar dan belon molekul asid hiposulfur. Sumber: Jynto Apa itu asid hiposulfur?
Dia Asid hyposulfurous, o asid dionik, tidak diketahui, tidak stabil semata -mata, ia tidak mempunyai kewujudan bebas dan belum dikesan dalam larutan akueus.
Secara teorinya, ia akan menjadi asid yang agak lemah, setanding dengan asid sulfur, H2SO3. Hanya garam mereka yang diketahui, Dionitos, yang stabil dan ejen pengurangan yang kuat. Garam asid natrium dionik adalah natrium dionito.
Formula
Formula asid hyposulfurous adalah seperti berikut:
Asid dionik: h2S2Sama ada4
Anion Dionito: S2O42-
Natrium Dionito: NA2S2Sama ada4
Nombor CAS: 20196-46-7 asid hiposulfur (atau dital)
Nombor CAS: 14844-07-6 asid hiposulfur (atau dition, ion)
Nombor CAS: 7775-14-6 Natrium Dionito (Natrium Natrium Asid Ditoring)
Sifat fizikal dan kimia
- Di dalam garam natrium Dionito, penampilannya adalah debu kristal, putih hingga kelabu, dengan serpihan hijau lemon yang ringan dan lemah.
- Berat molekul asid gumpalan ialah 130.132 g/mol. Anion Dionito, 128.116 g/mol, dan natrium Dionito, 174.096 g/mol.
- Pada titik mendidih natrium dionito, ia terurai, dan titik leburnya ialah 52 ° C.
- Ketumpatan natrium dionito adalah 2.38 g/cm³ (anhydrous), dan kelarutannya dalam air adalah 18.2 g/100 ml (anhydrous, 20 ° C).
- Asid hyposulfurous adalah oxoacid sulfur dengan formula kimia h2S2Sama ada4.
- Oxoacid sulfur adalah sebatian kimia yang mengandungi sulfur, oksigen dan hidrogen. Walau bagaimanapun, sesetengah daripada mereka hanya dikenali dengan garam mereka (seperti asid hiposulfur, asid dition, asid disulfida dan asid sulfur).
Ia boleh melayani anda: piridin: struktur, sifat, kegunaan, ketoksikan, sintesisAntara ciri -ciri struktur oxoacid yang kita ada:
- Tetrahedral sulfur apabila diselaraskan dengan oksigen.
- Atom oksigen di jambatan dan terminal.
- Kumpulan berkala.
- S = s terminal.
- Rantai (-s-) n
Asid sulfurik adalah sulfur oxoacid yang paling terkenal.
- Anion Dionito ([s2Sama ada4] 2-) adalah oxoanion (ion dengan formula generik axoy z-) sulfur secara rasmi berasal dari asid dition.
- Ion Dionito mengalami hidrolisis asid dan alkali ke thiosulfate dan bisulfite, dan sulfit dan sulfida.
- Garam asid natrium dionik adalah natrium dionite (juga dikenali sebagai natrium hidrosulfite).
- Ia boleh didapati dari natrium bisulfite melalui reaksi berikut:
2 Nahso3 + Zn → Na2SW4 + Zn (OH) ²
Aplikasi
Ion Dionite sering digunakan bersamaan dengan ejen kompleks (contohnya, asid sitrik), untuk mengurangkan besi oxi-hydroksida (III) dalam sebatian besi larut (ii) dan menghapuskan fasa mineral amorf yang mengandungi besi (iii) di dalam tanah analisis (pengekstrakan selektif).
Dionito membolehkan meningkatkan kelarutan besi. Terima kasih kepada pertalian kuat Ion Dionito untuk kation logam bivalen dan trivalen, ia digunakan sebagai ejen chelating.
Penguraian Dionito menghasilkan spesies sulfur yang dikurangkan yang boleh menjadi sangat agresif untuk kakisan keluli dan keluli tahan karat.
Antara aplikasi natrium Dionito yang kita ada:
Dalam industri
- Kompaun ini adalah garam larut air, dan boleh digunakan sebagai ejen pengurangan dalam larutan berair.
- Ia digunakan seperti dalam beberapa proses pewarna perindustrian, terutamanya yang melibatkan pewarna sulfur dan pewarna tab, di mana pewarna tidak larut air dapat dikurangkan ke garam logam alkali yang larut air (contohnya, pewarna indigo).
Boleh melayani anda: asid: ciri dan contoh- Sifat pengurangan natrium dionito juga menghapuskan pewarna yang berlebihan, oksida sisa dan pigmen yang tidak diingini, dengan itu meningkatkan kualiti warna global.
- Natrium Dionito juga boleh digunakan untuk rawatan air, pembersihan gas, pembersihan dan pengekstrakan. Ia juga boleh digunakan dalam proses perindustrian seperti ejen sulfonan atau sumber natrium.
- Sebagai tambahan kepada industri tekstil, sebatian ini digunakan dalam industri berkaitan kulit, makanan, polimer, fotografi, dan banyak lagi. Ia juga digunakan sebagai ejen decolorating dalam reaksi organik.
Dalam sains biologi
- Natrium Dionito sering digunakan dalam eksperimen fisiologi sebagai cara untuk mengurangkan potensi penyelesaian redoks.
Dalam sains geologi
- Natrium Dionito sering digunakan dalam eksperimen kimia tanah untuk menentukan jumlah besi yang tidak dimasukkan ke dalam mineral silikat utama.
Keselamatan dan risiko
Manipulasi elemen ini mesti dilakukan dalam keadaan penjagaan yang melampau. Ia sangat toksik dan boleh bertindak balas dengan bahaya bersama dengan air dan udara.
Seterusnya, kami menyerlahkan beberapa aspek.
Tindak balas udara dan air
- Natrium Dionito adalah bahan bakar pepejal yang terurai perlahan -lahan apabila ia bersentuhan dengan air atau wap air, membentuk thiosulfates dan bisulfites.
- Reaksi ini menghasilkan haba, yang dapat mempercepatkan tindak balas atau menyebabkan bahan -bahan sekitarnya dibakar. Sekiranya campuran terkurung, tindak balas penguraian dapat mengakibatkan penekanan bekas, yang dapat dipecahkan dengan kuat. Apabila tinggal di udara, ia mengoksidakan perlahan -lahan, menghasilkan gas sulfur dioksida toksik.
Boleh melayani anda: nitrofurans: ciri, mekanisme tindakan dan klasifikasiBahaya kebakaran
- Natrium Dionito adalah bahan mudah terbakar dan mudah terbakar. Boleh meradang apabila bersentuhan dengan udara basah atau kelembapan. Anda boleh membakar dengan cepat dengan kesan suar. Boleh bertindak balas dengan kuat atau meletup dengan air.
- Boleh dipecahkan secara meletup apabila dipanaskan atau terlibat dalam api. Dapat menghidupkan semula setelah api dipadamkan. Runoff dapat menimbulkan kebakaran atau bahaya letupan. Bekas boleh meletup apabila dipanaskan.
Bahaya kesihatan
- Apabila bersentuhan dengan api, natrium dionito akan menghasilkan gas yang menjengkelkan, menghakis dan/atau toksik. Penyedutan produk penguraian boleh menyebabkan kecederaan serius atau kematian. Hubungan dengan bahan boleh menyebabkan luka bakar serius pada kulit dan mata. Larian kawalan kebakaran boleh menyebabkan pencemaran.
Rujukan
- Benjah-bmm27 (2006). Model bola-dan-melekat ion dithionite [imej] pulih dari.Wikipedia.org.
- Mills, b. (2009). Natrium-dithionite -xtal-1992-3d-Balls [image] pulih dari: dalam.Wikipedia.org.

