Struktur, CRCL3) Struktur, Hartanah, Kegunaan Chrome Chrome

- 1636
- 427
- Delbert Dare
Dia Chrome Chloride (CRCL3) Ia adalah garam bukan organik yang terdiri daripada cation cr3+ dan cl anion- dalam perkadaran 1: 3; iaitu, untuk setiap cr3+ Terdapat tiga CL-. Seperti yang akan dilihat kemudian, interaksi mereka bukan ionik. Garam ini boleh berlaku dalam dua bentuk: anhydra dan hexahydrate.
Bentuk anhydrous dicirikan dengan menyampaikan pewarnaan violet-Reddish; Semasa Hexahydrate, CRCL3.6H2Atau, ia berwarna hijau gelap. Penggabungan molekul air mengubah sifat fizikal kristal ini; sebagai titik mendidih dan gabungan, kepadatan, dll.
 Kristal-kristal violet krom klorida (iii) anhydrous. Sumber: Ben Mills [Domain Awam]
Kristal-kristal violet krom klorida (iii) anhydrous. Sumber: Ben Mills [Domain Awam] Chrome Chloride (III) (mengikut nomenklatur stok) terurai pada suhu tinggi, menjadi Chrome Chloride (II), CRCL2. Ia menghakis logam, walaupun digunakan dalam krom: prosedur di mana logam ditutup dengan lapisan krom nipis.
Cr3+, Datang dari klorida masing -masing, ia telah digunakan dalam rawatan diabetes, terutamanya pada pesakit dengan jumlah pemakanan parenteral (TPN), yang tidak menelan jumlah krom yang diperlukan. Walau bagaimanapun, hasilnya jauh lebih baik (dan lebih dipercayai) jika ia dibekalkan sebagai picolinato.
[TOC]
Struktur Chrome Chloride
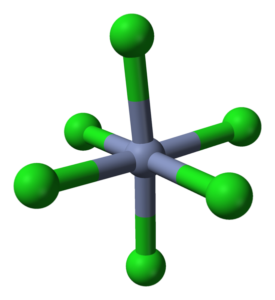 Koordinasi Octaedro untuk CRCL3 dalam kristalnya. Sumber: Ben Mills [Domain Awam]
Koordinasi Octaedro untuk CRCL3 dalam kristalnya. Sumber: Ben Mills [Domain Awam] CRCL3 Walaupun garam, sifat interaksi mereka bukan semata -mata ionik; Mereka mempunyai watak kovalen tertentu, produk koordinasi antara Cr3+ dan Cl-, yang menimbulkan octahedron yang cacat (imej unggul). Chrome terletak di tengah -tengah oktaedro, dan kloros di simpulnya.
CRCL Octahedron6 Anda boleh, pada pandangan pertama, bercanggah dengan formula CRCL3; Walau bagaimanapun, octahedron lengkap ini tidak menentukan sel unit kaca, tetapi kiub (juga cacat), yang memotong sfera hijau atau anion klorin pada separuh.
Boleh melayani anda: 20 contoh penyejatan dan ciri kimiaLapisan kristal anhydrous
Oleh itu, sel kesatuan dengan octaedro ini terus mengekalkan perkadaran 1: 3. Menghasilkan semula kiub yang cacat ini di ruang angkasa, kristal CRCL diperolehi3, yang diwakili dalam imej unggul dengan model pengisian tiga dimensi, dan model sfera dan bar.
 Lapisan struktur kristal CRCL3 diwakili dengan model sfera dan bar tiga dimensi. Sumber: Ben Mills [Domain Awam]
Lapisan struktur kristal CRCL3 diwakili dengan model sfera dan bar tiga dimensi. Sumber: Ben Mills [Domain Awam] Lapisan kristal ini adalah salah satu daripada banyak yang membuat3 (Jangan mengelirukan warna kaca, benar, dengan sfera hijau).
Seperti yang dapat dilihat, anion cl- Mereka menduduki permukaan, jadi beban negatif mereka menghalau lapisan kristal yang lain. Akibatnya, kristal menjadi penipuan dan rapuh; Tetapi cemerlang, kerana krom.
Sekiranya lapisan yang sama divisualisasikan dari perspektif sisi, ia akan diperhatikan, bukannya octahedra, tetraheders yang diputarbelitkan:
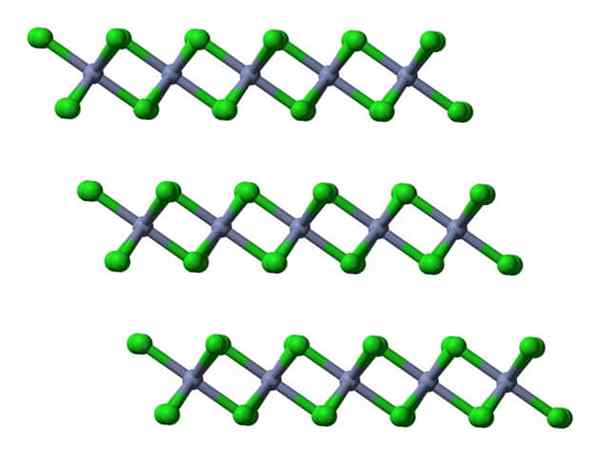 Lapisan kristal CRCL3 melihat secara lisan. Sumber: Ben Mills.
Lapisan kristal CRCL3 melihat secara lisan. Sumber: Ben Mills. Di sini pemahaman mengapa lapisan ditolak antara satu sama lain difasilitasi apabila Cl- permukaannya.
Sifat
Nama
-Chrome Chloride (III)
-Chrome Trichloride (III)
-Krom klorida (iii) anhydrous.
Formula kimia
-CRCL3 (anhydrous).
-CRCL3.6H2O (hexahing).
Berat molekul
-158.36 g/mol (anhydrous).
-266.43 g/mol (hexahydrate).
Penerangan fizikal
-Kristal pepejal dan violet-redistik (anhydrous).
-Debu kristal hijau gelap (hexahydrate, imej yang lebih rendah). Dalam hidrat ini dapat dilihat sebagai air menghalang kecerahan, ciri krom logam.
 Hexahydrate Chrome Chrome. Sumber: Pengguna: Walkerma [Domain Awam]
Hexahydrate Chrome Chrome. Sumber: Pengguna: Walkerma [Domain Awam] Takat lebur
-1.152 ºC (2.106 ºF, 1.425 k) (anhydrum)
-83 ºC (hexahydrate).
Takat didih
1300 ºC (2.370 ºF, 1.570) (anhydrum).
Kelarutan air
 Penyelesaian berair Chrome Chloride (III). Sumber: Leiem [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)]
Penyelesaian berair Chrome Chloride (III). Sumber: Leiem [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)] -Sedikit larut (anhydro).
-585 g/l (hexahydrate).
Di bahagian atas, siri tiub ujian yang dipenuhi dengan larutan akueus CRCL ditunjukkan3. Perhatikan bahawa yang lebih pekat, semakin kuat warna kompleks [CR (oh2)6]3+, Warna hijau bertanggungjawab.
Boleh melayani anda: putrescina: struktur, sifat, sintesis, kegunaanKelarutan dalam pelarut organik
Larut dalam etanol, tetapi tidak larut dalam eter (anhydrous).
Ketumpatan
-2.87 gr/cm3 (anhydrous).
-2.76 g/cm3 (Hexahydrate).
Suhu penyimpanan
Penguraian
Apabila dipanaskan ke penguraian, kromium klorida (iii) mengeluarkan asap toksik sebatian yang mengandungi klorin. Sebatian ini juga dikeluarkan apabila Chrome Chloride (III) bersentuhan dengan asid kuat.
Kakisan
Ia sangat menghakis dan boleh menyerang keluli tertentu.
Reaksi
Ia tidak sesuai dengan oksidan yang kuat. Ia juga bertindak balas dengan litium dan nitrogen.
Apabila ia dipanaskan dengan kehadiran hidrogen, ia dikurangkan kepada kromium klorida (II), dengan pembentukan hidrogen klorida.
2 CRCL3 + H2 => 2 CRCL2 + 2 HCl
Ph
Dalam larutan akueus, dan dengan kepekatan 0.2 m: 2.4.
Sintesis
Chrome Chloride (III) Hexahydrate dihasilkan, bertindak balas kromium hidroksida dengan asid hidroklorik dan air.
CR (oh)3 + 3 HCl +3 h2O => CRCL3.6H2Sama ada
Kemudian, untuk mendapatkan garam anhydra, CRCL dipanaskan3.6H2Atau di hadapan Tionilo Chloride, SOCl2, Asid hidroklorik, dan panas:
[CR (H2Sama ada)6] Cl3 + 6socl2 + Δ → CRCL3 + 12 HCl + 6SO2
Sebagai alternatif, CRCL3 Gas klorin diperolehi pada campuran kromium dan karbon oksida.
Cr2Sama ada3 + 3 c +cl2 => 2 CRCL3 + 3 co
Dan akhirnya, sebagai kaedah yang paling banyak digunakan, ia adalah untuk memanaskan oksida dengan agen halogenan, seperti karbon tetraklorida:
Cr2Sama ada3 + 3CCL4 + Δ → 2crcl3 + 3COCL2
Aplikasi
Industrialis
Chrome Chloride campur tangan dalam penyediaan di -tapak krom klorida (II); reagen yang campur tangan dalam pengurangan alkil halida, dan dalam sintesis haluros (e) -salquenilo.
Boleh melayani anda: Natrium oksalat (Na2C2O4): Struktur, sifat, kegunaan, risiko-Ia digunakan dalam teknik krom. Ini terdiri daripada mendepositkan, melalui galvanoplasti, lapisan krom halus pada objek logam atau bahan lain dengan objektif hiasan, sehingga meningkatkan ketahanan kakisan dan juga kekerasan permukaan.
-Ia digunakan sebagai mordan tekstil, berfungsi sebagai hubungan antara bahan pewarnaan dan kain yang akan dicelup. Di samping itu, ia digunakan sebagai pemangkin untuk pengeluaran olefin dan agen kalis air.
Terapeutik
Penggunaan suplemen USP USP Chrome Chloride disyorkan pada pesakit yang hanya menerima penyelesaian intravena, ditadbir untuk jumlah pemakanan parenteral (TPN). Oleh itu, hanya apabila pesakit ini tidak menerima semua keperluan pemakanan mereka.
Kromium (iii) adalah sebahagian daripada faktor toleransi glukosa, pengaktif tindak balas yang dipromosikan oleh insulin. Dianggap bahawa kromium (iii) mengaktifkan metabolisme glukosa, protein dan lipid, memudahkan tindakan insulin pada manusia dan haiwan.
Kromium hadir dalam banyak makanan. Tetapi kepekatannya tidak melebihi 2 oleh jatah, brokoli menjadi makanan dengan sumbangan terbesar (11 μg). Di samping itu, penyerapan usus krom adalah rendah, dengan nilai 0.4 hingga 2.5% daripada jumlah yang ditelan.
Ini menjadikan sukar untuk menubuhkan diet untuk bekalan krom. Pada tahun 1989, Akademi Sains Kebangsaan disyorkan antara 50 hingga 200 μg/hari sebagai pengambilan krom yang mencukupi.
Risiko
Antara kemungkinan risiko penggunaan garam ini sebagai suplemen krom adalah:
-Sakit perut yang kuat.
-Pendarahan yang tidak normal, yang boleh berubah dari kesukaran untuk menyembuhkan luka, lebam merah, atau kegelapan produk najis tahi pendarahan dalaman.
-Kerengsaan dalam sistem pencernaan, menyebabkan ulser perut atau usus.
-Dermatitis
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2019). Kromium (iii) klorida. Diperoleh dari: dalam.Wikipedia.org
- Kromium (iii) klorida [pdf]. Pulih dari: Alpha.Chem.Umb.Edu
- Pubchem. (2019). Chromium chloride hexahydrate. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Institut Kesihatan Kebangsaan. (21 September 2018). Chromium: Lembaran Fakta Tambahan Diet. Diperolehi dari: SDG.OD.NIH.Gov
- Tomlinson Carole a. (2019). Kesan sampingan kromium klorida. Leaf Group Ltd. Pulih dari: sihat.com
- « Mengapa penting untuk dibaca? 10 faedah membaca
- Sejarah Borax, Struktur, Sifat, Kegunaan, Sintesis, Risiko »

