Ciri, latihan, contoh
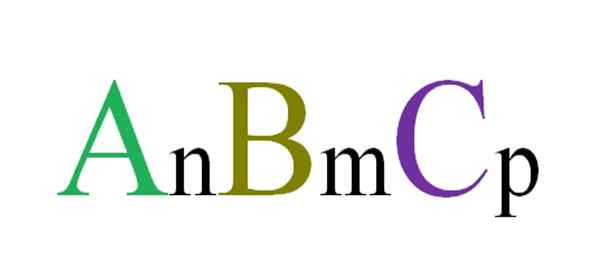
- 2765
- 692
- Ms. Micheal Rippin
The Sebatian ternary Mereka semua yang terdiri daripada tiga atom atau ion yang berbeza. Mereka boleh menjadi sangat pelbagai, dari asid atau bahan asas, kepada aloi logam, mineral atau bahan moden. Tiga atom mungkin tergolong dalam kumpulan yang sama dengan jadual berkala, atau meneruskan lokasi sewenang -wenang.
Walau bagaimanapun, bagi sebatian ternary berlaku mesti ada pertalian kimia antara atomnya. Tidak semua bersesuaian antara satu sama lain, dan oleh itu anda tidak boleh memilih secara rawak yang mana tiga akan mengintegrasikan dan menentukan kompaun atau campuran (dengan mengandaikan kekurangan ikatan kovalen).
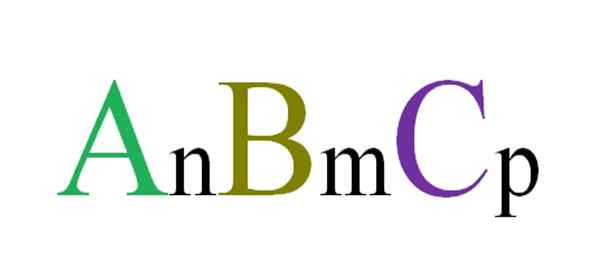 Formula Umum dan Rawak untuk Sebatian Ternary. Sumber: Gabriel Bolívar.
Formula Umum dan Rawak untuk Sebatian Ternary. Sumber: Gabriel Bolívar. Sebagai contoh, tiga huruf dipilih secara rawak yang akan mengawal sebatian ABC Ternary (imej unggul). Subskrip N, M dan P menunjukkan hubungan stoikiometrik antara atom atau ion a, b dan c. Mengubah nilai -nilai subskrip tersebut, dan identiti huruf, sebatian ternary yang tidak berkesudahan diperolehi.
Walau bagaimanapun, formula anBmCp Ia hanya akan sah jika ia memenuhi elektroneutraliti; iaitu jumlah caj anda mestilah sama dengan sifar. Dengan ini, terdapat batasan fizikal (dan kimia) yang membimbing sama ada pembentukan sebatian ternary yang mungkin berlaku.
[TOC]
Ciri -ciri sebatian ternary
Ciri -cirinya tidak umum tetapi berbeza -beza bergantung kepada sifat kimia mereka. Sebagai contoh, oxoacids dan pangkalan adalah sebatian ternary, dan masing -masing berkongsi atau bukan satu siri ciri wakil.
Sekarang, sebelum ABC kompaun hipotetikal, ini boleh menjadi ionik, jika perbezaan elektronegativiti antara A, B dan C tidak besar; atau kovalen, dengan pautan a-b-c. Yang terakhir diberikan dalam contoh tak terhingga dalam kimia organik, seperti alkohol, fenol, eters, karbohidrat, dll., formula yang boleh digambarkan dengan cnHm Sama adap.
Boleh melayani anda: Sifat mekanikal logamOleh itu, ciri -ciri sangat bervariasi dan berayun dalam tahap yang tinggi dari satu sebatian ternary ke yang lain. Kompaun cnHmSama adap Dikatakan bahawa ia adalah oksigen; sementara cnHmNp, Sebaliknya, ia adalah nitrogen (ia adalah amina). Sebatian lain mungkin sulfur, fosforasi, fluorized, atau mempunyai watak logam yang ditandakan.
Asas dan asid
Memajukan dalam bidang kimia bukan organik, anda mempunyai pangkalan logam, mnSama adamHp. Memberi.
Sebagai contoh, asas NaOH, memandangkan subskrip tersebut, harus ditulis sebagai NA1Sama ada1H1 (yang akan huru -hara). Di samping itu, ia akan diandaikan bahawa h adalah sebagai kation h+, Dan bukan bagaimana ia benar -benar muncul: menjadi sebahagian daripada anion oh-. Kerana tindakan oh- Pada kulit, pangkalan ini adalah sabun dan kaustik.
Pangkalan logam adalah bahan ionik, dan walaupun mereka terdiri daripada dua ion, mn+ Dan oh- (NA+ Dan oh- Untuk NaOH), mereka adalah sebatian ternary kerana mempunyai tiga atom yang berbeza.
Asid, sebaliknya, kovalen, dan formula umum mereka adalah Hao, di mana atom bukan logam biasanya. Walau bagaimanapun, memandangkan kemudahan mengion dalam hidrogen yang melepaskan air, ionnya+ Corroen dan menyakiti kulit.
Nomenclature
Seperti ciri -ciri, tatanama sebatian ternary sangat bervariasi. Atas sebab itu, hanya pangkalan, oxoacids dan oxisals akan dianggap secara dangkal.
Pangkalan
Pangkalan logam disebutkan dahulu dengan perkataan 'hidroksida' diikuti dengan nama logam dan valensinya dalam nombor Rom dalam kurungan. Oleh itu, NaOH adalah natrium hidroksida (I); Tetapi sejak natrium mempunyai valensi unik +1, ia tetap hanya sebagai natrium hidroksida.
Ia boleh melayani anda: AlceansAl (oh)3, Sebagai contoh, ia adalah aluminium hidroksida (III); dan cu (oh)2, Hidroksida Tembaga (II). Sudah tentu, semuanya mengikut tatanama yang sistematik.
Oxoacids
Oxóacids mempunyai formula yang agak umum jenis Hao; Tetapi pada hakikatnya, mereka lebih baik digambarkan sebagai AOH. Pautan HA-H muncul H dibebaskan+.
Nomenklatur tradisional adalah seperti berikut: perkataan 'asid' bermula, diikuti dengan nama atom pusat, didahului atau didahului oleh awalan masing -masing (hypo, per) atau akhiran (beruang, ico) mengikut sama ada dia bekerja dengan anak -anaknya atau nilai yang lebih tua.
Sebagai contoh, bromin oxoacids adalah Hbro, Hbro2, Hbro3 dan hbro4. Ini adalah asid: hypobromous, bromic, bromic dan percomic, masing -masing. Perhatikan bahawa dalam semua mereka terdapat tiga atom dengan nilai yang berbeza untuk subskrip mereka.
Oxisals
Juga dipanggil garam nullion, mereka adalah yang paling mewakili sebatian ternary. Satu -satunya perbezaan yang disebutkan ialah perubahan Bear dan ICO Sufijos untuk ITO dan ATO, masing -masing. Juga, H digantikan dengan kation logam, produk peneutralan asid-asas.
Berlanjut dengan bromin, oxisals natriumnya ialah: Nabro, Nabro2, Nabro3 dan Nabro4. Nama mereka akan menjadi: Hipobromito, Bromito, Bromato dan Natrium Perbromate. Tanpa ragu, bilangan oxisal yang mungkin melebihi oxoacids.
Latihan
Sekali lagi, setiap jenis kompaun ternary mempunyai asal usul atau proses latihannya sendiri. Walau bagaimanapun, adalah wajar untuk menyebutkan bahawa ini hanya boleh dibentuk jika terdapat pertalian yang mencukupi antara tiga ahli atom. Sebagai contoh, pangkalan logam wujud terima kasih kepada interaksi elektrostatik antara kation dan oh-.
Boleh melayani anda: asid sitrikSesuatu yang serupa berlaku dengan asid, yang tidak dapat dibentuk jika tidak ada ikatan kovalen seperti itu A-O-H.
Berdasarkan soalan, bagaimana sebatian utama terbentuk? Jawapan langsung adalah seperti berikut:
- Pangkalan logam dibentuk dengan membubarkan oksida logam di dalam air, atau dalam larutan alkali (biasanya disediakan oleh NaOH atau ammonia).
- Oxoacids adalah produk pembubaran oksida bukan logam dalam air; Antara mereka, CO2, Clo2, Tidak2, SW3, P4Sama ada10, dan lain-lain.
- Dan kemudian, oxisals timbul apabila oxoacids diikat atau dinetralkan dengan asas logam; Dari itu datang kation logam yang supplace h+.
Sebatian ternary lain dibentuk berikutan proses yang lebih rumit, seperti aloi atau mineral tertentu.
Contoh
Akhirnya, satu siri formula untuk sebatian ternary yang berbeza akan ditunjukkan sebagai senarai:
- Mg (oh)2
- CR (oh)3
- Kmno4
- Na3Bo3
- CD (OH)2
- Abang3
- Feaso4
- Bacr2Sama ada7
- H2SW4
- H2Teo4
- Hcn
- AGOH
Contoh lain yang kurang biasa (dan juga hipotesis) adalah:
- Cofecu
- Algasn
- UCAPB
- Bemgo2
Subskrip N, M dan P telah ditinggalkan supaya tidak merumitkan formula; Walaupun pada hakikatnya, pekali stoikiometriknya (kecuali yang terbaik untuk Bemgo2), mungkin mempunyai nilai perpuluhan.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- PUAN. Hilfstein. (s.F.). Ternary Comununds. Pulih dari: tenafly.K12.NJ.kita
- Wikipedia. (2019). Ternary Comund. Diperoleh dari: dalam.Wikipedia.org
- Carmen Bello, Arantxa Isasi, Ana Puerto, Germán Tomás dan Ruth Vicente. (s.F.). Sebatian ternary. Pulih dari: iesdmjac.Educa.Aragon.adalah

