Struktur Kapsul Bowman, Histologi, Fungsi
- 1886
- 489
- Miss Elmer Hagenes
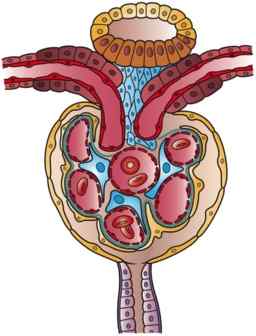
The Kapsul Bowman Ia mewakili segmen awal komponen tiub nefron, unit anátomo-fungsional buah pinggang di mana proses yang ditakdirkan untuk pengeluaran air kencing dijalankan dan dengan mana buah pinggang menyumbang kepada pemuliharaan homeostasis organisma.
Ia dinamakan sebagai penghormatan kepada pakar mata pakar ophthalmologist dan anatomi Sir William Bowman, yang menemui kewujudannya dan menerbitkan penerangan histologinya untuk kali pertama pada tahun 1842.
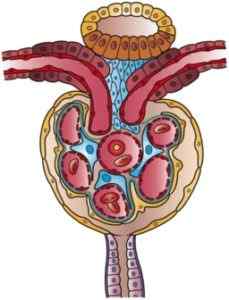 Ilustrasi Nephron (Sumber: Karya Seni oleh Holly Fischer [CC oleh 3.0 (https: // creativeCommons.Org/lesen/oleh/3.0)] melalui Wikimedia Commons)
Ilustrasi Nephron (Sumber: Karya Seni oleh Holly Fischer [CC oleh 3.0 (https: // creativeCommons.Org/lesen/oleh/3.0)] melalui Wikimedia Commons) Terdapat kekeliruan tertentu dalam kesusasteraan berhubung dengan tatanama segmen awal nefron, di antaranya kapsul Bowman dimasukkan. Kadang -kadang ia digambarkan sebagai bahagian yang berbeza dari glomerulus dan membentuknya dengan corpuscle buah pinggang, sementara bagi yang lain ia mempunyai fungsi sebagai ahli glomerulus.
Tidak kira hakikat bahawa dalam deskripsi anatomi kapsul adalah sebahagian daripada glomerulus, hakikatnya adalah bahawa kedua -dua elemen sangat dikaitkan dengan struktur dan fungsinya, bahawa istilah glomerulus membangkitkan dalam siapa yang menganggap idea spherit dengan ia kapal.
Jika tidak, kapsul hanya akan menjadi wadah di mana cecair ditapis ke dalam glomerulus dituangkan, tetapi ia tidak akan mempunyai bahagian dalam proses penapisan glomerular yang sama. Yang tidak begitu, kerana dia, seperti yang akan dilihat, adalah sebahagian daripada proses yang dia menyumbang dengan cara yang istimewa.
[TOC]
Struktur dan histologi
Kapsul Bowman adalah seperti sfera kecil yang dindingnya diserang dalam sektor vaskular. Dalam invagination ini, kapsul ditembusi oleh makanan ringan, yang berasal dari arteriola afferent dan yang membawa darah ke glomerulus, di mana arteriola eferen yang mengambil darah dari glomerulus juga keluar keluar.
Hujung bertentangan kapsul, yang dipanggil tiang kencing, dibentangkan seolah -olah dinding sfera mempunyai lubang yang akhir segmen pertama yang memulakan fungsi tiub itu sendiri, iaitu, tubulus kontur proksimal disambungkan.
Dinding luaran kapsul ini adalah epitelium rata dan dipanggil epitel parietal kapsul Bowman. Tukar struktur semasa membuat peralihan ke epitelium tubulus proksimal di tiang kencing dan ke arah epitel pendarahan di tiang vaskular.
Boleh melayani anda: papillae fungiformEpitelium yang dicabut dipanggil visceral kerana ia membungkus kapilari glomerular seolah -olah mereka adalah viscera. Ia dibentuk oleh sel -sel yang dipanggil podosit yang merangkumi, meliputi mereka, ke kapilari dan mempunyai ciri -ciri yang sangat khusus.
Podocytes dianjurkan dalam satu lapisan, memancarkan pemanjangan yang dihubungkan dengan sambungan podosit jiran, meninggalkan ruang di antara mereka yang dipanggil liang -liang di celah atau penapisan penapisan dan penyelesaian kesinambungan untuk langkah penapisan.
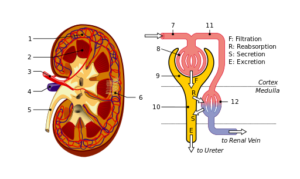 Struktur Ginjal dan Nephron: 1. Korteks buah pinggang; 2. Sumsum; 3. Arteri buah pinggang; 4. Urat buah pinggang; 5. Ureter; 6. Nefron; 7. Afferent Arteriola; 8. Glomerulus; 9. Kapsul Bowman; 10. Tubules dan Hanle lakukan; sebelas. Kapilari peritubular (sumber: fail: fisiologi_of_nephron.Svg: madhero88file: cickingsrurture_piom.SVG: Piotr Michał Jaworski; Piom dalam kerja-kerja Plderivative: Daniel Sachse (Antares42) [CC BY-SA 3.0 (https: // creativeCommons.Org/lesen/by-sa/3.0)] melalui Wikimedia Commons)
Struktur Ginjal dan Nephron: 1. Korteks buah pinggang; 2. Sumsum; 3. Arteri buah pinggang; 4. Urat buah pinggang; 5. Ureter; 6. Nefron; 7. Afferent Arteriola; 8. Glomerulus; 9. Kapsul Bowman; 10. Tubules dan Hanle lakukan; sebelas. Kapilari peritubular (sumber: fail: fisiologi_of_nephron.Svg: madhero88file: cickingsrurture_piom.SVG: Piotr Michał Jaworski; Piom dalam kerja-kerja Plderivative: Daniel Sachse (Antares42) [CC BY-SA 3.0 (https: // creativeCommons.Org/lesen/by-sa/3.0)] melalui Wikimedia Commons) Podocytes dan sel endothelial yang meliputi membran basal di mana mereka menyokong dan juga mempunyai penyelesaian kesinambungan untuk laluan air dan bahan. Sel endothelial adalah fenestradas dan juga membenarkan penapisan.
Jadi ketiga -tiga elemen ini: endothelium kapilari, membran basal dan epitelium visceral kapsul Bowman, membentuk halangan membran atau penapisan bersama.
Fungsi
Kapsul dikaitkan dengan proses penapisan glomerular. Di satu pihak, kerana ia adalah sebahagian daripada penutup epitel podosit yang mengelilingi kapilari glomerular. Ia juga menyumbang sintesis membran basal di mana epitel ini dan endothelium kapilari glomerular disokong.
Ketiga -tiga struktur ini: endothelium kapilari, membran basal dan epitelium visceral kapsul Bowman, membentuk halangan membran atau penapisan yang dibentuk, dan masing -masing mempunyai ciri -ciri kebolehtelapannya sendiri yang menyumbang kepada selektiviti global dari halangan itu.
Di samping itu, jumlah cecair yang menembusi ruang Bowman, bersama -sama dengan tahap ketegaran yang menentang dinding luaran kapsul, menentukan genesis tekanan intrakapsular yang membantu memodulasi tekanan penapisan yang berkesan dan untuk meningkatkan cecair di seluruh tubulus yang berkaitan.
Boleh melayani anda: periosteum: ciri, fungsi dan histologiPenentu magnitud penapisan glomerular
Pemboleh ubah yang mengumpul magnitud proses penapisan glomerular adalah jumlah penapisan glomerular yang dipanggil (VFG), yang merupakan jumlah cecair yang ditapis dalam semua glomeruli dalam unit masa. Purata nilai normalnya adalah kira -kira 125 ml/min atau 180 l/hari.
Besarnya pembolehubah ini ditentukan dari sudut pandang fizikal oleh dua faktor, iaitu pekali penapisan atau ultrafiltrasi (kf) dan tekanan penapisan yang berkesan (PEFF). Iaitu: vfg = kf x peff (Persamaan 1)
Koefisien penapisan (KF)
Koefisien penapisan (KF) adalah produk kekonduksian hidraulik (LP), yang mengukur kebolehtelapan air membran dalam ml/min per unit kawasan dan unit tekanan pelaksanaan, oleh kawasan permukaan (a) membran penapis, iaitu kf = lp x a (Persamaan 2).
Besarnya pekali penapisan menunjukkan jumlah cecair yang ditapis setiap unit masa dan per unit pemacu berkesan. Walaupun sangat sukar untuk diukur secara langsung, ia dapat diperolehi dari Persamaan 1, membahagikan VFG/PEFF.
KF dalam kapilari glomerular adalah 12.5 ml/min/mmHg per c/100g tisu, nilai kira -kira 400 kali lebih tinggi daripada KF sistem kapilari lain badan, di mana anda boleh menapis kira -kira 0.01 ml/min/mm hg setiap 100 g kain. Perbandingan menunjukkan kecekapan penapisan glomerular.
Tekanan penapisan yang berkesan (PEFF)
Tekanan penapisan yang berkesan mewakili hasil jumlah algebra dari daya tekanan yang berbeza yang memihak atau menentang penapisan. Terdapat kecerunan tekanan hidrostatik (ΔP) dan tekanan osmotik lain (oncotic, Δп) yang ditentukan oleh kehadiran protein dalam plasma.
Kecerunan tekanan hidrostatik adalah perbezaan tekanan antara bahagian dalam kapilari glomerular (PCG = 50 mm Hg) dan ruang kapsul Bowman (PCB = 12 mm Hg). Seperti yang dilihat, kecerunan ini diarahkan dari kapilari ke kapsul dan menggalakkan anjakan cecair dalam hal itu.
Boleh melayani anda: rangka apendikular: fungsi dan tulangKecerunan tekanan osmotik bergerak cecair lebih kecil ke tekanan osmotik yang lebih tinggi. Hanya zarah yang tidak menapis kesan ini. Protein tidak menyaring. Пcbnya adalah 0 dan di kapilari glomerular пcg ia adalah 20 mm hg. Kecerunan ini bergerak cecair dari kapsul ke kapilari.
Tekanan berkesan boleh dikira dengan menggunakan PEFF = ΔP-Δп; = (PCG-PCB)-(пCG-APB); = (50-12)-(20-0); = 38-20 = 18 mm Hg. Oleh itu, terdapat tekanan penapisan yang berkesan atau bersih kira -kira 18 mm Hg yang menentukan VFG kira -kira 125 ml/min.
Indeks penapisan (jika) bahan yang terdapat dalam plasma
Ini adalah penunjuk kemudahan (atau kesukaran) yang mana bahan yang terdapat di plasma dapat menyeberangi penghalang penapisan. Indeks diperolehi dengan membahagikan kepekatan bahan ke dalam penapisan (FX) antara kepekatannya dalam plasma (PX), iaitu: IFX = FX/ PX.
Julat nilai jika antara maksimum 1 untuk bahan -bahan yang ditapis secara bebas, dan 0 bagi mereka yang tidak menyaring apa -apa. Nilai pertengahan adalah untuk zarah dengan kesukaran pertengahan. Semakin dekat dengan 1 nilai, semakin baik penapisan. Lebih dekat dengan 0, lebih sukar untuk ditapis.
Salah satu faktor yang menentukan jika saiz zarah. Mereka yang mempunyai diameter kurang daripada 4 nm penapis secara bebas (jika = 1). Apabila saiz tumbuh dan mendekati albumin, Fe dikurangkan. Zarah saiz albumin, atau lebih besar, mempunyai 0 ifs 0.
Faktor lain yang membantu menentukan jika beban elektrik negatif pada permukaan molekul. Protein mempunyai banyak beban negatif, yang ditambah ke saiz mereka untuk menghalang filtrabilitas mereka. Sebabnya ialah liang -liang mempunyai caj negatif yang mengusir protein.
Rujukan
- Ganong WF: Fungsi Renal dan Micturition, IN Kajian Fisiologi Perubatan, Edisi ke -25. New York, McGraw-Hill Education, 2016.
- Guyton AC, Hall Ji: Sistem Urin, IN Buku teks fisiologi perubatan , Ed ke -13, AC Guyton, Je Hall (eds). Philadelphia, Elsevier Inc., 2016.
- Lang F, Kurtz A: Niere, IN Physiologie des Menschen Mite Pathophysiologie, 31 ed, RF Schmidt et al (eds). Heidelberg, Springer Medizin Verlag, 2010.
- Silbernagl S: Die Funkction der Nieren, IN Fisiologi, Ed 6; R Klinke et al (eds). Stuttgart, Georg Thieme Verlag, 2010.
- Stahl Rak et al: Niere Undoitende Harnwe, IN Klinche patofisiologi, 8th Ed, W Siegenthaler (ed). Stuttgart, Georg Thieme Verlag, 2001.
- « Apa itu sendi berserabut? Jenis dan ciri -ciri
- Baragonnosia Asal, Konsep, Ujian, Gangguan Berkaitan »

