Bahagian persamaan kimia dan contoh
- 2109
- 463
- Delbert Dare
The Persamaan Kimia Ini adalah perwakilan skematik beberapa ciri reaksi kimia. Ia juga boleh dikatakan bahawa persamaan kimia menerangkan perubahan yang dialami oleh bahan -bahan yang berbeza yang terlibat dalam reaksi.
Dalam persamaan kimia, formula dan simbol bahan -bahan penyertaan yang berbeza diletakkan, dengan jelas menunjukkan bilangan atom setiap elemen yang terdapat dalam sebatian, yang muncul sebagai subskrip dan tidak dapat diubah ketika mengimbangi persamaan.
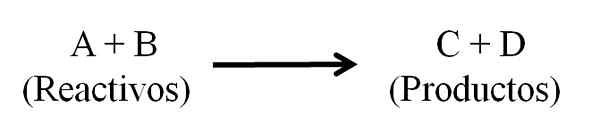
 Persamaan kimia umum untuk tindak balas kimia. Reagen dan produk. Sumber: Gabriel Bolívar.
Persamaan kimia umum untuk tindak balas kimia. Reagen dan produk. Sumber: Gabriel Bolívar. Persamaan kimia mesti kelihatan seimbang, iaitu bilangan atom kedua -dua reagen dan produk mestilah sama. Dengan cara ini undang -undang pemuliharaan bahan dipatuhi. Adalah wajar bahawa angka yang digunakan untuk mengimbangi persamaan adalah nombor keseluruhan.
Persamaan ini tidak mendedahkan langkah berturut -turut, atau mengapa reagen mekanisme berubah menjadi produk.
Itulah sebabnya walaupun mereka sangat berguna untuk memahami di mana tindak balas kimia sedang berlaku, ia tidak membenarkan untuk memahami aspek molekulnya atau bagaimana ia dipengaruhi oleh pembolehubah tertentu; seperti pH, kelikatan, masa tindak balas, kelajuan pergolakan, antara lain.
[TOC]
Bahagian persamaan kimia
Pada dasarnya terdapat tiga bahagian utama dalam persamaan kimia: reagen, produk dan anak panah yang menunjukkan makna reaksi kimia.
Lokasi reagen dan produk
Dalam persamaan kimia semua bahan yang berfungsi sebagai reagen dan semua produk yang muncul. Kumpulan bahan ini dipisahkan oleh anak panah yang menunjukkan makna reaksi. Reagen terletak di sebelah kiri anak panah dan produk di sebelah kanan.
Anak panah bermaksud apa yang dihasilkan dan berorientasikan dari kiri ke kanan (→), walaupun dalam reaksi yang boleh diterbalikkan terdapat dua anak panah yang setara dan selari; seseorang diarahkan ke kanan, dan yang lain ke kiri. Simbol (δ) biasanya diletakkan pada anak panah, menunjukkan bahawa haba digunakan dalam reaksi.
Boleh melayani anda: terpenosDi samping itu, pengenalan pemangkin biasanya diletakkan di atas anak panah, jika boleh dengan formula atau simbolnya. Bahan yang berbeza yang muncul sebagai reagen dipisahkan dengan tanda (+), menunjukkan bahawa bahan bertindak balas atau menggabungkan antara satu sama lain.
Dalam hal bahan yang muncul sebagai produk, tanda (+) tidak mempunyai konotasi sebelumnya; Kecuali reaksi itu boleh diterbalikkan. Adalah mudah bahawa tanda (+) diletakkan sama dari bahan yang memisahkan.
Keseimbangan persamaan kimia
Adalah keperluan penting bahawa persamaan kimia seimbang. Untuk ini, nombor yang dipanggil pekali stoikiometrik diletakkan. Bila perlu, pekali ini mesti pergi di hadapan bahan yang muncul sebagai reagen atau produk.
Ini adalah untuk memastikan bahawa bilangan semua atom unsur -unsur yang muncul sebagai reagen sama persis dengan bilangan mereka yang muncul dalam produk. Kaedah persamaan kimia yang paling mudah ialah Tanteo.
Keadaan fizikal komponen persamaan kimia
Dalam beberapa persamaan kimia, keadaan fizikal bahan ditunjukkan dengan sub -industri. Untuk ini, singkatan berikut digunakan dalam bahasa Sepanyol: (s) untuk keadaan pepejal; (l) untuk keadaan cecair; (g), keadaan gas; dan (ac), larutan akueus.
Contoh: Reaksi kalsium karbonat dengan asid hidroklorik.
Pencuri3 (s) + 2 HCl(Ac) → CACL2 (s) + H2Sama ada(L) + Co2 g)
Perubahan status fizikal
Dalam sesetengah kes, ia ditunjukkan dalam persamaan kimia jika terdapat pengeluaran gas dalam tindak balas kimia atau jika terdapat pemendakan mana -mana bahan yang dihasilkan.
Boleh melayani anda: garam binariKehadiran gas ditunjukkan dengan anak panah menegak dengan akhir yang diarahkan ke atas (↑), diletakkan di sebelah kanan bahan gas.
Contoh: Reaksi zink dengan asid hidroklorik.
Zn +2 HCl → ZnCl2 + H2↑
Jika dalam reaksi kimia salah satu bahan membentuk endapan, ini dilambangkan dengan meletakkan anak panah menegak dengan akhir yang diarahkan ke bawah (↓), diletakkan di sebelah kanan bahan yang dicetuskan.
Contoh: Reaksi asid hidroklorik dengan nitrat perak.
HCl + Agno3 → Hno3 + AGCL ↓
Contoh persamaan kimia
- Fotosintesis
 Persamaan fotosintesis
Persamaan fotosintesis Fotosintesis adalah proses yang mana tumbuhan menangkap dan mengubah tenaga cahaya, dari cahaya matahari, untuk menghasilkan tenaga yang diperlukan untuk hidup mereka. Photosynthesis dilakukan oleh organel yang tipikal sel tumbuhan yang disebut kloroplas.
Dalam membran kloroplas adalah tilacoids, tempat di mana klorofil dijumpai ke dan b, yang merupakan pigmen utama yang menangkap tenaga ringan.
Walaupun fotosintesis adalah proses yang kompleks, ia boleh dijangkau dalam persamaan kimia berikut:
6 co2 + 6 h2O → c6H12Sama ada6 + 6 o2↑ ΔGº = 2.870 kJ/mol
C6H12Sama ada6 Ia adalah formula glukosa, karbohidrat yang dimetabolisme untuk pengeluaran ATP; Kompaun yang merupakan takungan tenaga utama di kebanyakan makhluk hidup. Di samping itu, dari glukosa nadph dihasilkan, koenzim diperlukan untuk banyak reaksi.
- Pernafasan selular
Sel menggunakan oksigen untuk metabolisme pelbagai bahan yang terdapat dalam makanan yang ditelan. Sementara itu, ATP digunakan sebagai sumber tenaga aktiviti yang dijalankan oleh makhluk hidup, menghasilkan proses karbon dan air dioksida ini.
Boleh melayani anda: Aluminium acetate (AL (CH3COO) 3): Struktur, sifat, kegunaanJika glukosa digunakan sebagai model bahan yang dimetabolisme, pernafasan boleh dijangkau dengan persamaan kimia berikut:
C6H12Sama ada6 + 6 o2 → 6 co2 + 6 h2Sama ada
- Reaksi unsur biasa
Tindak balas penguraian
Sebatian atau sebatian memisahkan (n) yang membentuk atom -atomnya yang lain sebatian yang berbeza:
2 kclo3 (s) → 2 KCl(S) + 3 o2 g)
Tindak balas anjakan
Logam bertindak balas dengan sebatian menggantikan logam yang ada dalam hal ini:
Mg(S) + Cuso4 (ac) → Cu(S) + Mgso4 (ac)
Reaksi penghapusan
Dalam tindak balas jenis ini, bilangan atom atau kumpulan yang dilampirkan pada atom karbon:
Ch3-Ch2Br +NaOH → H2C = ch2 + H2O +NABR
Tindak balas penghidratan
Ia adalah tindak balas di mana sebatian menambah molekul air. Reaksi ini penting dalam penyediaan alkohol:
H2C = ch2 + H2O → h2C-ch2Oh
Tindak balas peneutralan
Pangkalan atau alkali bertindak balas dengan asid yang menghasilkan garam dan air:
HCl(Ac) + NaOH(Ac) → NaCl(Ac) + H2Sama ada(L)
Tindak balas sintesis
Dalam tindak balas jenis ini dua atau lebih bahan digabungkan untuk menyebabkan sebatian baru:
2 li(S) + Cl2 g) → 2 LiCl(S)
Reaksi anjakan berganda (metathesis)
Dalam tindak balas jenis ini terdapat pertukaran ion positif dan negatif untuk membentuk sebatian baru:
Agno3 (ac) + NaCl(Ac) → AGCL(S) + Abang3 (ac)
Rujukan
- Bunga, j. (2002). Kimia. Edisi 1adalah. Editorial Santillana
- Mathews, c. K., Van holde, k. Dan., Dan ahern, k. G. (2002). Biokimia. 3adalah Edisi. Editorial Pearson Addison Wesley
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Wikipedia. (2019). Persamaan Kimia. Diperoleh dari: dalam.Wikipedia.org
- Helmestine, Anne Marie, Ph.D. (20 September 2019). Apakah persamaan kimia? Pulih dari: Thoughtco.com
- « Konsep dan formula volum molar, pengiraan dan contoh
- Challenger Abyss Pembentukan Geologi, Lokasi, Ciri -ciri »

