Struktur, C7H16) struktur, sifat dan kegunaan
- 1587
- 235
- Donnie Ryan
Dia Heptano Ia adalah sebatian organik yang formula kimia adalah c7H16 dan terdiri daripada sembilan isomer struktur, yang paling terkenal adalah linear. Ia adalah hidrokarbon, khususnya alkana atau parafin, yang terletak di kebanyakan makmal kimia organik, sama ada pengajaran atau penyelidikan.
Tidak seperti pelarut parafinik lain, heptano mempunyai turun naik yang lebih rendah, yang menjadikan penggunaannya yang lebih selamat; Setiap kali tidak ada sumber haba yang mengelilingi wap anda dan ia berfungsi di dalam loceng pengekstrak. Meninggalkan mudah terbakarnya, ia adalah sebatian yang cukup lengai untuk berfungsi sebagai alat tindak balas organik.
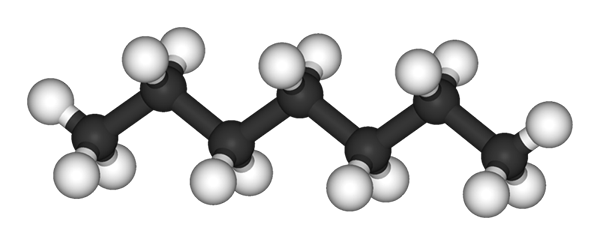
 Molekul N-Heptano yang diwakili oleh model sfera dan bar. Sumber: Ben Mills dan Jynto [Domain Awam]
Molekul N-Heptano yang diwakili oleh model sfera dan bar. Sumber: Ben Mills dan Jynto [Domain Awam] Di bahagian atas anda mempunyai struktur n-heptano, isomer linear dari semua heptans. Kerana ia adalah isomer yang paling biasa dan nilai komersial yang lebih besar, serta yang paling mudah untuk disintesis, ia cenderung pada akhirnya istilah 'heptano' merujuk secara eksklusif kepada n-Heptano; melainkan dinyatakan sebaliknya.
Walau bagaimanapun, dalam botol sebatian cecair ini ditentukan bahawa ia mengandungi n-Heptano. Mereka harus mendedahkan di dalam loceng pengekstrak dan melakukan pengukuran dengan teliti.
Ia adalah pelarut yang sangat baik untuk lemak dan minyak, jadi sering digunakan semasa esensi tumbuhan atau produk semula jadi lain.
[TOC]
Struktur
n-heptane dan interaksi intermolecularnya
Seperti yang dapat dilihat dalam imej pertama, molekul n-Heptano adalah linear, dan disebabkan oleh hibridisasi kimia atom karbonnya, rantai mengamalkan bentuk zigzagueada. Molekul ini dinamik, kerana ikatan C-Cnya boleh berputar, yang menjadikan rantai lipat sedikit pada sudut yang berbeza. Ini menyumbang kepada interaksi intermolecularnya.
Ia boleh melayani anda: pautan piDia n-Heptano adalah molekul apolar, hidrofobik, dan oleh itu interaksinya didasarkan pada daya dispersif London; Ini adalah, yang bergantung kepada jisim molekul sebatian dan kawasan hubungannya. Dua molekul n-Heptan.
Interaksi ini cukup berkesan untuk mengekalkan molekul n-Heptano bersatu dalam cecair yang mendidih pada 98 ºC.
Isomer
 Sembilan isomer heptan. Sumber: Steffen 962 [Domain Awam]
Sembilan isomer heptan. Sumber: Steffen 962 [Domain Awam] Pada mulanya dikatakan bahawa Formula C7H16 mewakili sembilan isomer struktur, sebagai n-heptane yang paling relevan (1). Lapan isomer yang lain ditunjukkan pada gambar atas. Perhatikan dengan mata kasar bahawa ada yang lebih bercabang daripada yang lain. Dari kiri ke kanan, bermula dari atas, kita ada:
(2): 2-methylhexan
(3): 3-methylhexan, yang terdiri daripada sepasang enantiomer (a dan b)
(4): 2,2-dimethylpentano, juga dikenali sebagai neoheptano
(5): 2,3-dimethylpentano, sekali lagi dengan sepasang enantiomer
(6): 2,4-dimethylpentano
(7): 3.3-dimethylpentano
(8): 3-etilpentane
(9): 2,2,3-trimethylbutane.
Setiap isomer ini mempunyai sifat bebas dan aplikasi n-heptano, terpelihara lebih daripada apa -apa untuk kawasan sintesis organik.
Hepthane Properties
Penampilan fizikal
Cecair tanpa warna dengan bau yang serupa dengan petrol.
Jisim molar
100,205 g/mol
Takat lebur
-90,549 ºC, menjadi kristal molekul.
Takat didih
98.38 ºC.
Tekanan wap
52.60 atm pada 20 ºC. Perhatikan betapa tinggi tekanan wap anda, walaupun kurang tidak menentu daripada pelarut parafinik lain, seperti Hexano dan Pentan.
Ketumpatan
0.6795 g/cm3. Sebaliknya, wap heptano adalah 3.45 kali padat daripada udara, yang bermaksud bahawa wap mereka akan bertahan di ruang di mana sedikit tumpahan cecair mereka.
Boleh melayani anda: asid formik (HCOOH)Kelarutan air
Heptane untuk menjadi sebatian hidrofobik hampir tidak dapat dibubarkan di dalam air untuk menyebabkan penyelesaian dengan kepekatan 0.0003% pada suhu 20 ºC.
Kelarutan dalam pelarut lain
Hepthane boleh didapati dengan karbon tetraklorida, etanol, aseton, eter minyak dan kloroform.
Indeks refraktif (nD)
1,3855.
Goo
0.389 mpa · s
Kapasiti haba
224.64 J/K · mol
titik pencucuhan
-4 ºC
Suhu sendiri
223 ºC
Ketegangan permukaan
19.66 mn/m A 25 ºC
Haba pembakaran
4817 kJ/mol.
Reaktiviti
Hepthane wap apabila mereka dekat dengan sumber haba (api), bertindak balas dengan eksotermik dan bersungguh -sungguh dengan oksigen udara:
C7H16 + 11o2 => 7co2 + 8h2Sama ada
Walau bagaimanapun, di luar tindak balas pembakaran, heptane adalah cecair yang agak stabil. Kekurangan kereaktifannya adalah disebabkan oleh fakta bahawa pautan C-H mereka sukar untuk dipecahkan, jadi tidak terdedah kepada penggantian. Ia juga tidak begitu sensitif terhadap ejen pengoksidaan yang kuat, dengan syarat tidak ada api di sekitar.
Bahaya terbesar Heptano diwakili oleh turun naik dan kemerosotan yang tinggi, jadi ada risiko kebakaran jika ia tumpah di tapak panas.
Aplikasi
Pelarut dan separuh tindak balas
 Hepthane adalah pelarut yang sangat baik untuk membubarkan minyak dan lemak. Sumber: Pxhere.
Hepthane adalah pelarut yang sangat baik untuk membubarkan minyak dan lemak. Sumber: Pxhere. Karakter hidrofobik heptano adalah pelarut yang sangat baik untuk membubarkan minyak dan lemak. Dalam aspek ini ia telah digunakan sebagai degreaser. Walau bagaimanapun, aplikasi terbesarnya terletak pada digunakan sebagai pelarut pengekstrak, kerana ia membubarkan komponen lipid, serta sebatian organik lain dari sampel.
Sebagai contoh, jika anda ingin mengekstrak semua komponen kopi tanah, ia akan menjadi macerated dalam heptane dan bukannya air. Kaedah ini dan variasinya telah dilaksanakan dengan semua jenis benih, terima kasih kepada mana -mana esensi tumbuhan dan produk semula jadi yang lain telah diperolehi.
Ia boleh melayani anda: sel kesatuan: sifat, pemalar merah dan jenisHeptane, yang secara semula jadi tidak berwarna, akan dicelup dari warna minyak yang diekstrak. Kemudian, ini diputar untuk akhirnya mempunyai jumlah minyak yang murni.
Sebaliknya, kereaktifan sedikit heptane juga membolehkan anda menjadi pilihan apabila mempertimbangkan cara reaksi untuk menjalankan sintesis. Menjadi pelarut yang baik dari sebatian organik, ia menjamin bahawa reagen tetap dalam penyelesaian dan berinteraksi antara satu sama lain kerana mereka bertindak balas.
Ejen Precipitating
Dalam kimia minyak, ia adalah amalan biasa untuk mendakan asfalten sampel mentah dengan menambahkan heptano. Kaedah ini membolehkan mengkaji kestabilan mentah yang berbeza dan menentukan bagaimana kandungan asphaltene yang terdedah adalah untuk mendakan dan membawa siri masalah untuk industri minyak.
Octane
Heptan telah digunakan sebagai bahan bakar kerana sejumlah besar haba yang ditawarkan apabila ia terbakar. Walau bagaimanapun, berkenaan dengan enjin kereta, ia akan memudaratkan operasinya jika ia akan digunakan semata -mata. Kerana ia terbakar dengan sangat meletup, ia berfungsi untuk menentukan 0 pada skala petrol oktana.
Petrol mengandungi peratusan tinggi heptano dan hidrokarbon lain ke tahap oktana kepada nilai yang diketahui (91, 95, 87, 89, dll.).
Rujukan
- Morrison, r. T. dan Boyd, R, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2020). Heptane. Diperoleh dari: dalam.Wikipedia.org
- Pusat Kebangsaan Maklumat Bioteknologi. (2020). Pangkalan Data Pubchem Heptane. CID = 8900. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Elsevier b.V. (2020). Heptans. Scientedirect. Diperoleh dari: Scientedirect.com
- Bell Chem Corp. (7 September 2018). Penggunaan Perindustrian Heptane. Pulih dari: Bellchem.com
- Andrea Kropp. (2020). Heptane: Struktur, Kegunaan & Formula. Kajian. Pulih dari: belajar.com
- « Formula Pondensed Apakah dan contoh (metana, etana, glukosa ...)
- Formula tenaga mekanikal, konsep, jenis, contoh, latihan »

