Hidrokarbon tak tepu
- 3836
- 1213
- Miss Elmer Hagenes
Kami menerangkan apa hidrokarbon tak tepu, klasifikasi, sifat, tatanama dan memberi beberapa contoh
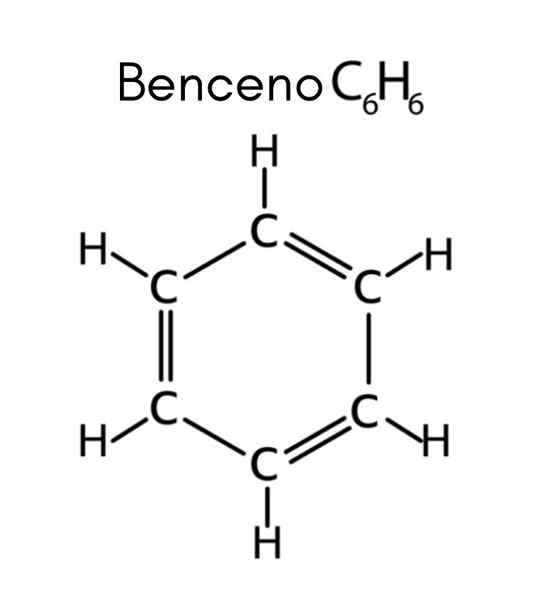
 Benzena adalah contoh hidrokarbon tak tepu
Benzena adalah contoh hidrokarbon tak tepu Apakah hidrokarbon tak tepu?
The hidrokarbon tak tepu Mereka adalah sebatian organik yang dibentuk hanya oleh karbon dan hidrogen, yang mempunyai satu atau lebih banyak ikatan antara atom karbon. Ini bermaksud bahawa sebatian formula cxHdan yang membentangkan ikatan berganda atau tiga adalah hidrokarbon tak tepu.
Hidrokarbon tak tepu dibentuk oleh alkena dan alkina, serta sebatian aromatik. Sebab mengapa mereka tidak tepu adalah kerana mereka mempunyai bilangan hidrogen yang lebih kecil daripada maksimum yang mereka dapat, memandangkan bilangan atom karbon dalam struktur.
Hidrokarbon tak tepu diiktiraf dengan mempunyai kurang daripada 2n+2 hidrogen (yang merupakan bilangan maksimum hidrogen yang boleh menjadi karbon), di mana n adalah bilangan atom karbon dalam formula molekul.
Contoh hidrokarbon tak tepu adalah buteno, yang formula molekulnya adalah c4H8. Jumlah maksimum hidrogen untuk 4 karbon akan 2 (4) +2 = 10 Hidrogen. Ini sepadan dengan bilangan hidrogen hidrokarbon tepu. Oleh kerana buteno hanya mempunyai 8 hidrogen, yang kurang dari 10, maka ia adalah hidrokarbon tak tepu.
Bilangan ketidakpastian
Hidrokarbon tak tepu dicirikan oleh bilangan ketidakpastian. Ini menunjukkan bilangan pasangan hidrogen kurang daripada hidrokarbon tak tepu dibandingkan dengan yang tepu yang mempunyai bilangan karbon yang sama.
Bilangan tidak tepu boleh dikira untuk mana -mana sebatian tak tepu melalui formula berikut:
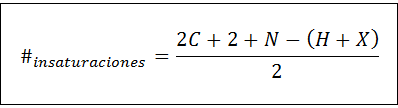
Di mana C, N, H dan X mewakili bilangan karbon, nitrogen, hidrogen dan halogen dalam formula molekul, masing -masing. Nombor ini memberi kita idea tentang berapa banyak beregu atau ikatan tiga mempunyai sebatian, memandangkan formula molekulnya, walaupun penjagaan mesti diambil kerana kitaran (yang tidak tidak tepu) juga menyumbang kepada bilangan ketidakpastian:

Contoh
Benzena mempunyai formula c6H6, Jadi bilangan tidak tepu adalah:
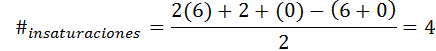
Dalam kes ini, 4 ketidakpatuhan sesuai dengan tiga pautan ganda dan kitaran.
Klasifikasi hidrokarbon tak tepu
Menurut jenis hidrokarbon
- Alkenes: Mereka adalah mereka yang mempunyai sekurang -kurangnya satu pautan berganda dalam struktur mereka.
- Alkynes: Mereka adalah mereka yang mempunyai sekurang -kurangnya satu pautan tiga dalam struktur mereka.
- Aromatik: Mereka adalah sebatian tak tepu polyunsatur dengan sifat khas yang menjadikannya sangat stabil.
Menurut rantai karbon
- Linear: sebatian tak tepu di mana semua atom karbon dikaitkan antara satu sama lain dalam satu rantai.
- RAMIFIED: Mereka adalah mereka yang mempunyai rantai utama dan juga beberapa rantai sisi yang membentuk ramuan.
- Siklik: Mereka adalah di mana kitaran tertutup atom karbon dibentangkan di mana sekurang -kurangnya satu ikatan dua atau tiga dibentangkan (sikloalquenos, sikloalquinos dan aromatik).
Menurut bilangan ketidakpastian
- Monounsaturated: Apabila mereka hanya mempunyai pautan berganda, iaitu, ia adalah satu ikatan berganda atau satu pautan triple tunggal.
- Polynsaturated: Apabila struktur mempunyai lebih daripada satu pautan berganda, seperti dalam kes alkian, alkian, alkenin, dll.
Sifat hidrokarbon tak tepu
Sifat hidrokarbon tak tepu sangat bergantung pada jenis hidrokarbon tertentu yang dipersoalkan:
Titik gabungan dan mendidih
Secara umum, hidrokarbon tak tepu mempunyai titik gabungan dan mendidih yang rendah. Walau bagaimanapun, berbanding dengan alkana, alkena dengan bilangan karbon yang sama dan rantaian utama yang sama biasanya mempunyai titik mendidih yang lebih rendah, sementara alkines cenderung mempunyai titik mendidih yang lebih besar.
Perkara yang sama berlaku untuk titik gabungan. Dalam jadual berikut, dapat dilihat bahawa kedua-dua titik gabungan dan mendidih 1-pentene lebih rendah daripada Pentan dan ini yang dari 1-pentino.

Keadaan fizikal
Oleh kerana titik lebur dan mendidih yang rendah, hidrokarbon berat badan molekul rendah yang tidak tepu cenderung menjadi gas pada suhu bilik. Ramai juga cair dan berat molekul yang lebih besar adalah pepejal. Dalam banyak kes, pepejal adalah pepejal amorf dan bukannya kristal.
Polariti
Semua hidrokarbon, termasuk tak tepu, adalah sebatian apolar, kerana elektronegativiti karbon dan hidrogen sangat serupa. Satu -satunya pengecualian adalah dalam hal Alkin Terminal2 dan sp3.
Kelarutan
Menjadi apolar, hidrokarbon tak tepu tidak larut dalam air dan pelarut kutub yang lain, tetapi mereka sangat larut dalam pelarut apolar seperti karbon tetraklorida, sikloheksan dan lain -lain. Sebenarnya, banyak sebatian ini, dalam diri mereka, pelarut apolar.
Ia boleh melayani anda: disposio: struktur, sifat, mendapatkan, menggunakanMereka adalah bahan api
Ciri -ciri semua hidrokarbon, termasuk tak tepu, adalah bahawa mereka membakar dengan kehadiran oksigen untuk menjadi karbon dioksida dan air melepaskan tenaga dalam bentuk cahaya dan panas.
Mereka boleh polimerisasi
Melalui tindak balas kimia yang berbeza, alkena dan alkina boleh bergabung satu sama lain untuk membentuk polimer seperti dalam hal polietilena dan polipropilena, untuk menyebut hanya beberapa. Jadi hidrokarbon tak tepu adalah bahan permulaan banyak plastik biasa.
Kereaktifan kimia
Kereaktifan sangat bergantung pada jenis kumpulan berfungsi yang mempunyai molekul. Dalam kes alkena dan alkina, ini biasanya agak reaktif dan boleh mengalami reaksi penghidrogenan, penghidratan, hidrohalogenasi dan lain -lain jenis tindak balas tambahan.
Sebaliknya, sebatian aromatik biasanya agak tidak aktif kerana mereka sangat stabil. Reaksi ciri -ciri sebatian ini adalah tindak balas penggantian elektrofilik aromatik.
Nomenclature hidrokarbon tak tepu
Nomenklatur Alkenes
Linear Alkenes
Nama alkenes linear dibina dengan meletakkan awalan yang menunjukkan bilangan atom karbon dalam rantai, diikuti oleh pencari karbon di mana ikatan berganda berasingan bermula dengan skrip dari seluruh nama dan selesai dengan akhiran _eno:
Awalan-localizer
- Contoh:
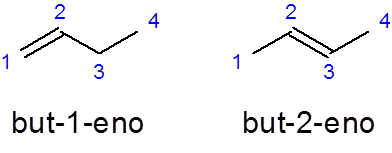
Dia Tetapi -1 -no Ia adalah nama butene linear dengan ikatan berganda dalam karbon pertama semasa Tetapi-2-sembilan Ia mempunyai ikatan berganda dalam karbon kedua.
Alkenes bercabang
Dalam kes alkenes bercabang, rantaian utama terpanjang yang mengandungi kedua -dua karbon ikatan berganda pertama kali dipilih dan keutamaan kepada ikatan berganda adalah bernombor. Nama ini dibina terlebih dahulu dengan meletakkan ramuan dalam susunan abjad yang didahului oleh pencari diikuti dengan nama rantai utama seperti yang ditunjukkan di atas.
- Contoh:
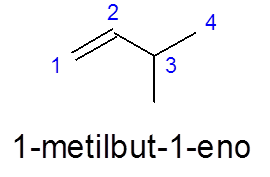
Dalam 3-methylbut-1 -en, penomboran dilakukan dari kiri ke kanan untuk memberi keutamaan kepada ikatan berganda, dan bukannya memberi keutamaan kepada cawangan (kumpulan metil).
Polene
Dalam kes alkena polyunsaturated atau polienous, yang mengandungi lebih daripada satu ikatan berganda, bilangan bon dua yang terbesar dipilih sebagai rantaian utama, tanpa mengira sama ada terdapat rantai yang lebih panjang.
Dalam nama rantaian utama pencari ditambah untuk setiap ikatan ganda dan awalan di, tri, tetra, dll. Sebelum penamatan -eno, untuk menunjukkan bilangan pautan berganda yang anda ada.
- Contoh:
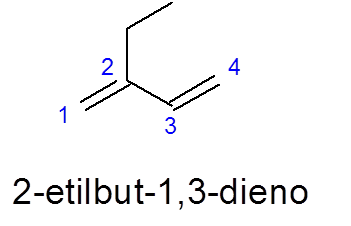
Perhatikan dalam kes ini bahawa walaupun pada hakikatnya terdapat rantai 5 -karbon yang lebih lama, 4 dari 4 dipilih, kerana ia mengandungi dua pautan ganda.
Nomenklatur Alquinos
Alkynes dinamakan sangat mirip dengan alkenes, dengan satu -satunya perbezaan nama yang berakhir di -ino bukannya -eno. Dalam kes -kes di mana terdapat lebih daripada satu pautan tiga, pencari semuanya diletakkan dan awalan berangka yang menunjukkan berapa banyak yang ada.
- Contoh:
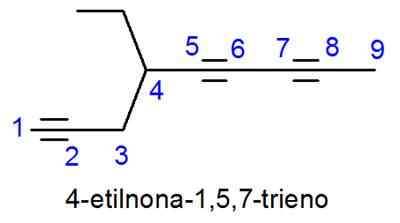
Nomenklatur sebatian aromatik
Hidrokarbon aromatik dilantik sebagai derivatif benzena dan kedua -dua penomboran dan cara menamakannya bergantung kepada berapa banyak substituen cincin yang ada.
Cincin aromatik dengan substituen tunggal
Dalam kes ini tidak perlu. Nama itu terdiri daripada nama cawangan yang diikuti dengan perkataan benzena.
- Contoh:
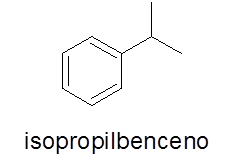
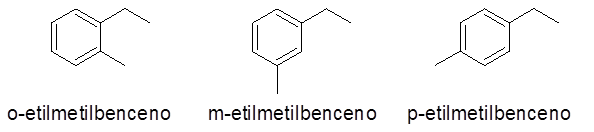
Cincin aromatik dengan dua substituen
Dalam kes ini, 3 nombor atau corak penggantian boleh diberikan (1.2), (1.3) dan (1,4). Kerana tidak peduli untuk menunjukkan pengganti mana yang ada dalam karbon 1 dan yang lain, ortho awalan (o-), meta- (m-) dan para- (p-), masing-masing, untuk merujuk kepada yang sama.
- Contoh:
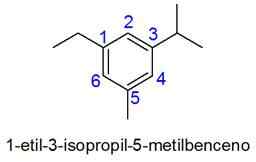
Cincin aromatik dengan lebih daripada 2 substituen
Dalam kes ini, penomboran kombinasi terkecil locator dipilih. Sekiranya dua nombor adalah sama, keutamaan diberikan kepada substituen mengikut urutan abjad.
- Contoh:
Contoh hidrokarbon tak tepu
Seterusnya, contoh tambahan hidrokarbon tak tepu dibentangkan kepada yang sudah disebutkan.
Acetylene (c2H2)
Acetylene adalah nama biasa etino, alkimia yang paling mudah. Kompaun ini mempunyai 2 ketidakpastian kerana pautan tiga dan digunakan, antara lain, dalam peralatan keluli dan kimpalan.
Cyclohexen (c6H10)
6 -Alkene kitaran karbon yang mempunyai dua ketidakpastian: satu disebabkan oleh kitaran dan yang lain kerana ikatan berganda.
Regangan (c8H8)
Kompaun ini biasanya digunakan dalam penyediaan polimer. Ia adalah alkena aromatik dengan 5 ketidakpastian.

