Hydroxiapatite

- 4873
- 832
- Dallas Bernhard
Kami menerangkan apa yang hydroxylapatite, strukturnya, bagaimana ia disintesis, kegunaannya dan sifat fizikal dan kimia
 Hydroxiapatite. Sumber: Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0, CC BY-SA 3.0, melalui Wikimedia Commons
Hydroxiapatite. Sumber: Rob Lavinsky, Irocks.COM-CC-BY-SA-3.0, CC BY-SA 3.0, melalui Wikimedia Commons Apa itu hydroxyapatite?
The Hydroxiapatite Ia adalah mineral kalsium fosfat, yang formula kimianya adalah ca10(PO4)6(Oh)2. Bersama -sama dengan mineral lain dan bahan organik organik dan dipadatkan, ia membentuk bahan mentah yang dikenali sebagai batu fosforik. Istilah hidroksi merujuk kepada anion oh-.
Sekiranya anion itu fluorida, mineral akan dipanggil fluoroapatita (CA10(PO4)6(F)2; Dan sebagainya dengan anion lain (cl-, Br-, Co32-, dan lain-lain.). Begitu juga, hydroxyapatite adalah komponen tak organik utama tulang dan enamel pergigian, yang kebanyakannya hadir dalam kristal.
Oleh itu, ia adalah elemen penting dalam tisu tulang makhluk hidup. Kestabilannya yang hebat terhadap fosfat kalsium yang lain membolehkannya menyokong keadaan fisiologi, memberikan tulang kekerasan ciri mereka. Hydroxiapatite tidak bersendirian: ia memenuhi fungsinya disertai oleh kolagen, protein berserabut tisu konjunktif.
Hydroxyapatite (atau hydroxylapatite) mengandungi ion ca2+, Tetapi kation lain juga boleh menempatkan strukturnya (mg2+, Na+), kekotoran yang terlibat dalam proses biokimia lain tulang (seperti pembentukan semula mereka).
Struktur Hydroxyapatite
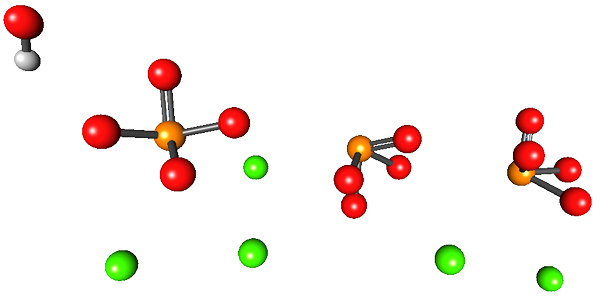
Imej unggul menggambarkan struktur kalsium hydroxyapatite. Semua sfera menduduki jumlah separuh daripada "laci" heksagon, di mana separuh lagi sama dengan yang pertama.
Dalam struktur ini, sfera hijau sesuai dengan kation CA2+, Walaupun sfera merah ke atom oksigen, oren ke atom fosforus, dan putih ke atom hidrogen OH-.
Ion fosfat dalam imej ini mempunyai kecacatan tidak memaparkan geometri tetrahedral; Sebaliknya, mereka kelihatan seperti piramid asas persegi.
Boleh melayani anda: keadaan vitreousOh- memberi gambaran bahawa ia terletak jauh dari CA2+. Walau bagaimanapun, unit kristal dapat mengulangi sendiri di atas bumbung yang pertama, dengan itu menunjukkan kedekatan yang dekat antara kedua -dua ion. Juga, ion ini boleh digantikan oleh orang lain (na+ dan f-, Sebagai contoh).
Sintesis Hydroxylapatite
Hydroxylapatite boleh disintesis dengan tindak balas kalsium hidroksida dengan asid fosforik:
10 CA (OH)2 + 6 h3PO4 => Ca10(PO4)6(Oh)2 + 18 h2Sama ada
Hydroxiapatita (ca10(PO4)6(Oh)2) dinyatakan oleh dua unit formula CA5(PO4)3Oh.
Begitu juga, hydroxyapatite boleh disintesis melalui reaksi berikut:
10 CA (Tidak3)2.4H2O + 6 nh4H2PO4 => Ca10(PO4)6(Oh)2 + 20 nh4Tidak3 + 52 h2Sama ada
Kawal kelajuan hujan membolehkan tindak balas ini menghasilkan nanopartikel hidroksiapatite.
Kristal Hydroxyapatite

Ion dipadatkan dan tumbuh untuk membentuk bio -kritikal yang tegar dan tahan. Ini digunakan sebagai biomaterial mineralisasi tulang.
Walau bagaimanapun, ia memerlukan kolagen, sokongan organik yang berfungsi sebagai acuan pertumbuhannya. Kristal ini dan proses pembentukan rumit mereka bergantung kepada tulang (atau gigi).
Kristal ini tumbuh diresapi dengan bahan organik, dan penggunaan teknik mikroskopi elektronik memperincikan mereka dalam gigi sebagai agregat dengan bentuk rod yang disebut prisma.
Kegunaan hydroxylapatite
Penggunaan Perubatan dan Pergigian
Oleh kerana persamaannya dalam saiz, kristalografi dan komposisi dengan tisu manusia yang keras, nanohydroxyapatite menarik untuk digunakan dalam prostesis. Juga, nanohydroxyapatite adalah biokompatibel, bioaktif dan semula jadi, selain tidak menjadi toksik atau keradangan.
Akibatnya, seramik nanohydroxyapatite mempunyai pelbagai aplikasi, termasuk:
- Dalam pembedahan tulang Tejido ia digunakan dalam pengisian rongga dalam pembedahan ortopedik, traumatologi, maxillofacial dan pergigian.
- Ia digunakan sebagai salutan implan ortopedik dan gigi. Ia adalah ejen desensitizing yang digunakan untuk pemutihan pergigian. Dia juga digunakan sebagai ejen remineralizing dalam pasta pergigian dan rawatan karies awal.
- Implan keluli tahan karat dan titanium sering ditutup dengan hidroksiapatit untuk mengurangkan kelajuan penolakan mereka.
- Ini adalah alternatif kepada tulang alogenik dan xenogenik tulang. Masa penyembuhan lebih pendek dengan kehadiran hydroxyapatite daripada ketiadaannya.
- Nanohidroxyapatite sintetik mimetiza ke hydroxyapatite hadir secara semulajadi dalam dentin dan apatite enmaltic, jadi penggunaannya dalam pembaikan enamel dan penggabungan dalam pasta pergigian adalah berfaedah, serta dalam mulut.
Penggunaan hidroksiapatit lain
- Hydroxyapatite digunakan dalam penapis udara kenderaan bermotor untuk meningkatkan kecekapan mereka dalam penyerapan dan penguraian karbon monoksida (CO). Ini mengurangkan pencemaran alam sekitar.
- Kompleks alginat-hydroxyapatite telah disintesis bahawa ujian medan telah menunjukkan bahawa ia dapat menyerap fluorida melalui mekanisme pertukaran ion.
- Hydroxiapathite digunakan sebagai medium kromatografi untuk protein. Ini mempunyai caj positif (ca++) dan negatif (po4-3), jadi ia boleh berinteraksi dengan protein yang dikenakan elektrik dan membenarkan pemisahannya dengan pertukaran ion.
- Hydroxyapatite juga telah digunakan sebagai sokongan untuk asid nukleik elektrofotik. Adalah mungkin untuk memisahkan DNA dari RNA, serta DNA helai mudah dari dua helai DNA.
Sifat fizikal dan kimia
Hydroxyapatite adalah pepejal putih yang dapat memperoleh nada kelabu, kuning dan kehijauan. Seperti pepejal kristal, ia memberikan titik gabungan yang tinggi, menunjukkan interaksi elektrostatik yang kuat; Untuk hydroxyapatite, ini adalah 1100 ºC.
Ia lebih padat daripada air, dengan ketumpatan 3.05 - 3.15 g/cm3. Di samping itu, ia hampir tidak larut dalam air (0.3 mg/ml), yang disebabkan oleh ion fosfat.
Walau bagaimanapun, dalam media berasid (seperti dalam HCl) ia larut. Kelarutan ini disebabkan oleh pembentukan CACL2, Garam air yang sangat larut. Begitu juga, fosfat adalah proton (HPO42- dan h2PO4-) dan berinteraksi dengan tahap yang lebih baik dengan air.
Kelarutan hydroxyapatite berasid adalah penting dalam patofisiologi karies. Bakteria di rongga mulut merembeskan asid laktik, produk penapaian glukosa, yang mengurangkan pH permukaan pergigian hingga kurang daripada 5, jadi hidroksiapatite mula larut.
Boleh melayani anda: sublimasi: konsep, proses dan contohFluorida (f-) Anda boleh menggantikan ion oh- Dalam struktur kristal. Apabila ini berlaku, ia memberikan ketahanan terhadap hidroksiapatit enamel pergigian di hadapan asid.
Mungkin, rintangan ini mungkin disebabkan oleh ketidaksuburan kafe2 terbentuk, enggan "meninggalkan" kaca.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Keempat ed., p. 349, 627). MC Graw Hill.
- Fluidinova. (2017). Hydroxylapatite. Diperolehi daripada Fluidinova.com
- Gaiabulbanix. (5 November 2015). Hydroxyapatite. [Rajah]. Pulih dari Commons.Wikimedia.org
- Martin.Neitsov. (25 November 2015). Hüdroksüapatiidi Kristallid. [Rajah]. Pulih dari Commons.Wikimedia.org
- Wikipedia. (2018). Hydroxylapatite. Diambil dari.Wikipedia.org
- Fiona Petchey. Tulang. C14dating pulih.com

