Pengionan dalam konsep, proses dan contoh fizik dan kimia

- 2997
- 545
- Anthony Breitenberg
The pengionan Ini semua proses di mana beban elektrik dihasilkan dari zarah neutral. Ini boleh berlaku melalui pelbagai mekanisme semula jadi atau daya, sama ada dengan radiasi, haba, medan elektrik, medan magnet atau tindak balas kimia. Ion dihasilkan sebagai akibat, yang secara positif atau atom yang dimuatkan secara negatif.
Pengionan adalah proses asas untuk simfin fenomena fizikal, kimia atau semulajadi, yang terakhir adalah banyak campuran perubahan fizikokimia. Sebagai contoh, dalam pengionan fizikal, pada dasarnya, tindak balas kimia tidak berlaku; Iaitu, pengeluaran ion tidak membayangkan kerosakan atau pembentukan pautan baru.
 Banyak fenomena semulajadi, seperti lampu utara, berdasarkan pengionan molekul atmosfera. Sumber: Pixabay.
Banyak fenomena semulajadi, seperti lampu utara, berdasarkan pengionan molekul atmosfera. Sumber: Pixabay. Walau bagaimanapun, dalam fenomena semulajadi pengionan ini biasanya disertai dengan tindak balas kimia, seperti pembentukan ozon di ketinggian rendah. Juga, semasa ribut petir nitrogen oksida dihasilkan kerana sinar dan suhu sengit mereka, yang mengoksidakan nitrogen udara.
Sebaliknya, pengionan dapat menyelinap: di dalam air yang sama, dalam menggosok antara dua permukaan, dalam pengoksidaan logam atau dalam pembubaran gas tertentu di dalam air.
[TOC]
Pengionan Kimia
Pengurangan pengoksidaan
 Semasa operasi bateri mainan, ion dan elektron terus. Sumber: D J SHIN/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/3.0)
Semasa operasi bateri mainan, ion dan elektron terus. Sumber: D J SHIN/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/3.0) Dalam pengionan kimia, ion dihasilkan oleh pemecahan atau pembentukan pautan. Dua bahan memperoleh atau kehilangan elektron secara tidak langsung: yang kehilangan elektron memperoleh beban positif, sementara yang menang mengekalkan beban negatif.
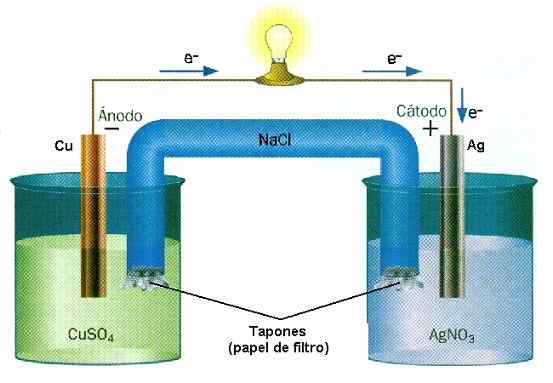
 Contoh pengurangan tindak balas oksida dalam tumpukan Cu-Ag. Sumber: Water Wall/CC By-SA (http: // creativeCommons.Org/lesen/by-sa/3.0/)
Contoh pengurangan tindak balas oksida dalam tumpukan Cu-Ag. Sumber: Water Wall/CC By-SA (http: // creativeCommons.Org/lesen/by-sa/3.0/) Di bateri, bahan kehilangan elektron sementara yang lain memenanginya. Elektron ini bergerak dan mengaktifkan litar elektrik peralatan, akhirnya kembali ke petak tumpukan kedua, di mana bahan lain menanti mereka untuk menangkap mereka dan memuatkan negatif. Ini adalah contoh pengionan kimia yang dijalankan oleh tindak balas pengurangan oksida.
Boleh melayani anda: asid glukonik: struktur, sifat, sintesis, kegunaanPecah heterolytic
Satu lagi jenis pengionan kimia adalah disebabkan oleh pecah heterolitik. Apabila rehat ini berlaku, pautan A-B dipecahkan untuk membentuk ion ke+ dan b-, Kerana elektron diarahkan ke arah atom yang mereka "merasakan" pertalian yang lebih besar. Pecah heterolitik biasanya merupakan langkah pertama yang mengawal mekanisme banyak reaksi organik.
Selfionisasi
Beban elektrik bukan sahaja dapat muncul oleh pergerakan elektron itu sendiri, tetapi oleh pautan yang rosak atau terbentuk dalam pertukaran atom. Inilah kes -kes, yang berlaku di antara dua molekul sebatian yang sama.
Dari semua pengionan kimia, penyebaran diri adalah yang paling mudah dan paling tidak dapat dilihat, kerana ia tidak mempunyai keupayaan untuk menjalankan arus elektrik dengan sendirinya.
Pengionan dalam Fizik
Elektrik statik
 Rambut gadis ini mengenakan positif dan menangkis satu sama lain kerana elektrik statik. Sumber: Biseup Ganguly/CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0)
Rambut gadis ini mengenakan positif dan menangkis satu sama lain kerana elektrik statik. Sumber: Biseup Ganguly/CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0) Pengionan juga mempunyai banyak penyertaan dalam fenomena fizikal. Secara umum, pengionan fizik tidak menyiratkan tindak balas kimia. Atom -atom bahan dikenakan elektrik tanpa kehilangan identiti asalnya.
Permukaan boleh bertukar elektron apabila mereka menggosok jika salah satu daripada mereka lebih berkesan dalam menyimpannya, yang membawa kepada elektrik statik. Tidak lagi bercakap tentang atom, tetapi bahan keseluruhan yang memperoleh beban negatif atau positif, dan apabila baki dipulihkan, kejutan elektrik secara literal dapat menghasilkan antara dua bahan atau badan.
Pengionan gas
Atom gas yang tersebar boleh kehilangan elektron jika mereka tertakluk kepada medan elektrik. Dengan berbuat demikian, atom -atom teruja dan dikeluarkan elektron. Kemudian, ketika menyejukkan dan kembali ke status mereka sebagai tenaga kecil, foton mengucapkan selamat tinggal. Dan prosesnya diulang lagi dan lagi. Hasilnya: sumber pencahayaan atau elektrik.
Boleh melayani anda: Boron Oxide (B2O3): Apa, Struktur, Hartanah, KegunaanRadiasi atau perlanggaran pengionan
Begitu juga, perkara boleh mendapatkan tenaga yang disediakan oleh pelbagai jenis radiasi (gamma, x -rays, ultraviolet, dll.) atau dengan bertembung dengan zarah tenaga yang tinggi (Alfas, betas dan neutron).
Tenaga yang disumbangkan sedemikian rupa sehingga elektron atom adalah segera. Pengionan jenis ini berkaitan dengan pelbagai fenomena radioaktif dan kosmik.
Pengionan air
 Pemisahan air
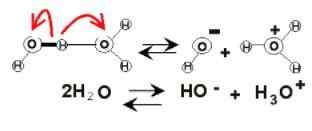
Pemisahan air Di pangkuan air, caj elektrik mungkin muncul kerana pengionannya. Ini adalah bahan kimia, kerana dua molekul air tiba -tiba bertindak balas terhadap satu sama lain untuk memisahkan dan menjana ion H3Sama ada+ Dan oh-:
2h2Atau (l) ⇌ h3Sama ada+(Ac) + oh-(Ac)
Keseimbangan ini sangat terpesona ke arah air, jadi tidak ada jumlah yang hina dari ion -ion ini.
Pengionan udara
Molekul Udara tidak mengambil bahagian dalam keseimbangan diri. Oksigen, nitrogen, argon, wap air dan gas lain yang membentuk udara, jangan bertukar atom atau elektron. Oleh itu, udara bukan konduktor elektrik yang baik dalam keadaan biasa.
Walau bagaimanapun, jika ia tertakluk kepada medan elektrik, radiasi, atau suhu yang sengit, ia boleh menjadi ion dan menjadi pemacu yang baik. Inilah yang berlaku, sebagai contoh, apabila sinar elektrik jatuh dari awan ke bumi, mengembara elektron melalui udara dengan letupan cahaya tiba -tiba.
Contoh pengionan
Sepanjang bahagian sebelumnya, beberapa contoh pengionan telah dilantik. Akhirnya, beberapa yang lain akan disebutkan.
Pengoksidaan logam
Apabila logam mengoksidakan, sama ada dengan tindakan oksigen bumi atau dengan serangan bahan berasid, mereka memperoleh caj positif untuk membentuk oksida atau garam, masing -masing.
Boleh melayani anda: Proses Kimia: Prinsip, Jenis, ContohSebagai contoh, besi diionkan terima kasih kepada oksigen untuk berubah menjadi ion iman3+, Terletak di kristal oksida besi. Magnesium, sebaliknya, larut dalam asid sulfurik untuk kehilangan elektron dan kekal sebagai ion Mg2+ Dalam garam magnesium sulfat.
Pembubaran gas di dalam air
Beberapa gas, seperti ammonia dan hidrogen klorida, larut dalam air untuk kehilangan berkecuali dan menimbulkan pembentukan ion. Contohnya, ammonia apabila ia larut sebahagiannya melepaskan ion NH4+ Dan oh-. Sementara itu, hidrogen klorida apabila melarutkan akan menghasilkan ion3Sama ada+ dan Cl- sepenuhnya.
Kes yang sama adalah pembubaran garam di dalam air, seperti magnesium sulfat, mgso4. Walau bagaimanapun, ion mg2+ Dan juga42- Mereka sudah ada di kristal garam sebelum larut di dalam air.
Lampu atau tiub pencahayaan

Dalam lampu stim atau tiub pencahayaan, atom gas dengan kejutan elektrik teruja untuk menghasilkan sejumlah cahaya dan warna tertentu. Sebagai contoh, pengionan ini berlaku dalam lampu natrium atau merkuri, serta dalam lampu neon yang terkenal dengan warna -warna cerah mereka di restoran atau penyertaan kedai.
Tenaga pengionan
Tenaga pengionan, harta berkala, dikaji untuk mencirikan unsur -unsur kimia mengikut kemudahan yang mana atom gas mereka mendermakan elektron mereka untuk memuatkan secara positif. Oleh itu, sebagai contoh, logam biasanya mempunyai tenaga pengionan terendah, sementara unsur -unsur bukan logam dan gas mulia, yang tertinggi.
Rujukan
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Serway, r., Jewett, J. (2008). Fizik untuk Sains dan Kejuruteraan. Jilid 1. Ke -7. Edisi. Mexico. Editor Pembelajaran Cengage.
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2020). Pengionan. Diperoleh dari: dalam.Wikipedia.org
- Editor enyclopaedia Britannica. (17 Oktober 2016). Pengionan. Encyclopædia Britannica. Pulih dari: Britannica.com
- Doug Stewart. (2018). Definisi pengionan: Apakah pengionan? Pulih dari: chemicool.com
- John Zavisa. (1 April 2020). Bagaimana Lightning berfungsi. Pulih dari: sains.Howstuffwork.com
- « 18 jenis tingkah laku dan ciri -ciri mereka (dengan contoh)
- Asal liberalisme kuning, ciri, sebab, akibatnya »

