Undang -undang Avogadro
- 698
- 7
- Horace Gulgowski
Apa itu undang -undang avogadro?
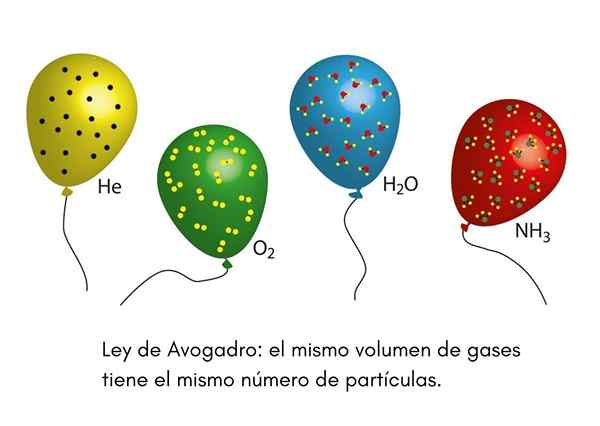
The Undang -undang Avogadro, Juga dipanggil prinsip Avogadro, ia adalah undang -undang yang terpakai kepada gas ideal dan diiktiraf oleh saintis abad kesembilan belas yang dipanggil Amadeo Avogadro. Undang -undang ini menetapkan bahawa dua jilid yang sama dengan gas yang berbeza yang berada dalam keadaan suhu dan tekanan yang sama, akan mengandungi bilangan zarah gas yang sama.
Ini bermakna, jika kita mempunyai dua belon, satu penuh dengan helium dan yang lain dengan oksigen, dan kedua -dua belon mempunyai jumlah yang sama, tekanan yang sama dan suhu yang sama, maka akan ada jumlah atom helium gas yang sama pada mulanya Globe bahawa molekul oksigen di tempat kedua.
Formula Undang -undang Avogadro
Cara lain untuk menyatakan undang -undang Avogadro adalah untuk mengatakan bahawa, jika tekanan dan suhu tetap dikekalkan, jumlah gas akan berkadar dengan bilangan tahi lalat. Ini diwakili secara matematik seperti:
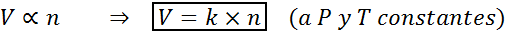
Formula ini boleh disusun semula kepada v/n = k, iaitu, hubungan antara jumlah dan bilangan tahi lalat tetap malar apabila p dan t tetap.
Oleh itu, jika kita memperkenalkan atau mengeluarkan sejumlah gas dari kontena yang memelihara p dan t tetap, jumlahnya akan berubah dan keadaan awal dan akhir akan dikaitkan dengan persamaan berikut:
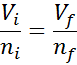
Syarat di mana undang -undang avogadro dipenuhi
Undang -undang ini berlaku tepat untuk gas ideal. Ini adalah gas yang dibentuk oleh zarah tertentu (yang tidak menduduki jumlah di ruang angkasa) yang tidak berinteraksi antara satu sama lain dengan cara apa pun.
Ia boleh melayani anda: biodiesel: sejarah, sifat, jenis, kelebihan, kelemahanSeperti namanya, jenis gas ini tidak wujud dalam realiti tetapi dalam imaginasi kita. Mereka adalah "idea" yang dipermudahkan tentang apa yang kita percaya adalah gas. Walau bagaimanapun, terdapat beberapa keadaan di mana gas sebenar, seperti udara, berkelakuan ideal: pada tekanan yang sangat rendah dan pada suhu yang sangat tinggi.
Tekanan rendah menyebabkan jumlah yang diduduki oleh zarah gas dapat diabaikan berbanding saiz bekas, sementara suhu tinggi membuat zarah bergerak begitu cepat sehingga mereka tidak mempunyai masa untuk berinteraksi ketika mereka menyeberang antara satu sama lain.
Di bawah syarat -syarat ini, kebanyakan gas memenuhi undang -undang Avogadro dengan ketepatan yang baik.
Kepentingan undang -undang avogadro
Salah satu sumbangan yang paling penting dalam undang -undang Avogadro ialah ia dibenarkan untuk menunjukkan kewujudan gas asas yang dibentuk oleh lebih daripada satu atom sebagai o2 atau h2. Ini menyumbang kepada kemajuan teori atom.
Di samping itu, undang-undang Avogadro melengkapkan undang-undang Boyle, Charles dan Gay-Lussac, dan menggabungkannya dengan ketiga-tiga undang-undang ini, undang-undang Avogadro membenarkan undang-undang gas ideal, salah satu undang-undang yang paling penting dalam kimia.
Sebaliknya, undang -undang Avogadro juga membolehkan mewujudkan hubungan antara berat molekul gas yang berlainan, kerana ia menunjukkan bahawa jisim jumlah yang sama dari gas yang berbeza diukur pada suhu dan tekanan yang sama, adalah berkadar dengan jisim setiap zarah setiap gas.
Boleh melayani anda: natrium nitrat (nano3): struktur, sifat, kegunaan, risikoOleh itu, dengan sampel penyesalan tunggal dua gas yang menduduki jumlah yang sama dengan suhu dan tekanan yang sama, hubungan antara massa molarnya dapat diperoleh.
Contoh undang -undang avogadro dalam kehidupan seharian
Belon parti
Kami pernah melihat badut di pesta kanak -kanak yang menaikkan belon helium untuk mengedarkannya di kalangan kanak -kanak. Belon ini berada pada suhu yang sama. Sekiranya dua belon parti dipenuhi dengan tekanan yang sama dan kedua -duanya adalah saiz yang sama, undang -undang Avogadro memastikan bahawa kedua -dua belon akan mempunyai bilangan mol helium yang sama.
Sebaliknya, jika salah satu belon lebih besar daripada yang lain, ia akan mempunyai jumlah yang lebih besar dan, menurut undang -undang Avogadro, ia akan mempunyai lebih banyak zarah helium di dalamnya.
Tayar kereta
Terlepas dari gas mana yang dipenuhi, tayar di seberang kereta selalu dipenuhi dengan tekanan akhir yang sama sekitar 32 psi.
Di samping itu, kami sentiasa memastikan bahawa kedua -dua karet adalah sama, jadi mereka akan mempunyai jumlah yang sama. Oleh itu, menurut prinsip Avogadro, kita boleh mengatakan bahawa kedua -dua tayar akan mengandungi bilangan zarah gas yang sama.
Picagari yang penuh dengan udara
Katakan kami mempunyai jarum suntikan terbuka dan penuh 50 cm3 udara. Seperti yang terbuka, bahagian dalam jarum suntik dan luaran (persekitaran) berada pada suhu dan tekanan yang sama.
Sekarang anggap kita tekan pelocok jarum suntik dan gerakkannya sehingga 10 cm dibaca3. Apabila jarum suntik ditemui, udara melarikan diri melalui hujung apabila plunger bergerak, jadi bilangan zarah udara di dalam jarum suntikan berkurangan bersama dengan kelantangan.
Boleh melayani anda: volatilisasiKerana tekanan atau suhu tidak berubah, undang -undang avogadro boleh digunakan untuk mengaitkan jumlah akhir dengan jumlah zarah udara yang kekal di dalam picagari. Hubungan ini adalah:
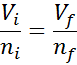
Menyusun semula persamaan ini, kami mendapatnya:
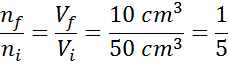
Hasil ini bermakna, jika kita mengurangkan jumlah di dalam picagari ke kelima, menjaga p dan t tetap, maka bilangan tahi lalat atau zarah yang ada di dalam pada akhir proses juga akan menjadi bahagian kelima dari apa yang asalnya.


