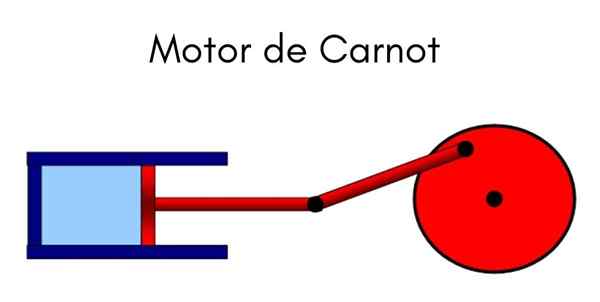
Mesin Carnot
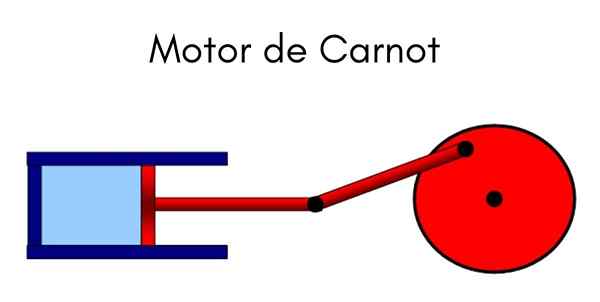
- 3618
- 416
- Delbert Dare
Apakah mesin Carnot?
The Mesin Carnot Ia adalah model kitaran yang ideal di mana haba digunakan untuk melakukan pekerjaan. Sistem ini dapat difahami sebagai omboh yang bergerak di dalam silinder yang memampatkan gas. Kitaran yang dikenakan ialah Carnot, yang dinyatakan oleh bapa termodinamik, ahli fizik Perancis dan jurutera Nicolas Leonard Sadi Carnot.
Carnot menyatakan kitaran ini pada awal abad kesembilan belas. Mesin ini tertakluk kepada empat variasi keadaan, keadaan berganti seperti suhu dan tekanan malar, di mana variasi isipadu dibuktikan apabila memampatkan dan mengembangkan gas.
Formula
Menurut Carnot, menundukkan mesin ideal kepada suhu dan variasi tekanan, mungkin untuk memaksimumkan prestasi yang diperolehi.
Kitaran Carnot mesti dianalisis secara berasingan dalam setiap empat fasa: pengembangan isoterma, pengembangan adiabatik, mampatan isoterma dan pemampatan adiabatik.
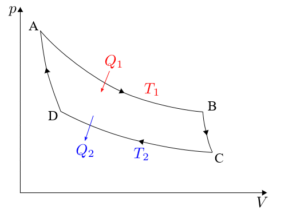
Formula yang dikaitkan dengan setiap fasa kitaran yang dikenakan pada mesin Carnot akan terperinci di bawah.
Pengembangan isoterma (A → B)
Premis fasa ini adalah seperti berikut:
- Jumlah gas: Ia dari jumlah minimum ke jumlah purata.
- Suhu mesin: suhu malar T1, nilai tinggi (t1> t2).
- Tekanan mesin: Turun dari P1 hingga P2.
Proses isoterma menunjukkan bahawa suhu T1 tidak berubah semasa fasa ini. Pemindahan haba mendorong pengembangan gas, yang mendorong pergerakan pada omboh dan menghasilkan kerja mekanikal.
Apabila berkembang, gas membentangkan kecenderungan tertentu untuk menyejukkan. Walau bagaimanapun, ia menyerap haba yang dipancarkan oleh sumber suhu dan semasa pengembangannya ia mengekalkan suhu malar.
Dapat melayani anda: apakah kelajuan linear? (Dengan latihan yang diselesaikan)Oleh kerana suhu tetap malar semasa proses ini, tenaga dalaman gas tidak berubah, dan semua haba yang diserap oleh gas secara berkesan berubah menjadi kerja. Jadi:
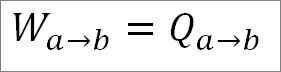
Sebaliknya, pada akhir fasa kitaran ini juga mungkin untuk mendapatkan nilai tekanan menggunakan persamaan gas ideal untuknya. Dengan cara ini, anda mempunyai perkara berikut:
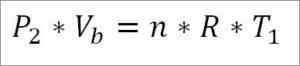
Dalam ungkapan ini:
- P2: Tekanan pada akhir fasa.
- Vb: Kelantangan di titik b.
- N: Bilangan tahi lalat gas.
- J: Pemalar sejagat gas ideal. R = 0.082 (atm*liter)/(moles*k).
- T1: Suhu awal mutlak, darjah Kelvin.
Pengembangan Adiabatik (B → C)
Semasa fasa proses ini, pengembangan gas dijalankan tanpa perlu menukar haba. Dengan cara ini, premis terperinci di bawah:
- Jumlah gas: Ia dari jumlah purata ke jumlah maksimum.
- Suhu mesin: Turun dari t1 hingga t2.
- Tekanan mesin: tekanan p2 malar.
Proses adiabatik menunjukkan bahawa tekanan P2 tidak berubah semasa fasa ini. Suhu berkurangan dan gas terus berkembang sehingga mencapai maksimum jumlahnya; iaitu, omboh mencapai bahagian atas.
Dalam kes ini, kerja yang dilakukan datang dari tenaga dalaman gas dan nilainya adalah negatif kerana tenaga berkurangan semasa proses ini.
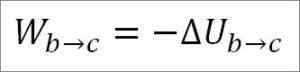
Dengan mengandaikan bahawa ia adalah gas yang ideal, teori dikekalkan bahawa molekul gas hanya mempunyai tenaga kinetik. Menurut prinsip termodinamik, ini dapat disimpulkan oleh formula berikut:
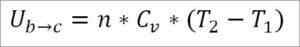
Dalam formula ini:
- ΔUb → c: Variasi tenaga dalaman gas ideal antara titik b dan c.
- N: Bilangan tahi lalat gas.
- CV: Kapasiti haba molar gas.
- T1: Suhu awal mutlak, darjah Kelvin.
- T2: Suhu akhir mutlak, darjah Kelvin.
Mampatan Isotermik (C → D)
Dalam fasa ini mampatan gas bermula; iaitu, omboh digerakkan ke dalam silinder, yang mana gas itu kontrak kelantangannya.
Keadaan yang wujud dalam proses ini terperinci di bawah:
- Jumlah gas: Ia dari jumlah maksimum ke jumlah pertengahan.
- Suhu mesin: suhu malar T2, nilai yang dikurangkan (T2 < T1).
- Tekanan mesin: Meningkatkan dari P2 hingga P1.
Di sini tekanan pada gas meningkat, jadi ia mula memampatkan. Walau bagaimanapun, suhu tetap berterusan dan, oleh itu, variasi tenaga dalaman gas adalah sifar.
Analog dengan pengembangan isoterma, kerja yang dilakukan adalah sama dengan haba sistem. Jadi:
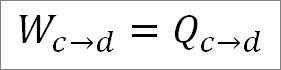
Ia juga boleh mencari tekanan pada ketika ini menggunakan persamaan gas yang ideal.
Pemampatan adiabatik (d → a)
Ini adalah fasa terakhir proses, di mana sistem kembali ke keadaan awalnya. Untuk melakukan ini, syarat -syarat berikut dipertimbangkan:
- Jumlah gas: Ia dari jumlah pertengahan hingga kelantangan minimum.
- Suhu mesin: Meningkatkan dari T2 hingga T1.
- Tekanan mesin: Tekanan berterusan P1.
Sumber haba yang dimasukkan ke dalam sistem dalam fasa sebelumnya dikeluarkan, sehingga gas ideal akan menaikkan suhunya sementara tekanan tetap tetap.
Gas kembali ke keadaan suhu awal (T1) dan pada jumlahnya (minimum). Sekali lagi, kerja yang dilakukan datang dari tenaga dalaman gas, jadi anda perlu:
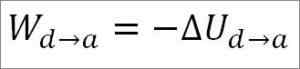
Sama seperti kes pengembangan adiabatik, adalah mungkin untuk mendapatkan variasi tenaga gas melalui ungkapan matematik berikut:
Boleh melayani anda: kalsium fluorida (CAF2): struktur, sifat, kegunaan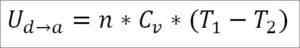
Bagaimana mesin Carnot berfungsi?
Mesin Carnot berfungsi sebagai enjin di mana prestasi dimaksimumkan oleh variasi proses isoterma dan adiabatik, menggantikan fasa pengembangan dan pemahaman gas yang ideal.
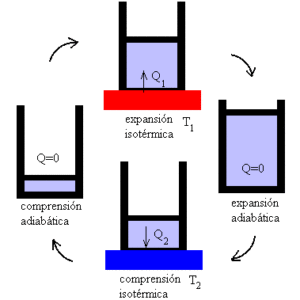
Mekanisme ini dapat difahami sebagai peranti ideal yang menjalankan pekerjaan yang tertakluk kepada variasi haba, memandangkan kewujudan dua lampu sorotan suhu.
Dalam tumpuan pertama, sistem ini terdedah kepada suhu T1. Ia adalah suhu yang tinggi yang menonjolkan sistem untuk menekankan dan menghasilkan pengembangan gas.
Sebaliknya, ini diterjemahkan ke dalam pelaksanaan kerja mekanikal yang membolehkan penggerak omboh keluar dari silinder, dan batasnya hanya mungkin oleh pengembangan adiabatik.
Kemudian datang tumpuan kedua, di mana sistem terdedah kepada suhu T2, kurang daripada T1; iaitu, mekanisme itu tertakluk kepada penyejukan.
Ini mendorong pengekstrakan haba dan penghancuran gas, yang mencapai jumlah awalnya selepas pemampatan adiabatik.
Aplikasi
Mesin Carnot telah digunakan secara meluas kerana sumbangannya dalam pemahaman tentang aspek termodinamik yang paling penting.
Model ini membolehkan anda memahami dengan jelas variasi gas ideal yang tertakluk kepada perubahan suhu dan tekanan, yang merupakan kaedah rujukan ketika merancang enjin sebenar.