Kalsium nitrat (CA (NO3) 2)

- 4583
- 327
- Anthony Breitenberg
Dia Kalsium nitrat Ia adalah garam bukan organik tertiari yang formula kimia adalah Ca (tidak3)2. Dari formulanya diketahui bahawa pepejalnya terdiri daripada ion CA2+ dan tidak3- Dalam perkadaran 1: 2. Oleh itu, ia adalah sebatian sifat ionik semata -mata.
Salah satu sifatnya adalah watak pengoksidaannya, mengikuti anion nitrat. Ia bukan bahan bakar, iaitu, ia tidak terbakar pada suhu tinggi. Menjadi bukan fuel, ia mewakili pepejal yang selamat untuk memanipulasinya tanpa penjagaan utama; Walau bagaimanapun, ia dapat mempercepatkan pencucuhan bahan mudah terbakar.
 Kalsium pepejal nitrat. Sumber: Ondřej Mangl [Domain Awam], dari Wikimedia Commons
Kalsium pepejal nitrat. Sumber: Ondřej Mangl [Domain Awam], dari Wikimedia Commons Penampilannya terdiri daripada pepejal berbutir, yang membentangkan warna putih atau kelabu ringan (imej unggul). Ia boleh menjadi anhydrous atau tetrahydrate, ca (tidak3)2· 4h2Sama ada. Ia sangat larut dalam air, metanol dan aseton.
Kalsium nitrat telah digunakan secara meluas sebagai baja, kerana ia mudah bergerak di tanah lembap, dan cepat diserap oleh akar tumbuhan. Membekalkan dua elemen penting untuk pemakanan dan pertumbuhan tumbuhan: nitrogen dan kalsium.
Nitrogen adalah salah satu daripada tiga elemen penting untuk pembangunan tumbuhan (n, p dan k), penting dalam sintesis protein. Sementara itu, kalsium diperlukan untuk mengekalkan struktur dinding sel tumbuhan. Atas sebab ini CA (tidak3)2 Taman sangat ditakdirkan.
Sebaliknya, garam ini mempunyai tindakan toksik, terutamanya dengan hubungan langsung dengan kulit dan mata, serta menghirup habuknya. Di samping itu, ia dapat dipecahkan dengan pemanasan.
Struktur kalsium nitrat
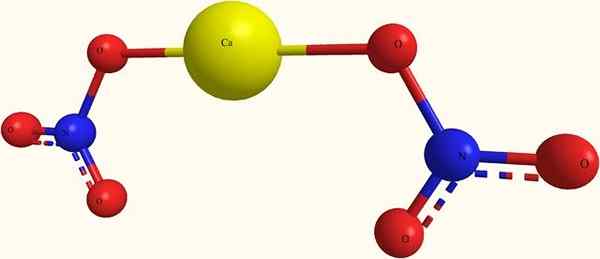 Ion kalsium nitrat. Sumber: iri.Hardnox di Ru.Wikipedia [Domain Awam], dari Wikimedia Commons
Ion kalsium nitrat. Sumber: iri.Hardnox di Ru.Wikipedia [Domain Awam], dari Wikimedia Commons Di bahagian atas, struktur CA (tidak3)2 Dalam model sfera dan bar. Di sini, bagaimanapun, terdapat kecacatan: kewujudan ikatan kovalen Ca-O diandaikan, yang bertentangan dengan watak ioniknya. Menjelaskan ini, interaksi benar -benar jenis elektrostatik.
Kation ca2+ Ia dikelilingi oleh dua anion no3- Menurut perkadarannya di kaca. Nitrogen dalam bentuk nitrat dalam struktur kristal mendominasi.
Ion dikelompokkan sedemikian rupa sehingga mereka menubuhkan konfigurasi yang ekspresi minimum adalah sel kesatuan; yang, untuk garam anhydrous, adalah padu. Iaitu, dari kiub yang mengandungi bahagian 1: 2 untuk ion -ion ini, seluruh kaca diterbitkan semula.
Boleh melayani anda: timah: struktur, sifat, mendapatkan, menggunakanSebaliknya, garam tetrahydrate, CA (tidak3)2· 4h2Atau, ia mempunyai empat molekul air untuk setiap set3- Ac2+ Tidak3-. Ini mengubah struktur kristal, mengubahnya dalam sel monoklinik kesatuan.
Oleh itu, kristal untuk kedua -dua garam, anhidrat dan tetrahidrat, berbeza; Perbezaan yang boleh ditentukan dalam sifat fizikal mereka, contohnya, titik gabungan.
Sifat fizikal dan kimia
Nama kimia
-Kalsium nitrat
-Kalsium dinitrate
-Nitrocalcita
-Salitre dan Limesaltpetro Norway.
Formula molekul
Spout3)2 atau boleh2Sama ada6
Berat molekul
Anhidro 164,088 g/mol dan tetrahydrate 236.15 g/mol. Perhatikan kesan air pada berat molekul, dan tidak boleh dihina ketika membuat berat masing -masing.
Penampilan fizikal
Granul kelabu pepejal atau muda. Kristal putih kubik atau granul yang lazat; iaitu, mereka menyerap kelembapan sehingga mereka membubarkan produk kelarutan yang tinggi.
Takat didih
Bentuk anhydrous terurai dengan pemanasan pada suhu yang menghalang penentuan titik mendidihnya; Walaupun bentuk garam tetrahydrate mempunyai titik mendidih 132 ºC (270 ºF, 405 K).
Takat lebur
-Borang Anhydra: 561 ºC hingga 760 mmHg (1042 ºF, 834 K).
-Borang Tetrahydrate: 42.7 ºC (109 ºF, 316 K).
Ini menunjukkan bagaimana molekul air mengganggu interaksi elektrostatik antara CA2+ dan tidak3- di dalam kristal; Dan akibatnya, pepejal cair pada suhu yang jauh lebih rendah.
Kelarutan air
-Borang Anhydra: 1212 g/L pada 20 ºC.
-Tetrahydrate Borang: 1290 g/L pada 20 ºC.
Air dalam kristal hampir tidak meningkatkan kelarutan garam.
Kelarutan dalam pelarut organik
-Dalam etanol, 51.42 g/100 g pada 20 ºC.
-Dalam metanol, 134 g/100 g pada 10 ºC.
-Dalam aseton, 168 g/100 g pada 20 ºC.
Keasidan (PKA)
6.0
Ketumpatan
2.5 g/cm3 pada 25 ºC (tetrahydrate).
Penguraian
Apabila kalsium nitrat dipanaskan kepada incandescence, ia terurai menjadi kalsium oksida, nitrogen oksida dan oksigen.
Profil reaktif
Ia adalah ejen pengoksidaan yang kuat, tetapi ia bukan bahan bakar. Mempercepat pencucuhan bahan mudah terbakar. Bahagian kalsium nitrat menjadi zarah halus, memudahkan letupannya apabila sebatian itu terdedah kepada api yang berpanjangan.
Boleh melayani anda: aloi bukan ferus: struktur, sifat, kegunaan, contohCampuran dengan ester alkil menjadi letupan dengan menyebabkan ester alkil nitrat. Gabungan kalsium nitrat dengan fosforus, timah klorida (II) atau ejen pengurangan lain, boleh bertindak balas secara meletup.
Aplikasi
Pertanian
Ia digunakan dalam tanaman sebagai sumber nitrogen dan kalsium. Kalsium nitrat sangat larut di dalam air dan mudah diserap oleh akar tumbuhan. Di samping itu, ia tidak mengasingkan tanah kerana ion mereka tidak dapat menghidrolisis.
Campurannya harus dielakkan dengan baja yang mengandungi fosforus atau sulfat, untuk mengelakkan pembentukan garam tidak larut. Mengikuti hygroscopicity anda, ia mesti disimpan dalam persekitaran yang kering dan segar.
Penggunaannya mempunyai kelebihan terhadap penggunaan ammonium nitrat sebagai baja. Walaupun sebatian terakhir membawa nitrogen ke tumbuh -tumbuhan, mengganggu penyerapan kalsium, yang boleh menghasilkan kekurangan kalsium dalam tumbuhan.
Kalsium menyumbang kepada penyelenggaraan struktur dinding sel tumbuhan. Di hadapan kekurangan kalsium, tisu dalam pembentukan tumbuhan, seperti hujung akar, daun muda dan hujung wabak, sering menunjukkan pertumbuhan yang menyimpang.
Penurunan ammonium
Kalsium nitrat mengurangkan pengumpulan asid lemak yang tidak menentu dan sebatian fenolik, fitotoksik yang terkumpul oleh penguraian sisa soya.
Di samping itu, terdapat trend kalsium nitrat untuk mengurangkan kepekatan ammonium di dalam tanah, yang meningkatkan kapasiti redaman hidrogen.
Konkrit
Kalsium nitrat digunakan untuk mengurangkan masa penetapan konkrit. Ini dihasilkan oleh penjanaan kalsium hidroksida, dengan mungkin reaksi anjakan berganda.
Di samping itu, kalsium nitrat mendorong penjanaan sebatian hidroksida besi, yang tindakan perlindungan konkrit mengurangkan kakisannya. Iaitu, besi sekarang boleh bertindak balas dengan komponen asas konkrit, seperti kalsium hidroksida itu sendiri.
Kalsium nitrat mengurangkan masa penetapan, serta rintangan konkrit, yang mana abu gunung berapi ditambah. Untuk mengkaji kesan agregat kalsium nitrat ke konkrit, meningkatkan kepekatan kalsium nitrat, antara 2% dan 10% telah digunakan.
Ia boleh melayani anda: pecahan molar: bagaimana ia dikira, contoh, latihanPenurunan yang lebih besar dalam penetapan masa telah diperhatikan, serta peningkatan rintangan konkrit sebagai kepekatan kalsium nitrat meningkat kepada 10%.
Rawatan kumbahan atau sisa
Kalsium nitrat digunakan untuk mengurangkan bau kumbahan yang buruk, dengan mengurangkan sulfida hidrogen. Di samping itu, bahan organik yang menjana keadaan anaerobik yang menghalang kelangsungan hidup banyak spesies biologi dimakan.
Penyediaan kompres sejuk
Tetrahydrate kalsium nitrat adalah sebatian endotermik, iaitu, ia mempunyai keupayaan untuk menyerap haba dari persekitaran yang mengelilinginya. Ini menghasilkan penyejukan badan yang bersentuhan dengan bekas yang mengandunginya.
Memampatkannya meningkatkan suhu mereka, dan untuk menjana semula mereka, sudah cukup untuk meletakkannya di dalam peti sejuk
Pembekuan lateks
Kalsium nitrat digunakan dalam fasa pembekuan lateks. Ia adalah sebahagian daripada penyelesaian rendaman, dan apabila ia bersentuhan dengan penyelesaian yang mengandungi lateks, ia memecahkan penstabilannya dan menyebabkan pembekuannya.
Pemindahan dan penyimpanan haba
Campuran binari garam nitrat cair, termasuk kalsium dengan nitrat lain, digunakan bukannya minyak terma dalam tumbuhan tenaga solar untuk pemindahan dan penyimpanan haba.
Bentuk permohonan
-Kalsium nitrat bercampur dengan tanah digunakan untuk kepekatan 1.59 kg untuk 30.48 m2, dengan pengairan yang mencukupi. Kalsium nitrat diselesaikan di dalam air, yang membolehkan penyerapannya oleh akar tumbuhan. Dalam tanaman hidroponik ia larut dalam air penanaman.
-Nitrat kalsium berbentuk semburan juga digunakan untuk menyemburkan daun dan bunga, menjadi rawatan yang berkesan dalam pencegahan reput bunga tomato, tempat gabus dan lubang pahit epal.
-Ia ditambah kepada campuran bentuk konkrit (simen, pasir, batu dan air) jumlah kalsium nitrat, dan kesan penambahannya pada sifat -sifat tertentu konkrit; seperti menetapkan kelajuan dan rintangan.
-Kalsium nitrat ditambah kepada kepekatan yang mencukupi untuk mengurangkan bau kumbahan atau sisa yang tidak baik, ke tahap yang bau boleh diterima oleh orang.
Rujukan
- Spesifikasi kalsium nitrat. Pulih dari: Direct2farmer.com
- Kalsium nitrat. Pulih dari: pubchem.NCBI.NLM.NIH.Gov

