Struktur Kimia Pencanona, Sifat, Sintesis, Kegunaan
- 1488
- 279
- Julius Dibbert
The Pentanona Ia adalah sebatian organik, milik keluarga keton, yang formulanya adalah c5H10Sama ada. Ia tetap menjadi salah satu keton yang paling mudah, dan terdiri daripada cecair tanpa warna dengan aroma yang serupa dengan aseton. Dari situ dari sekarang, berkenaan dengan nombor karbon kerangka mereka, Ketones hadir isomer kedudukan.
Semasa bercakap mengenai kedudukan isomeria merujuk kepada tempat kumpulan karbonil, c = o. Oleh itu, Puntanona sebenarnya terdiri daripada dua sebatian dengan sifat fizikal yang berbeza antara satu sama lain: 2-penon dan 3-penon (imej yang lebih rendah). Kedua -duanya cair, tetapi titik mendidih mereka adalah sama, jadi mereka tidak dapat dipisahkan oleh penyulingan.
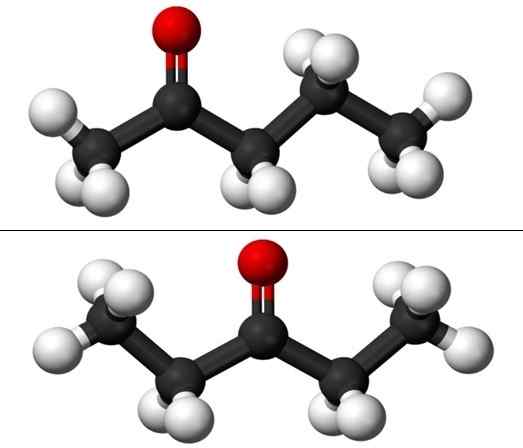
 Molekul isomer kedudukan untuk Pentanona. Sumber: Jynto & Ben Mills melalui Wikipedia.
Molekul isomer kedudukan untuk Pentanona. Sumber: Jynto & Ben Mills melalui Wikipedia. Walau bagaimanapun, setiap dua pentanon mempunyai laluan sintesis sendiri, jadi tidak mungkin terdapat campuran mereka; campuran yang mungkin dapat dipisahkan dengan membeku.
Kegunaannya terhad terutamanya sebagai pelarut organik; Alternatif untuk aseton dalam media di mana anda bekerja dengan suhu yang lebih tinggi daripada titik mendidih yang rendah. Mereka juga memulakan bahan untuk sintesis organik yang lain, kerana kumpulan mereka C = o dapat mengurangkan atau mengalami penambahan nukleofilik.
[TOC]
Struktur kimia
Isomer kedudukan
Dalam imej kita mempunyai struktur molekul kedua -dua isomer kedudukan untuk puntanona, yang diwakili oleh model sfera dan bar. Sfera hitam sesuai dengan kerangka berkarbonat, putih ke atom hidrogen, dan atom oksigen merah dalam kumpulan c = o.
2-Pintanone
2-Ponanona (di atas) mempunyai kumpulan C = atau dalam karbon kedua, yang bersamaan dengan jika ia berada di dalam bilik; iaitu, 2-Ponanona dan 4-pantanona bersamaan, kerana sudah cukup untuk memutarnya 180º sehingga struktur mereka sama.
Boleh melayani anda: Karbon Tetrachloride (CCL4)Di sebelah kiri C = o anda mempunyai radikal metil, cho3-, Dan di sebelah kanannya, propil radikal. Itulah sebabnya Cetona ini juga menerima nama (kurang digunakan) dari Metil Propil Cetona (MPK dalam Bahasa Inggeris). Anda dapat melihat asimetri struktur ini pada pandangan pertama.
3-penone
3-péntanona (di bawah) mempunyai kumpulan c = o dalam karbon ketiga. Perhatikan bahawa isomer ini adalah versi aseton yang lebih besar, dan ia juga sangat simetri; Kedua -dua radikal di sisi kumpulan c = o adalah sama: dua radikal etil, CH3Ch2-. Itulah sebabnya 3-pananona juga dipanggil cetona diestil (atau dimetil aseton).
Interaksi intermolecular
Kehadiran kumpulan karbonil, baik dalam 2-pantanone dan di 3-penona, memberikan kutub kepada molekul.
Oleh itu, kedua-dua isomer Pentanona dapat berinteraksi antara satu sama lain melalui dipole-dipol.
Begitu juga, penyebaran London antara karbon dan kerangka hidrogenasi campur tangan ke tahap yang lebih rendah.
Dengan mempunyai puntanona, kawasan molekul yang lebih besar dan jisim berbanding dengan aseton, sumbangan ini menambah momen dipole dan membolehkan titik didih yang lebih tinggi (102 ºC> 56 ºC) untuk memiliki titik didih yang lebih tinggi). Malah, kedua -dua isomer menguap pada 102 ºC; sementara mereka membeku pada suhu yang berbeza.
Kristal
Mungkin dalam penghabluran melakukan simetri memainkan peranan penting. Sebagai contoh, titik gabungan 2 -pantanona adalah -78 ºC, manakala 3 -péntanona, -39 ºC.
Boleh melayani anda: undang -undang avogadroIni bermakna kristal 3-Pantanona lebih stabil terhadap suhu; Molekulnya lebih kohesif dan memerlukan lebih banyak haba untuk dipisahkan dalam fasa cecair.
Sekiranya terdapat campuran kedua-dua isomer, 3-penon akan menjadi yang pertama untuk mengkristal, akhirnya menjadi 2-pananona pada suhu yang lebih rendah. Molekul 3-pantanone, lebih simetri, berorientasikan lebih mudah daripada yang 2-Ponanona: asimetrik dan pada masa yang sama lebih dinamik.
Sifat
Penampilan fizikal
Cecair tanpa warna dengan aroma yang serupa dengan aseton.
Jisim molar
86.13 g/mol
Ketumpatan
0.81 g/ml (3-Ponanona)
0.809 g/ml (2-Ponanona)
Takat lebur
-78 ºC (2-Ponanona)
-39 ºC (3-Ponanona)
Takat didih
102 ºC (untuk kedua -dua isomer)
Kelarutan air
35 g/l (3-Ponenona)
60 g/l (2-Ponenona)
Tekanan wap
35 mmhg (3-Ponenona)
270 mmHg (2-pantanone) pada 20 ºC
Nilai -nilai ini tidak berguna untuk membandingkan tekanan wap secara langsung kedua -dua isomer, seperti yang pertama dilaporkan tanpa suhu di mana ia diukur.
Titik kilat
12.78 ºC (3-Ponanona)
10 ºC (2-Ponanona)
Kestabilan
Kedua -dua isomer Pentanona sangat mudah terbakar, jadi mereka mesti tinggal jauh dari sumber haba. Titik kilat menunjukkan bahawa api boleh menetapkan wap kedua -dua pentanas walaupun pada suhu 10 ºC.
Sintesis
Walaupun kedua -dua isomer Pentanona secara fizikal dan kimia sangat serupa, laluan sintetik mereka bebas daripada yang lain, jadi tidak mungkin kedua -duanya diperolehi dalam sintesis yang sama.
2-Pintanone
Bermula dari reagen 2-penol, alkohol sekunder, ini boleh dioksidakan hingga 2-ponanon menggunakan asid hipoklorus yang terbentuk di situ, HCLO, sebagai ejen pengoksidaan. Pengoksidaan akan:
Ia boleh melayani anda: tiada elektrolit: ciri dan contoh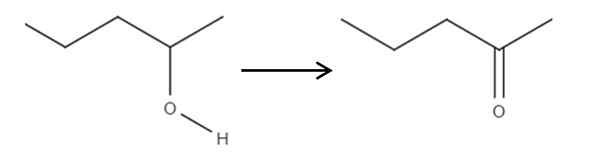 Pengoksidaan 2-pantanol di 2-Pantanona. Sumber: Gabriel Bolívar.
Pengoksidaan 2-pantanol di 2-Pantanona. Sumber: Gabriel Bolívar. Cukup pautan c-oh menjadi c = o. Terdapat kaedah lain untuk mensintesis 2-penona, tetapi ini adalah yang paling mudah difahami.
3-penone
3-pintanone boleh disintesis dengan cara3Ch2COOH. Laluan sintetik ini menghasilkan keton simetri, dan adalah molekul CHO3COOH akan kehilangan kumpulan COOH dalam bentuk CO2, Sementara kumpulan anda yang lain oh dalam bentuk h2Sama ada:
2ch3Ch2Cooh => ch3Ch2COCH2Ch3 + Co2 + H2Sama ada
Satu lagi laluan yang lebih kompleks adalah untuk bertindak secara langsung campuran etilena, CHO2= Ch2, Co2 dan h2 Untuk membentuk 3-Ponanona.
Aplikasi
Kecuali permohonan itu sangat ketat, ia adalah sintesis tertentu, atau ia juga telah menunjukkan bahawa kedua-dua isomer tidak menyebabkan hasil yang sama, tidak relevan untuk memilih antara menggunakan 2-penon atau 3-penone dalam mana-mana penggunaan.
Iaitu, "tidak penting" jika anda ingin menggunakan 2-Ponanona atau 3-penona sebagai pelarut lukisan atau resin, atau sebagai sengsara, kerana kriteria yang paling penting akan menjadi harga dan ketersediaannya. 3-penone digunakan dalam industri automotif untuk mengkaji tingkah laku gas di dalam enjin pembakaran dalaman.
Rujukan
- Morrison, r. T. dan Boyd, R, n. (1987). Kimia organik. Edisi ke -5. Editorial Addison-Wesley Inter-American.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. Amina. (Edisi ke -10.). Wiley Plus.
- Wikipedia. (2019). 3-Pain. Diperoleh dari: dalam.Wikipedia.org
- Pusat Kebangsaan Maklumat Bioteknologi. (2019). 2-pontenone. Pangkalan data PUBCHEM. CID = 7895. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Persatuan Kimia Diraja. (2019). 3-Pain. Pulih dari: chemspider.com
- Profesor t. Nalli. (2013). Pengoksidaan 2-polit dan penyulingan produk. Pulih dari: kursus1.Winona.Edu

