Struktur piridin, sifat, kegunaan, ketoksikan, sintesis
- 3158
- 351
- Julius Dibbert
The Pyridine Ia adalah amina aromatik yang formula kimia adalah c5H5N. Ia adalah versi nitrogen benzena, sebagai kumpulan -ch = telah digantikan oleh atom nitrogen (n). Bersama Pyrol, piridin membentuk kumpulan amina aromatik yang lebih mudah.
Pada mulanya piridin berlaku dari tar hulla, tetapi ia adalah kaedah prestasi yang sedikit. Ini membawa kepada penciptaan beberapa kaedah untuk sintesis kimianya, yang berlaku di mana reaksi formaldehid, acetaldehyde dan ammonia digunakan.
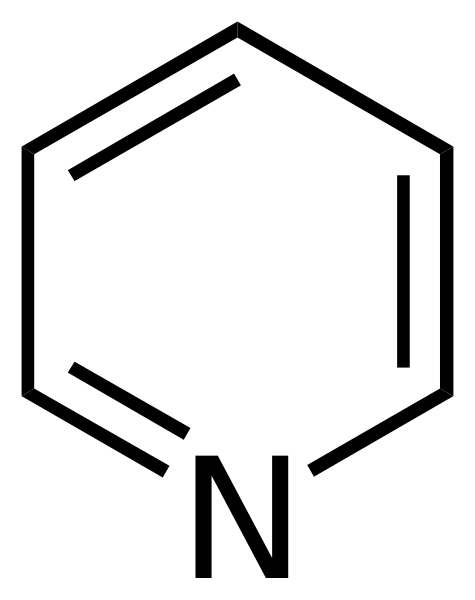 Formula struktur piridin. Sumber: Calvero. / Domain awam
Formula struktur piridin. Sumber: Calvero. / Domain awam Pyridine diperoleh buat kali pertama oleh Thomas Anderson (1843), seorang ahli kimia escosses, yang melalui pemanasan daging dan tulang haiwan menghasilkan minyak dari mana piridin itu disucikan.
 Thomas Anderson (Julai 1819)
Thomas Anderson (Julai 1819) Pyridine digunakan sebagai bahan mentah untuk sintesis sebatian yang menghilangkan dan mengawal percambahan serangga, kulat, herba, dll. Ia juga digunakan dalam penjelasan banyak ubat dan vitamin, selain digunakan sebagai pelarut.
Pyridine adalah sebatian toksik yang boleh merosakkan kronik pada hati, buah pinggang dan fungsi sistem saraf pusat. Piridin boleh memasuki badan kerana pengambilan, penyedutan dan penyebaran melalui kulit. Ia dikenali dalam bahan kimia kerana ia adalah bahan yang mampu menyebabkan ketidakberdayaan pada lelaki.
[TOC]
Struktur piridin
Molekul
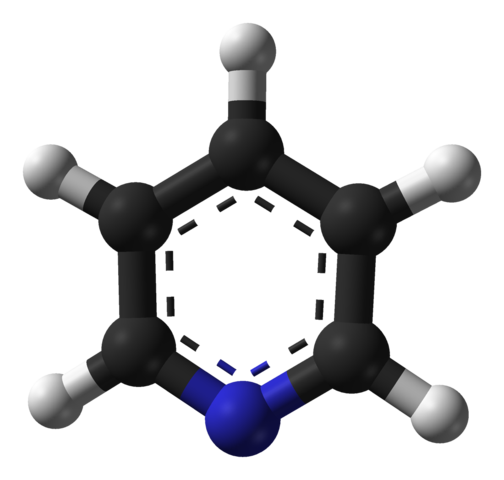 Struktur molekul piridin. Sumber: Benjah-bmm27 / domain awam
Struktur molekul piridin. Sumber: Benjah-bmm27 / domain awam Imej unggul menunjukkan struktur molekul piridin yang diwakili oleh model sfera dan bar. Seperti yang dapat dilihat, molekulnya sangat mirip dengan benzena, dengan satu -satunya perbezaan yang mempunyai salah satu karbonnya (sfera hitam) digantikan oleh nitrogen (sfera biru).
Nitrogen, kerana ia lebih elektronegatif, menarik kepadatan elektronik ke arah dirinya sendiri, yang menghasilkan momen dipole kekal di piridin. Oleh itu, molekul piridin berinteraksi melalui daya dipole-dipolo.
Atom hidrogen adalah kawasan termiskin di elektron, sehingga mereka akan berorientasikan ke arah atom nitrogen molekul jiran.
Kristal
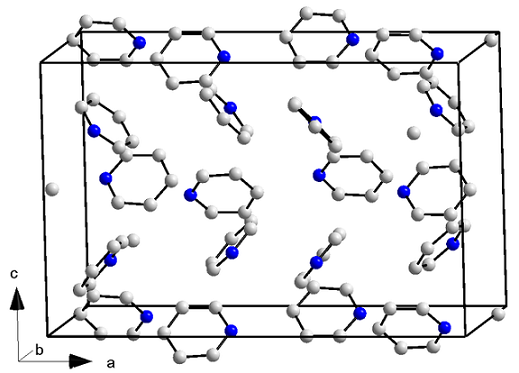
 Struktur piridin kristal. Sumber: ORCI/CC BY-S (https: // creativeCommons.Org/lesen/by-sa/3.0)
Struktur piridin kristal. Sumber: ORCI/CC BY-S (https: // creativeCommons.Org/lesen/by-sa/3.0) Molekul piridin bukan sahaja mempunyai daya dipole-dipolo, tetapi juga dengan interaksi cincin aromatik. Oleh itu, molekul -molekul ini berjaya meletakkan diri mereka secara teratur untuk menyebabkan kristal struktur ortorrombik (imej atas) pada suhu -41.6 ° C.
Sifat piridin
 Sampel Pyridine. LHCHEM/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/3.0)
Sampel Pyridine. LHCHEM/CC BY-SA (https: // creativeCommons.Org/lesen/by-sa/3.0) Penampilan fizikal
Cecair tanpa warna, dengan bau menembusi, serupa dengan ikan.
Boleh melayani anda: Kaedah keseimbangan redoks: Langkah, contoh, latihanJisim molar
79.1 g/mol
Ketumpatan
0.9819 g/ml
Takat lebur
-41.6 ºC
Takat didih
115.2 ºC
Kelarutan
Ia boleh didapati dengan air, dan juga dengan alkohol, eter, minyak eter, minyak dan banyak cecair organik secara umum.
Tekanan wap
16 mmHg pada 20 ºC.
Ketumpatan wap
2,72 berhubung dengan air = 1
Indeks pembiasan (nD)
1,5093
Goo
0.88 cp
Momen dipolar
2.2 d
titik pencucuhan
21 ºC
Suhu arah diri
482 ºC
Penguraian
Apabila dipanaskan hingga penguraian memancarkan asap sianida.
Kakisan
Pyridine dalam bentuk cecair menyerang beberapa bentuk plastik, karet dan lapisan.
Ph
8.5 (penyelesaian 0.2 m dalam air)
Asas dan kereaktifan
Piridin adalah asas yang lemah. Ia adalah amina tersier yang larutan 0.2 m dalam air menghasilkan pH 8.5. Ia mempunyai sedikit pertalian untuk elektron kerana elektronegativiti nitrogen, jadi karbon mereka biasanya tidak mengalami penggantian elektrofilik.
Pyridine mengalami penggantian nukleofilik, lebih baik dalam kedudukan c4 dan c2 Dari cincin. Oleh kerana keupayaannya untuk menderma elektron, piridin lebih banyak pengoksidaan lebih daripada benzena dan bertindak balas dengan ganas dengan asid sulfurik, asid nitrik dan anhidrida maleico.
Penggunaan pyridine
Racun perosak
Pyridine adalah pendahuluan herbisida yang terdahulu dan diquat. Dengan cara yang sama, ia berfungsi untuk sintesis insektisida chlorpirifos, yang langkah awalnya adalah pengklorinan piridin. Ia juga merupakan bahan mentah awal untuk mendapatkan fungisida berdasarkan piru.
Pelarut
Pyridine adalah pelarut kutub, digunakan untuk tindak balas peniaga dan pengekstrakan antibiotik. Pyridine digunakan sebagai pelarut dalam industri cat dan getah, dan juga di makmal penyelidikan sebagai pelarut dalam pengekstrakan hormon tumbuhan.
Ubat
Pyridine berfungsi sebagai titik awal dalam sintesis cetilpyridinium dan laurilpyridinium, sebatian yang digunakan sebagai antiseptik dalam produk penjagaan lisan dan pergigian. Molekul piridin adalah sebahagian daripada struktur kimia pelbagai ubat.
Sebagai contoh, esmeprazole, yang digunakan dalam rawatan refluks gastroesophageal. Loratidine adalah ubat lain yang disediakan berdasarkan piridin, yang dikenali sebagai claritin, yang digunakan sebagai rawatan proses alergi.
Tablet piridin (phenazopyridine) digunakan dalam rawatan gejala kerengsaan saluran kencing, yang disertai, dalam beberapa kes, kesakitan, pembakaran dan segera kencing. Phenazopyridine adalah pewarna yang memenuhi fungsi analgesik di saluran kencing.
Di-acylhidrazine adalah derivatif piridin yang mempunyai aktiviti antibakteria yang menggunakan bakteria negatif gram, seperti Dan. coli, dan bakteria positif gram, seperti S. Albus.
Pyridine berfungsi sebagai asas untuk thiazolo [5,4-6] piridin, terdiri daripada aktiviti antiviral, terutamanya terhadap virus β-massa influenza. 2-acetylpyridine, derivatif piridin, mempunyai aktiviti antitumor yang hebat dan merupakan perencat leukemia.
Boleh melayani anda: Mercury Oxide (HG2O)Yang lain
Pyridine digunakan dalam pembuatan vitamin, produk getah, pelekat, lukisan dan racun serangga. Ia juga digunakan dalam denaturasi alkohol dan dalam pewarnaan beberapa tekstil.
20 % piridin digunakan dalam penyediaan piperidine. Piperidine campur tangan dalam pemvulkanan dan pertanian.
Pyridine juga digunakan dalam sintesis resin polikarbonat, sebagai rasa makanan dan sebagai reagen untuk pengesanan sianida.
Ketoksikan
- Piridin memasuki organisma terutamanya disebabkan oleh penyedutan dan penyebaran melalui kulit. Pendedahan akut kepada piridin dapat menghasilkan kerengsaan dan luka bakar di mata dan kulit.
- Piridin boleh berasal dermatitis dan alahan pada kulit. Perkembangan alahan boleh disertai selain gatal -gatal dan ruam.
- Penyedutan piridin boleh menyebabkan kerengsaan hidung dan tekak, disertai dengan batuk dan nafas pernafasan asma.
- Dengan pengambilan, piridin boleh menyebabkan mual, muntah, cirit -birit dan sakit perut. Begitu juga, penggabungan dos piridin yang tinggi ke dalam organisma boleh menyebabkan: sakit kepala, keletihan, pudar, menakjubkan, pening, kekeliruan dan akhirnya makan dan mati.
- Organ -organ yang paling terjejas oleh tindakan piridin adalah hati, buah pinggang, alat kelamin lelaki dan sistem saraf pusat. Ia juga boleh bertindak pada sumsum tulang, mendorong pengeluaran platelet darah. Tindakan karsinogenik piridin belum dibuktikan pada haiwan.
OSHA menubuhkan pendedahan di udara 5 ppm setiap hari kerja.
Sintesis
Kaedah pertama mendapatkan piridin adalah berdasarkan pengekstrakan bahan organik. Thomas Anderson (1843) diperoleh buat kali pertama piridin dengan memanaskan daging dan tulang haiwan. Pada peringkat pertama, Anderson menghasilkan minyak dari mana dia berjaya menyuling piridin.
Secara tradisinya, piridin diperoleh dari hulla tar atau gasifikasi arang batu. Prosedur ini rumit dan sedikit prestasi, kerana kepekatan piridin dalam bahan mentah ini sangat rendah. Kaedah sintesis diperlukan.
Kaedah Chichibabin
Walaupun terdapat banyak kaedah untuk sintesis piridin, prosedur chichibabin yang diperkenalkan pada tahun 1923 masih digunakan terutamanya. Dalam kaedah ini, piridin disintesis dari reaksi formaldehid, acetaldehid dan ammonia, yang merupakan reagen murah.
Boleh melayani anda: jenis pautan 02Di peringkat pertama, formaldehid dan asetaldehid bertindak balas untuk membentuk sebatian acroleine, dalam reaksi pemeluwapan knoevegel, juga membentuk air.
 Pemeluwapan piridin dari acroleína dan acetaldehyde
Pemeluwapan piridin dari acroleína dan acetaldehyde Akhirnya, pada peringkat kedua, Acroleína bertindak balas dengan formaldehid dan ammonia untuk membentuk dihydropyridine. Selepas itu, dihydropyridine dioksidakan kepada piridin dalam tindak balas pada 350 -550 ° C dengan kehadiran pemangkin pepejal, contohnya, silika -alumina.
Reaksi
Penggantian elektrofil
Penggantian ini biasanya tidak berlaku disebabkan oleh ketumpatan piridin elektronik yang rendah.
Sulfanasi memberikan kesukaran yang lebih besar daripada nitrasi. Tetapi bromasi dan pengklorinan berlaku dengan lebih mudah.
Pyridine-n-oksida
Tapak pengoksidaan di piridin adalah atom nitrogen, yang menjadi pengoksidaan yang dihasilkan oleh pic (asid yang mempunyai kumpulan OOH). Pengoksidaan nitrogen menggalakkan penggantian elektrofilik dalam karbon 2 dan 4 piridin.
Penggantian nukleofilik
Pyridine boleh mengalami beberapa penggantian nukleofilik kerana ketumpatan elektronik rendah karbon cincin piridin. Penggantian ini berlaku lebih mudah dalam molekul piridin yang diubahsuai oleh bromin, klorin, fluorin atau asid sulfonik.
Sebat.
Reaksi radikal
Pyridine boleh diminjau oleh reaksi radikal. Dimerization piridin radikal dilakukan dengan natrium asas atau nikel raney, dapat menghasilkan 4.4'-bipperidine atau 2.2'-bipperidine.
Tindak balas pada atom nitrogen
Asid, menurut Lewis, mudah ditambah kepada atom nitrogen piridin, membentuk garam piridin. Pyridine adalah pangkalan Lewis yang menyumbangkan beberapa elektron.
Tindak balas penghidrogenasi dan pengurangan
Piperidine dihasilkan oleh penghidrogenan piridin dengan nikel, kobalt atau ruthenium. Tindak balas ini dibuat pada suhu tinggi yang disertai dengan penggunaan pemangkin.
Rujukan
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (10th Edisi.). Wiley Plus.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Morrison dan Boyd. (1987). Kimia organik. (Edisi Kelima). Addison-Wesley Iberoamericana.
- Wikipedia. (2020). Pyridine. Diperoleh dari: dalam.Wikipedia.org
- Pusat Kebangsaan Maklumat Bioteknologi. (2020). Pyridine. Pangkalan data PUBCHEM., CID = 1049. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Laura Foist. (2020). Pyridine: struktur, formula & sifat fizikal. Kajian. Pulih dari: belajar.com
- Atof Ali Altaf, Adnan Shahzad, Zarif Gul, Nasir Rasool, Amin Badshah, Bhajan Lal, Ezzat Khan. (2015). Kajian mengenai kepentingan perubatan derivatif piridin. Jurnal Reka Bentuk Dadah dan Kimia Ubat. Vol. 1, tidak. 1, ms. 1-11. Doi: 10.11648/j.JDDMC.20150101.sebelas
- Webmd. (2020). Tablet Pyridin. Diperolehi dari: WebMD.com
- Jabatan Kesihatan dan Perkhidmatan Kanan New Jersey. (2002). Pyridine. [Pdf]. Pulih dari: NJ.Gov
- « C ++ Sejarah, Ciri, Jenis Data, Contoh
- Fungsi Asid Lemak Essential, Kepentingan, Nomenclature, Contoh »

