Asas ujian, teknik dan kegunaan Catalase

- 1726
- 118
- Ms. Santos Fritsch
The Catalase Ini adalah metodologi yang digunakan dalam makmal bakteriologi untuk menyerlahkan kehadiran enzim catalase dalam bakteria yang memilikinya. Di sebelah pewarnaan Gram adalah ujian utama yang perlu dilakukan pada mikroorganisma yang baru terpencil. Ujian ini membimbing ahli mikrobiologi pada langkah -langkah untuk diikuti untuk mengenal pasti mikroorganisma yang dipersoalkan.
Secara umum, bakteria yang mengandungi cytochrome mempunyai enzim catlase, iaitu bakteria anaerobik aerobik dan pilihan harus memilikinya. Walau bagaimanapun, terdapat pengecualian, seperti Streptococcus, yang walaupun mikroorganisma anaerobik pilihan tidak mempunyai enzim catalase.
 Pelaksanaan ujian catalase, menunjukkan reaksi positif. Sumber: Tiada pengarang yang boleh dibaca mesin yang disediakan. Nase diasumsikan (berdasarkan tuntutan hak cipta). [CC BY-SA 3.0 (http: // creativeCommons.Org/lesen/by-sa/3.0/]]
Pelaksanaan ujian catalase, menunjukkan reaksi positif. Sumber: Tiada pengarang yang boleh dibaca mesin yang disediakan. Nase diasumsikan (berdasarkan tuntutan hak cipta). [CC BY-SA 3.0 (http: // creativeCommons.Org/lesen/by-sa/3.0/]] Itulah sebabnya ujian catalase digunakan terutamanya untuk membezakan staphylococaee dan micrococaceae (kedua -dua catalase positif) dari keluarga streptococaee (catalase negatif) (catalase negatif).
Begitu juga, genus Bacillus (Catalase Positif) dibezakan dari genus Clostridium (Catalase Negatif), antara lain.
[TOC]
Asas
Catalase adalah enzim yang diklasifikasikan sebagai hidroperoxidase, ini bermakna mereka menggunakan hidrogen peroksida sebagai substrat (h2Sama ada2).
Ia juga dianggap sebagai oksidoreductase, kerana dalam tindak balas di mana terdapat elemen yang berfungsi sebagai penderma elektron (mengurangkan bahan) dan satu lagi sebagai penerima elektron (bahan pengoksidaan).
Catalase adalah protein yang mengandungi kumpulan prostorik dengan empat atom besi trivalen (Faith+++), oleh itu ia adalah homoprotein. Ion ferrik tetap teroksida semasa reaksi.
Dikatakan bahawa catalase adalah enzim detoksifikasi, kerana fungsinya adalah untuk menghapuskan bahan yang berlaku semasa metabolisme bakteria yang beracun kepada bakteria. Antara bahan ini ialah hidrogen peroksida.
Hidrogen peroksida terbentuk dari penguraian gula oleh aerobik. Proses ini berlaku seperti berikut:
Ion superoxide (atau2-) (Radikal bebas) dibentuk sebagai produk akhir asimilasi glukosa oleh jalan aerobik. Ini adalah toksik dan dihapuskan oleh dismutase superoxide enzim yang mengubahnya menjadi oksigen gas dan hidrogen peroksida.
Ia boleh melayani anda: Holdridge Life Zon: Apa yang ada di Amerika LatinHidrogen peroksida juga toksik kepada bakteria dan mesti dihapuskan. Enzim catalase membentangkan hidrogen peroksida dalam air dan oksigen.
Catalase boleh bertindak pada substrat lain selain daripada hidrogen peroksida, seperti alkohol, aldehid, asid, amina aromatik dan fenol. Walau bagaimanapun, hidrogen peroksida juga boleh digunakan oleh catalase untuk mengoksidakan sebatian toksik lain seperti metil dan etil alkohol.
Begitu juga, catalase terdapat dalam sel phagocytic, melindunginya dari tindakan toksik hidrogen peroksida.
Teknik rutin untuk ujian catalase
-Kaedah dalam slaid
Bahan
3% hidrogen peroksida (10 jilid).
Lamina mudah alih
Pemegang plastik guna atau kayu kayu.
Prosedur
Ambil jumlah yang cukup dari koloni untuk belajar tanpa menyentuh agar dari mana ia berasal. Koloni mesti segar, iaitu, dari tanaman 18 hingga 24 jam.
Letakkan koloni pada pemegang kering dan di atasnya tambahkan setitik 3% hidrogen peroksida (anda juga boleh menggunakan h2Sama ada2 pada 30%). Perhatikan dengan segera jika gelembung terpisah atau tidak.
Tafsiran
Reaksi Positif: Detasmen Gas, yang terbukti dengan pembentukan gelembung (gelembung kuat).
Reaksi negatif: tidak ada pembentukan gelembung.
-Kaedah Langsung dalam Budaya Murni
Letakkan 1 ml H2Sama ada2 3% pada tanaman tulen dalam plat atau baji yang tidak mengandungi darah (lebih baik cengkaman berkhasiat). Perhatikan sama ada atau tidak ada pembentukan gelembung dengan segera. Anda juga boleh menggunakan h2Sama ada2 30%.
Ia ditafsirkan seperti kaedah pemegang objek.
-Kaedah dengan tiub kapilari atau kulat dan petrishko
Isi tiub kapilari 67 mm pada ketinggian 20 mm dengan 3% hidrogen peroksida setiap kapilariti.
Sentuh koloni terpencil yang ingin anda pelajari dengan kapilari penuh h2Sama ada2 3%. Perhatikan jika kapilari dipenuhi dengan gelembung dalam kira -kira 10 saat. Kaedah ini membolehkan untuk menyesuaikan reaksi di salib:
Tanpa salib tidak ada gelembung (reaksi negatif).
Boleh melayani anda: Flora dan Fauna Kepulauan Falkland: Spesies Cemerlang+ --Gelembung yang terhad (tindak balas yang lemah atau tertunda).
++ -Gelembung yang banyak (tindak balas sederhana).
+++ -Gelembung mencapai hujung yang bertentangan (tindak balas bertenaga).
-Kaedah Taylor dan Achanzar untuk ujian catalase yang memberi ragu -ragu
Dalam slaid yang bersih dan kering diletakkan koloni terpencil, kemudian letakkan set setitik h2Sama ada2 0.5% dan tutup dengan penutup. Perhatikan sama ada atau tidak ada pembentukan gelembung yang dipenjarakan.
Tafsiran: Kehadiran gelembung menunjukkan reaksi positif. Tanpa gelembung, ia ditafsirkan sebagai tindak balas negatif.
Ujian catalase untuk spesies mycobacterium
Teknik ini perlu dilakukan dengan mengawal pH dan suhu. Ia mesti dilaksanakan di bawah loceng aliran laminar, kerana manipulasi spesies mycobacterium yang berlainan berbahaya.
-Bahan
30% atau 110 Jumlah hidrogen peroksida (superoxal).
Fosfat penampan ph 7
Tween 80 hingga 10%
Budaya Mycobacterium dalam baji dari 3 hingga 4 minggu
-Penyediaan dari reagen
Fosfat penampan ph 7
Timbang:
1,361 g (KH2PO4) Anhydra.
1,420 g (Na2HPO3) fosfat disodik anhydrous.
Larutkan kedua -dua garam dalam sedikit air suling steril dan lengkap dengan air sehingga 1000 ml.
Tween 80 hingga 10%
Lakukan pencairan 1:10 ke tween 80 yang datang secara komersial, untuk ini meneruskan seperti berikut:
Ambil 1 ml Tween 80 dan letakkan di dalam air sulingan sedikit, larut dan kemudian lengkapkan jumlah dengan air sehingga 10 ml.
Reagen Akhir
Campurkan jumlah penampan fosfat dengan jumlah tween 80 hingga 10% (di bahagian yang sama). Tentukan di makmal berapa banyak yang anda mahu sediakan.
-Prosedur
Letakkan 5 ml penampan fosfat dalam tiub ujian steril dengan tudung benang (Baquelita).
Dengan pemegang inokulasi, ambil jajahan cukup pertumbuhan Mycobacterium yang disemai dalam baji dan larut dalam penampan fosfat.
Tutup tiub tanpa mengetatkan utas. Letakkan di bilik mandi pada suhu 68 ° C selama 20 hingga 30 minit. Keluarkan dan sejuk pada 22-25 ° C
Ukur 0.5 ml reagen akhir (campuran) dan masukkannya ke tiub dengan penyelesaian sejuk. Perhatikan atau tidak pembentukan gelembung.
Ia ditafsirkan serta teknik sebelumnya.
Gunakan
Apabila pertumbuhan koloni dalam media diperkaya diperoleh, pewarnaan gram dan ujian catalase mesti dijalankan ke koloni yang diperoleh. Ini akan membimbing ahli mikrobiologi mengenai prosedur yang harus diikuti untuk pengenalan muktamad.
Boleh melayani anda: epitel rata sederhana: ciri, fungsi dan jenis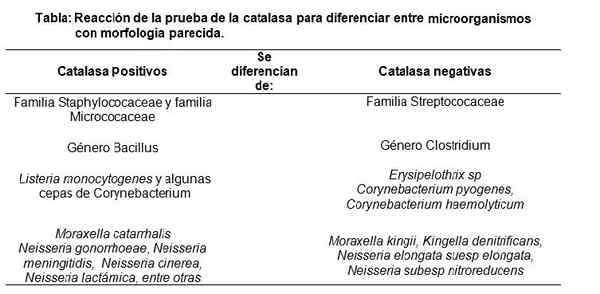 Sumber: Disediakan oleh pengarang MSC. Marielsa Gil
Sumber: Disediakan oleh pengarang MSC. Marielsa Gil QA
Untuk menilai fungsi reagen hidrogen peroksida yang betul, gunakan kawalan yang baru ditanam, seperti Staphylococcus aureus sebagai kawalan positif dan strain Streptococcus sp sebagai kawalan negatif.
Alternatif lain yang berfungsi sebagai kawalan positif adalah meletakkan setitik hidrogen peroksida pada agar darah, erythrocytes mempunyai catalase, oleh itu, akan ada menggelegak jika reagen berada dalam keadaan baik.
Anda boleh menggunakan agar coklat sebagai kawalan negatif, di sini erythrocytes sudah disenaraikan dan ujian memberi negatif.
Batasan
-Jangan gunakan tanaman lama untuk ujian, kerana ini boleh menyebabkan negatif palsu.
-Elakkan mengambil koloni dari tanaman dalam agar darah, jika anda berhati -hati untuk tidak menyentuh agar; Prosedur ini boleh menyebabkan positif palsu, kerana erythrocytes mengandungi catalase.
-Sekiranya anda mengambil tanah jajahan dengan pemegang platinum, jangan melabur perintah prosedur kerana ini dapat menghasilkan positif palsu. Ini kerana platinum dapat bertindak balas dengan hidrogen peroksida, yang berasal dari gelembung.
-Jangan gunakan reagen hidrogen peroksida jika ia sangat tua, kerana reagen sangat tidak stabil dan cenderung rosak dari masa ke masa.
-Pastikan reagen hidrogen peroksida dilindungi dari cahaya dan penyejukan untuk mengelakkan kerosakan.
-Lakukan kawalan kualiti ke reagen hidrogen peroksida setiap kali ia digunakan.
-Ambil perhatian bahawa jika h digunakan2Sama ada2 Pada 30% reaksi lebih kuat daripada yang dilakukan dengan H2Sama ada2 3%.
Rujukan
- Koneman E, Allen S, Janda W, Schreckenberger P, Winn W. (2004). Diagnosis mikrobiologi. Edisi ke -5. Pan -American Editorial S.Ke. Argentina.
- Forbes B, Sahm D, Weissfeld A. (2009). Diagnosis Mikrobiologi Bailey & Scott. 12 ed. Pan -American Editorial S.Ke. Argentina.
- Mac Faddin J. (2003). Ujian biokimia untuk mengenal pasti bakteria kepentingan klinikal. Edisi ke -3. Pan -American Editorial. Buenos Aires. Argentina.
- Makmal BD. Reagen Catalase. Terdapat di: http: // winklerltda.Cl
- Makmal Vadequímica. Hidrogen peroksida. Kesetaraan antara jumlah dan peratusan. Terdapat di: Vadequimica.com

