Tindak balas penggantian ganda
- 676
- 165
- Delbert Dare
Kami menerangkan reaksi penggantian berganda, jenis yang ada dan memberikan beberapa contoh
Apakah tindak balas penggantian berganda?
The tindak balas penggantian ganda, anjakan atau metesis berganda, ia adalah satu di mana pertukaran ion dua kali berlaku di antara dua sebatian, tanpa mana -mana yang dioksidakan atau dikurangkan. Ia merupakan salah satu tindak balas kimia yang paling asas.
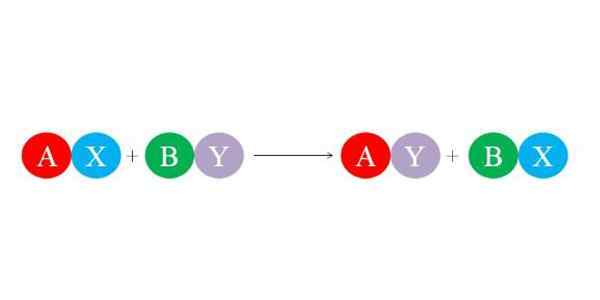
Pautan baru dibentuk oleh daya tarikan elektrostatik yang hebat di antara ion. Begitu juga, tindak balas memihak kepada pembentukan spesies yang paling stabil, seperti molekul air, terutamanya. Dalam imej yang lebih rendah, persamaan kimia umum untuk tindak balas penggantian berganda digambarkan.

Sebatian awal kapak dan dengan bertindak balas dengan bertukar "rakan kongsi mereka" dan dengan itu membentuk dua sebatian baru: ay dan bx. Tindak balas ini berjalan jika dan hanya jika E dan lebih berkaitan daripada A dan B, atau jika pautan BX lebih stabil daripada yang oleh oleh. Oleh kerana reaksi adalah pertukaran ion mudah, tidak ada yang menang atau kehilangan elektron (reaksi redoks).
Oleh itu, jika A adalah kation beban +1 dalam sebatian kapak, ia akan mempunyai beban yang sama +1 dalam sebatian ay. Perkara yang sama berlaku untuk selebihnya "huruf". Tindak balas jenis ini adalah sokongan reaksi pembentukan asid dan precipitous.
Jenis tindak balas penggantian berganda
Peneutralan
Asid kuat bertindak balas dengan asas yang kuat untuk menghasilkan garam dan air larut. Apabila salah satu daripada dua - asid atau asas - lemah, garam yang dihasilkan tidak sepenuhnya terionisasi; iaitu, dalam medium berair yang mampu menghidrolisis. Begitu juga, asid atau asas dapat dinetralkan dengan garam.
Boleh melayani anda: Beryl Oxide (Beeo)Di atas boleh diwakili semula dengan persamaan kimia dengan huruf axby. Walau bagaimanapun, kerana keasidan Brønsted hanya ditunjukkan oleh ion H+ Dan oh-, Ini datang untuk mewakili huruf kepada e y:
Hx + boh => hoh + bx
Persamaan kimia ini sepadan dengan peneutralan, yang hanya reaksi antara asid Hx dan asas BOH untuk menghasilkan HOH (h (h2O) dan garam bx, yang mungkin larut atau tidak di dalam air.
Kerangka anda mungkin berbeza mengikut pekali stoikiometrik atau sifat asid (sama ada organik atau bukan organik).
Hujan
Dalam tindak balas jenis ini, salah satu produk tidak larut di tengah, umumnya berair, dan precipitates (sedimen pepejal sisa penyelesaiannya).
Skim ini adalah seperti berikut: Dua sebatian larut, kapak dan oleh, dan salah satu produk, ay atau bx, mendakan, yang bergantung kepada peraturan kelarutan:
Kapak + by => ay (s) + bx
Kapak + by => ay + bx (s)
Sekiranya kedua -dua AY dan BX tidak larut dalam air, ia akan menimbulkan sepasang ion yang membentangkan interaksi elektrostatik yang paling kuat, yang dapat dicerminkan secara kuantitatif dalam nilai malar kelarutannya (KPS).
Walau bagaimanapun, dalam kebanyakan tindak balas hujan, garam larut dan yang lain mendakan. Kedua -dua tindak balas - peneutralan dan pemendakan - boleh berlaku dalam campuran bahan yang sama.
Contoh tindak balas penggantian berganda
Contoh 1
HCl (AC) + NaOH (AC) => H2Atau (l) + naCl (ac)
Apa jenis reaksi ini? Asid hidroklorik bertindak balas dengan natrium hidroksida menjana air dan natrium klorida akibatnya. Kerana NaCl sangat larut dalam medium berair, dan molekul air juga terbentuk, reaksi Contoh 1 adalah penetapan.
Boleh melayani anda: benzena: sejarah, struktur, sifat, derivatif, kegunaanContoh 2
Setem3)2(Ac) + na2S (ac) => cus (s) + 2nano3(Ac)
Dalam reaksi ini mereka tidak hadir walaupun ion h+ Bahkan OH-, Dan juga molekul air di sebelah kanan persamaan kimia.
Nitrat tembaga (ii), atau nitrat cuprik, pertukaran ion dengan natrium sulfida. Sulfida tembaga tidak larut, precipitating tidak seperti natrium nitrat, garam larut.
Penyelesaian Cu (tidak3)2 Itu kebiruan, sementara na2S adalah kekuningan. Apabila kedua -duanya bercampur, warna -warna hilang dan cus precipitates, yang merupakan kegelapan.
Contoh 3
Ch3COOH (AC) + NaOH (AC) => CH3Poon (ac) + h2Atau (l)
Sekali lagi, ini adalah reaksi peneutralan yang lain. Asid asetik bertindak balas dengan natrium hidroksida untuk membentuk garam natrium asetat dan molekul air.
Tidak seperti Contoh 1, natrium asetat bukan garam yang benar -benar terionisasi, kerana anion dihidrolisis:
Ch3COO-(Ac) + h2Atau (l) cho3COOH (AC) + OH-(Ac)
Contoh 4
2hi (ac) + Caco3(s) => h2Co3(ac) + cai2(Ac)
Dalam tindak balas ini - yang walaupun ia tidak kelihatan sebagai peneutralan - asid iarhydric bertindak balas sepenuhnya dengan batu kapur untuk menghasilkan asid karbonik dan kalsium iodida. Di samping itu, detasmen haba (tindak balas eksotermik) mengurai asid karbonik dalam karbon dioksida dan air:
H2Co3(ac) => co2(g) + h2Atau (l)
Reaksi global kekal:
2hi (ac) + Caco3(s) => co2(g) + h2Atau (l) + cai2(Ac)
Begitu juga, kalsium karbonat, garam asas, meneutralkan asid iarchloric.
Contoh 5
Agno3(ac) + NaCl (ac) => Agcl (s) + nano3(Ac)
Boleh melayani anda: putrescina: struktur, sifat, sintesis, kegunaanIon pertukaran nitrat perak dengan natrium klorida, dengan itu membentuk garam klorida perak yang tidak larut (mendakan putih) dan natrium nitrat.
Contoh 6
2h3PO4(Ac) + 3ca (OH)2(Ac) => 6H2Atau (l) + ca3(PO4)2(S)
Asid fosforik dinetralkan oleh kalsium hidroksida, akibatnya membentuk garam fosfat kalsium yang tidak larut dan enam tahi lalat molekul air.
Ini adalah contoh tindak balas penggantian berganda kedua -dua jenis: peneutralan asid dan pemendakan garam yang tidak larut.
Contoh 7
K2S (ac) + mgso4(ac) => k2SW4(ac) + mgs (s)
Potassium sulfida bertindak balas dengan magnesium sulfat, berkumpul dalam penyelesaian s ion2- dan mg2+ Untuk membentuk magnesium sulfida dan garam larut dalam sulfat.
Contoh 8
Na2S (ac) + hcl (ac) → naCl (ac) + h2S (g)
Natrium sulfida meneutralkan asid hidroklorik, menghasilkan natrium klorida dan hidrogen sulfida.
Dalam tindak balas ini, air tidak terbentuk (tidak seperti neutralizations yang paling biasa) tetapi molekul non -elektrolitik hidrogen sulfida, yang bau telur busuk sangat tidak menyenangkan. H2S melarikan diri penyelesaian dalam bentuk gas dan selebihnya spesies tetap dibubarkan.

