Reaksi eksotermik
- 1734
- 270
- Mr. Tracy Parisian
Kami menerangkan reaksi eksotermik, ciri -ciri mereka, perbezaan dengan reaksi endotermik dan memberi beberapa contoh
Apakah reaksi eksotermik?
The Reaksi eksotermik Mereka adalah tindak balas kimia yang melepaskan tenaga dalam bentuk haba. Perkataan eksotermik dibentuk oleh "Exo" yang bermaksud "keluar", dan "Thermos" yang bermaksud haba, jadi "reaksi eksotermik" secara harfiah bermakna, tindak balas di mana haba keluar.
Reaksi ini sangat biasa dan kita dapat mencari mereka di mana -mana, dari rumah kita ke sel yang merupakan sebahagian daripada badan kita.
Di rumah kita dapat menjumpainya di dapur ketika gas terbakar di tanduk untuk memasak makanan kita. Kami juga mendapati mereka di dalam enjin kereta ketika mereka membakar bahan api.
 Contoh tindak balas eksotermik
Contoh tindak balas eksotermik Sebaliknya, tindak balas eksotermik adalah penting untuk kehidupan, kerana mereka menyediakan sel -sel dengan tenaga yang mereka perlukan untuk hidup, berkembang dan menghasilkan semula.
Ciri -ciri tindak balas eksotermik
Mereka melepaskan tenaga dalam bentuk panas
Ini adalah ciri utama yang menjadikan mereka reaksi eksotermik.
Tenaga yang dikeluarkan berasal dari reagen yang sama
Setiap tindak balas kimia memerlukan beberapa tenaga pengaktifan berlaku. Sekiranya berlaku tindak balas eksotermik, tenaga ini berasal dari reagen yang sama apabila berubah menjadi produk.
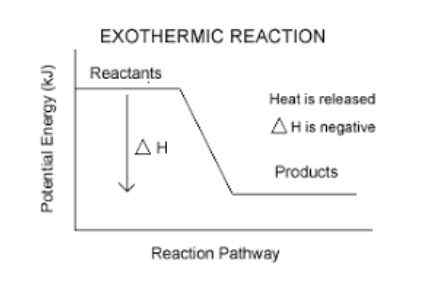
Produk reaksi eksotermik sentiasa lebih stabil daripada reagen.
Reagen dengan menjadi produk, kehilangan sebahagian daripada tenaga mereka dalam bentuk haba. Atas sebab ini, produk sentiasa kekal dengan tenaga yang kurang daripada reagen, yang menjadikannya lebih stabil.
Mereka mempunyai variasi entalpi negatif.
Ini adalah cara mudah untuk mengetahui sama ada tindak balas adalah eksotermik atau tidak. Sebarang tindak balas yang mempunyai negatif AH (baca delta h), akan menjadi eksotermik.
- Sebagai contoh, Reaksi pembakaran butana (gas yang kita terbakar di dapur) mempunyai variasi entalpi -11.823 kcal/mol. Oleh itu, ia adalah reaksi eksotermik.
Mereka hanya memerlukan pencetus untuk berlaku dalam kebanyakan kes.
Banyak reaksi eksotermik hanya memerlukan sesuatu yang memberi mereka tenaga yang cukup untuk bermula. Selepas ini, haba yang sama yang mereka lepaskan sudah cukup untuk memastikan reaksi berjalan.
- Sebagai contoh, Dengan membakar gas, hanya satu percikan diperlukan, maka api terus menghidupkan sehingga gas berakhir.
Perbezaan antara tindak balas eksotermik dan tindak balas endotermik
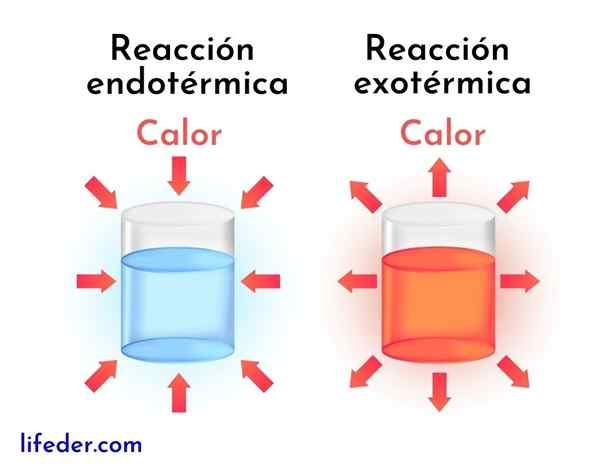
Reaksi eksotermik adalah bertentangan dengan tindak balas endotermik. Pada yang terakhir, reagen menyerap tenaga dalam bentuk haba dan bukannya melepaskannya, seperti dalam reaksi eksotermik.
Seterusnya, perbezaan utama antara tindak balas eksotermik dan endotermik dibentangkan:
Reaksi eksotermik | Reaksi endotermik |
Mereka melepaskan tenaga dalam bentuk panas. | Mereka menyerap tenaga dalam bentuk panas. |
Mereka mempunyai variasi entalpi negatif, iaitu DH<0. | Mereka mempunyai variasi entalpi positif, iaitu dh> 0. |
Mereka cenderung meningkatkan suhu sekitar. | Mereka cenderung mengurangkan suhu atau sejuk. |
Tenaga yang membuat reaksi berjalan dari reagen yang sama. | Tenaga yang membuat reaksi berjalan dari persekitaran. |
Lebih banyak produk yang stabil selalu diperoleh dengan tenaga yang kurang. | Produk yang kurang stabil selalu diperoleh dengan tahap tenaga yang lebih tinggi. |
Contoh tindak balas eksotermik
Pembakaran gas dapur
Di kebanyakan rumah di dunia, gas yang digunakan untuk memasak makanan adalah butana, yang mempunyai formula molekul c4H10. Hidrokarbon ini dibakar dengan oksigen udara melalui tindak balas pembakaran seterusnya yang melepaskan sejumlah besar haba:
Boleh melayani anda: mikroskop sederhana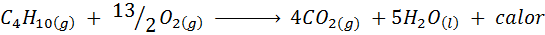
Letupan dinamit
Dynamite mengandungi letupan yang disebut nitrogliserin (c3H5N3Sama ada9). Kompaun ini terurai dengan sangat keras melepaskan sejumlah besar haba, yang menyebabkan letupan hebat. Tindak balas kimia adalah:
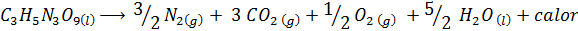
Reaksi ini mempunyai ΔH = -368 kcal / mol, Jadi itu adalah reaksi eksotermik.
Pembakaran spontan fosforus putih
Unsur fosforus (P) boleh didapati sebagai fosforus merah atau fosforus putih. Fosfor putih. Tindak balasnya adalah:
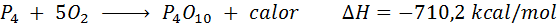
Pernafasan selular
Pernafasan selular adalah tindak balas kimia eksotermik yang terdiri daripada pengoksidaan makanan yang kita makan. Haba yang dikeluarkan oleh tindak balas ini digunakan oleh sel untuk menjalankan tindak balas kimia endotermik yang tidak berkesudahan yang memerlukan tenaga berlaku.
Bunga api
Bunga api mengandungi serbuk mesiu hitam sebagai komponen letupan utama. Serbuk mesiu adalah campuran yang mengandungi potassium nitrat, grafit dan karbon sulfur yang bertindak balas antara satu sama lain melalui reaksi eksotermik. Haba yang disiarkan tindak balas ini, menghasilkan pelbagai warna yang kita lihat di syurga ketika bunga api meletup.
Pad termal kimia
Pad haba digunakan sebagai pemampatan panas untuk melegakan kecederaan sukan. Ini terdiri daripada beg tertutup yang mengandungi air dan ahli kimia di dalam tiub kecil. Apabila tiub rosak, ahli kimia bercampur dengan air yang menghasilkan tindak balas kimia eksotermik yang memanaskan pad.
Tindak balas natrium logam dengan air
Natrium (NA) adalah logam alkali yang sangat reaktif yang apabila bersentuhan dengan air bertindak balas dengan ganas melepaskan banyak haba dan hidrogen gas. Tindak balasnya adalah:
Ia dapat melayani anda: Kaedah pemisahan campuran heterogen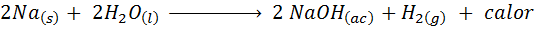
Reaksi ini mengeluarkan 1900 kalori untuk setiap gram NA yang bertindak balas dengan air. Ini bermaksud bahawa 1 gram natrium cukup untuk memanaskan 3 cawan kopi sederhana.
Pembubaran Detergen
Ini adalah tindak balas yang boleh dialami oleh sesiapa di rumah mereka. Semasa mengambil beberapa detergen debu untuk mencuci pakaian dan basah dengan sedikit air, tangan akan segera terasa panas. Ini kerana proses pembubaran detergen dalam air adalah eksotermik.
Reaksi Trimita
Termita adalah campuran aluminium dalam bentuk serbuk yang sangat halus dan oksida logam lain seperti besi. Selepas percikan, tindak balas yang berlaku adalah:
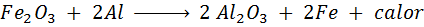
Reaksi ini mengeluarkan banyak haba, yang mampu mencairkan besi dan banyak digunakan untuk mengimpal kereta api.
Pemeluwapan air
Untuk semua bahan, perubahan fasa gas (pemeluwapan), cecair ke pepejal (pemejalan) dan gas pepejal (pemendapan), selalu melepaskan haba dan oleh itu adalah proses eksotermik. Dalam kes air, pemeluwapan hanya 18 gram air mengeluarkan kira -kira 10.000 kalori, yang cukup untuk memanaskan 15 cawan kopi kecil.
Rujukan
- Chang, R. dan Goldsby, k. (2014). Kimia. Edisi ke -11. New York: Pendidikan McGraw-Hill.
- Reaksi Exothermic (2020, 19 Disember). Di Wikipedia. Diambil daripada.Wikipedia.org
- Holmes, w. S. (1963). Haba pembakaran fosforus dan enthalpies pembentukan P4O10 dan H3PO4. Faraday Soc. 58. 1916-1925. Doi: 10.1039/TF9625801916.
- Prada p. dari., F. Yo. (2014). Mercun, roket dan banyak kimia. Pendidikan Kimia. 44-51. Doi: 10.2436/20.2003.02.134
- Reaksi Thermite. Universiti Minnesota (Jabatan Kimia). Diambil dari chem.Umn.Edu

