Penemuan, sifat, struktur, kegunaan renio

- 5077
- 965
- Ms. Micheal Rippin
Dia Renio Ia adalah elemen logam yang simbol kimianya, dan terletak di Kumpulan 7 jadual berkala, dua kedudukan di bawah mangan. Kongsi dengan pemilikan ini dan Technecio bagi pelbagai nombor atau keadaan pengoksidaan, dari +1 hingga +7. Juga, membentuk anion yang dipanggil perrenato, banduan4-, Analogi dengan permanganat, MNO4-.
Logam ini adalah salah satu yang paling jarang dan jarang berlaku, jadi harganya tinggi. Ia diekstrak sebagai hasil sampingan molibdenum dan perlombongan tembaga. Salah satu sifat Renio yang paling relevan adalah titik lebur yang tinggi, hampir tidak diatasi oleh karbon dan tungsten, dan ketumpatannya yang besar, yang dua kali ganda memimpin.
 Renio Metal Sphere. Sumber: Hi-Res Imej Elemen Kimia/CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0)
Renio Metal Sphere. Sumber: Hi-Res Imej Elemen Kimia/CC oleh (https: // creativeCommons.Org/lesen/oleh/3.0) Penemuannya mempunyai nuansa yang kontroversial dan malang. Nama 'Renio' berasal dari perkataan Latin 'Rhenus', yang bermaksud Rin, sungai Jerman yang terkenal berhampiran tapak di mana ahli kimia Jerman yang mengasingkan dan mengenal pasti unsur baru ini bekerja.
Renio mempunyai banyak kegunaan, di antaranya penghalusan oktana petrol berdiri.
[TOC]
Penemuan
Kewujudan dua elemen berat dengan ciri -ciri kimia yang serupa dengan mangan telah meramalkan sejak tahun 1869, melalui jadual berkala Dmitri Mendeleev berkala. Walau bagaimanapun, ia tidak diketahui oleh itu nombor atom mereka; Dan di sini pada tahun 1913 ketika ramalan ahli fizik Inggeris Henry Moseley diperkenalkan.
Menurut Moseley, kedua -dua elemen ini milik kumpulan mangan mesti mempunyai nombor atom 43 dan 75.
Walau bagaimanapun, beberapa tahun sebelum ini, ahli kimia Jepun Masataka Ogawa telah menemui unsur yang dikatakan 43 dalam sampel torianita mineral. Selepas mengumumkan keputusannya pada tahun 1908, dia mahu membaptiskan elemen ini dengan nama 'Niponio'. Malangnya, ahli kimia pada masa itu menunjukkan bahawa Ogawa tidak menemui elemen 43.
Ia boleh melayani anda: Cycloalques: Struktur Kimia, Sifat, TatanamaDan sebagainya, tahun -tahun lain berlalu ketika pada tahun 1925 tiga ahli kimia Jerman: Walter Noddack, Ida Noddack, dan Otto Berg, mendapati elemen 75 di Columbita, Gadolinite dan Molybdenite Sampel Mineral. Ini memberinya nama Renio, sebagai penghormatan kepada Rin Rin of Jerman ('Rhenus', dalam bahasa Latin).
Kesalahan Masataka Ogawa adalah untuk disace offced dalam pengenalan elemen: dia telah menemui Renio, bukan elemen 43, yang dipanggil Tecnecio hari ini.
Renio Properties
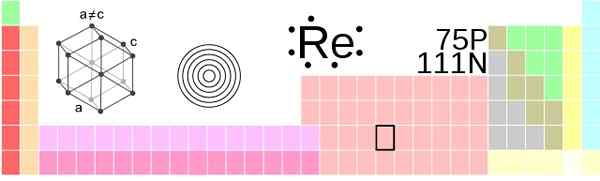 Keadaan renio dalam jadual berkala. !Asal: AhoteseerVector: Sushant Savla/CC BY-S (https: // creativeCommons.Org/lesen/by-sa/3.0)
Keadaan renio dalam jadual berkala. !Asal: AhoteseerVector: Sushant Savla/CC BY-S (https: // creativeCommons.Org/lesen/by-sa/3.0) Penampilan fizikal
Renio biasanya dipasarkan dalam bentuk habuk kelabu. Kepingan logamnya, biasanya titisan sfera, kelabu perak, yang juga sangat terang.
Jisim molar
186,207 g/mol
Nombor atom
75
Takat lebur
3186 ºC
Takat didih
5630 ºC
Ketumpatan
-Pada suhu bilik: 21.02 g/cm3
-Betul -betul di titik lebur: 18.9 g/cm3
Renio adalah logam yang hampir dua kali lebih padat daripada yang sama. Oleh itu, sfera renio yang beratnya 1 gram dapat disamakan dengan kristal plumbum yang mantap dari jisim yang sama.
Elektronegativiti
1.9 pada skala Pauling
Tenaga pengionan
Pertama: 760 kJ/mol
Kedua: 1260 kJ/mol
Ketiga: 2510 kJ/mol
Kapasiti haba molar
25.48 j/(mol · k)
Kekonduksian terma
48.0 w/(m · k)
Resistiviti elektrik
193 nΩ · m
Kekerasan mohs
7
Isotop
Atom Renio dibentangkan sebagai dua isotop: 185Re, dengan banyaknya 37.4%; dan 187Re, dengan banyaknya 62.6%. Renio adalah salah satu daripada unsur -unsur yang paling banyak isotop adalah radioaktif; Walau bagaimanapun, masa separuh kehidupan 187Re sangat besar (4.12 · 1010 tahun), jadi praktikal dianggap stabil.
Boleh melayani anda: nikel: sejarah, sifat, struktur, kegunaan, risikoReaktiviti
Renio logam adalah tahan bahan untuk mengoksidakan. Apabila dia melakukannya, oksida, semula2Sama ada7, Ia volatilisasi pada suhu tinggi dan terbakar dengan api hijau kekuningan. Potongan Renio menentang serangan Hno3 tertumpu; Tetapi panas, larut untuk menghasilkan asid renik dan nitrogen dioksida, yang berwarna coklat penyelesaian:
Re + 7hno3 → Hreo4 + 7 tidak2 + 3h2Sama ada
Kimia Renio luas, kerana ia dapat membentuk sebatian dengan spektrum luas pengoksidaan, serta menubuhkan ikatan quadrupolo antara dua atom renio (empat ikatan kovalen semula).
Struktur dan konfigurasi elektronik
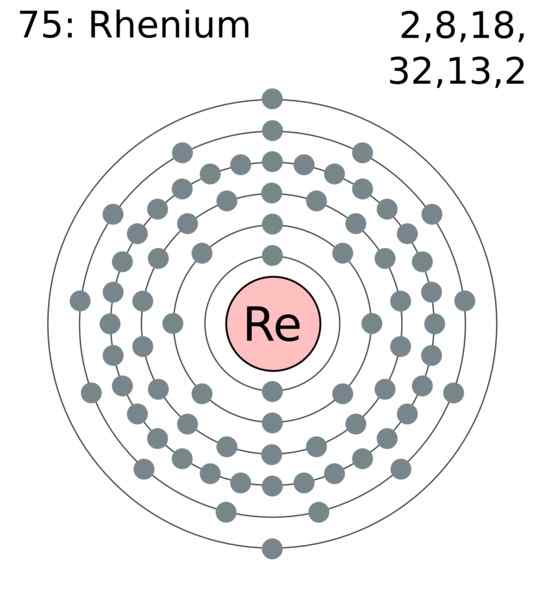 Lapisan elektron renio. Pengarang: Pengguna: Gregrobson (Greg Robson). Wikimedia Commons
Lapisan elektron renio. Pengarang: Pengguna: Gregrobson (Greg Robson). Wikimedia Commons Atom Renio dikelompokkan ke dalam kristal mereka untuk menyebabkan struktur heksagon padat, HCP, yang dicirikan dengan sangat padat. Ini bersetuju dengan fakta menjadi logam yang mempunyai ketumpatan yang hebat. Pautan logam, produk pertindihan orbital luarannya, mengekalkan atom -atom yang sangat kohesif.
Dalam pautan logam ini, Re-re, elektron Valencia mengambil bahagian, yang menurut konfigurasi elektronik:
[Xe] 4f14 5 d5 6s2
Pada dasarnya, orbital 5d dan 6s yang bertindih untuk memadatkan atom RE dalam struktur HCP. Perhatikan bahawa elektron anda menambah sejumlah 7, sepadan dengan nombor kumpulan anda dalam jadual berkala.
Nombor pengoksidaan
Konfigurasi elektronik renio sekali melihat bahawa atomnya mampu kehilangan sehingga 7 elektron, untuk menjadi kation hipotesis semula7+. Apabila kewujudan RE diandaikan7+ Di mana -mana sebatian renio, sebagai contoh, dalam re2Sama ada7 (Re27+Sama ada72-), Dikatakan bahawa ia mempunyai bilangan pengoksidaan +7, semula (vii).
Nombor pengoksidaan positif lain untuk renio adalah: +1 (semula+), +2 (semula2+), +3 (semula3+), Dan sebagainya ke +7. Begitu juga, Renio dapat memperoleh elektron menjadi anion. Dalam kes ini, dikatakan bahawa ia mempunyai nombor pengoksidaan negatif: -3 (semula3-), -2 (semula2-) dan -1 (semula-).
Ia dapat melayani anda: hidrolisis: apa itu dan contoh reaksiAplikasi
Petrol
Renio, bersama -sama dengan platinum, digunakan untuk membuat pemangkin yang meningkatkan tahap oktana petrol, sambil mengurangkan kandungannya. Sebaliknya, pemangkin renio ditakdirkan untuk pelbagai tindak balas hidrogenasi, ini disebabkan oleh penentangan mereka terhadap keracunan nitrogen, fosforus dan sulfur.
Superleations refraktori
Renio adalah produk logam refraktori titik lebur yang tinggi. Itulah sebabnya aloi nikel ditambah untuk menjadikan mereka tahan api dan tahan terhadap tekanan dan suhu yang besar. Superleations ini kebanyakannya digunakan untuk reka bentuk turbin dan enjin untuk kapal aeroangkasa.
Filamen tungsten
Renio juga boleh membentuk aloi dengan tungsten, yang meningkatkan kemulurannya dan, oleh itu, memudahkan pembuatan filamen. Filamen renio-tungsten ini digunakan sebagai sumber sinar-X, dan untuk reka bentuk termosupla yang mampu mengukur suhu sehingga 2200 ° C.
Begitu juga, filamen renio ini digunakan sekali untuk kamera kuno berkedip, dan kini untuk lampu peralatan yang canggih; seperti spektrofotometer massa.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Sarah Pierce. (2020). Rhenium: Penggunaan, Sejarah, Fakta & Isotop. Kajian. Pulih dari: belajar.com
- Pusat Kebangsaan Maklumat Bioteknologi. (2020). Rhenium. Pangkalan data PUBCHEM., CID = 23947. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Wikipedia. (2020). Rhenium. Diperoleh dari: dalam.Wikipedia.org
- Dr. Doug Stewart. (2020). Fakta Elemen Rhenium. Pulih dari: chemicool.com
- Eric Scerri. (18 November 2008). Rhenium. Kimia dalam elemennya. Pulih dari: dunia kimia.com

