Penyelesaian kimia
- 4545
- 18
- Dallas Bernhard
Kami menerangkan penyelesaian kimia, ciri -ciri mereka, jenis yang ada dan memberikan beberapa contoh
 Bahan kimia adalah campuran homogen antara dua bahan
Bahan kimia adalah campuran homogen antara dua bahan Apakah penyelesaian kimia?
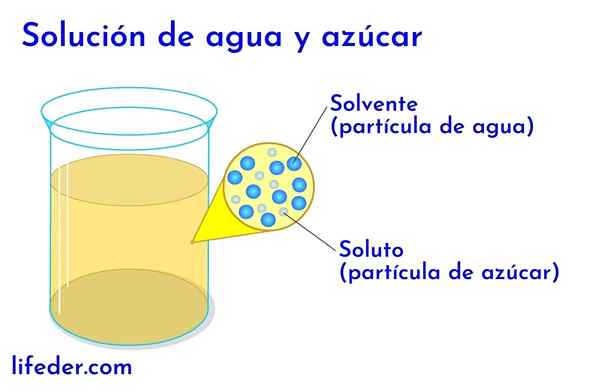
The Penyelesaian kimia Mereka adalah campuran homogen antara pelarut dan satu atau lebih larutan. Penyelesaian yang paling mudah dibentuk oleh pelarut tunggal dan pelarut, seperti ketika kita membubarkan gula di dalam air, tetapi ada penyelesaian yang dapat menjadi sangat kompleks dengan beratus -ratus larutan.
Penyelesaian yang paling biasa adalah dalam keadaan cair, dan dalam kebanyakan kes pelarut adalah air. Atas sebab ini, air biasanya dipanggil "pelarut sejagat". Tetapi penyelesaiannya tidak terhad kepada cecair, kerana terdapat penyelesaian dalam keadaan gas dan pepejal.
Pelarut juga boleh didapati di negeri yang berbeza. Sebagai contoh, penyelesaian cecair dengan larutan pepejal (seperti garam), cecair (seperti alkohol) atau gas (seperti gas karbonik dalam minuman ringan) boleh mempunyai penyelesaian pepejal).
Bagaimana mengenali larutan dan pelarut?
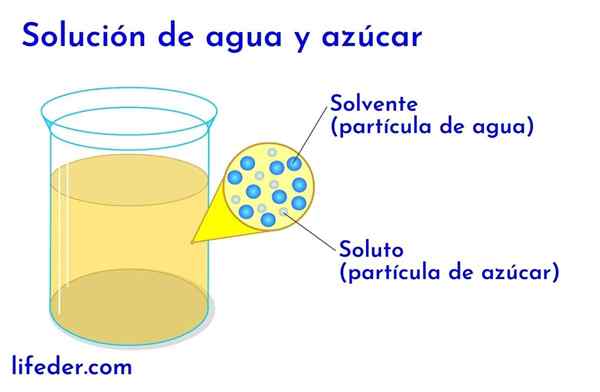 Larut dan pelarut di dalam air dengan gula
Larut dan pelarut di dalam air dengan gula Dalam sebarang penyelesaian di mana terdapat air, ini dianggap sebagai pelarut. Dalam semua kes lain, pelarut sepadan dengan komponen yang mempunyai kuantiti yang lebih besar atau lebih tinggi dan hampir selalu menjadi cecair. Komponen lain yang terdapat dalam penyelesaiannya dianggap sebagai larutan.
Mari lihat dua contoh:
- Dalam larutan air dan gula, air adalah pelarut dan gula larut.
- Alkohol isopropil yang kami beli di farmasi adalah penyelesaian yang dibentuk oleh air dan alkohol. Dalam penyelesaian ini pelarut adalah air walaupun berada dalam bahagian yang lebih kecil daripada alkohol.
Ciri -ciri dan sifat penyelesaian kimia
Mereka adalah campuran homogen
Penyelesaiannya adalah campuran di mana larutan pelarut tidak dapat dibezakan, sama ada ke mata kasar atau dengan penggunaan kaca pembesar atau mikroskop.
Mereka mempunyai komposisi seragam
Ini bermakna bahawa mana -mana bahagian penyelesaian akan sentiasa mempunyai komponen yang sama (larut dan pelarut) dengan kepekatan yang sama.
Boleh melayani anda: kadmium (CD): sejarah, sifat, struktur, kegunaanMereka dicirikan oleh kepekatan mereka
Konsentrasi adalah salah satu ciri yang paling penting dalam penyelesaian, kerana ia menentukan banyak sifatnya.
Mereka lutut (telus)
Penyelesaian cecair mestilah lut, iaitu, cahaya mesti dapat menyeberangi mereka tanpa bersurai.
Mereka stabil
Penyelesaian di mana larutan dan pelarut tidak bertindak balas antara satu sama lain akan stabil selama -lamanya. Ini bermakna ia tidak akan mengalami apa -apa perubahan dari masa ke masa, selagi komposisinya tetap malar (pelarut tidak menguap, sebagai contoh).
Sifat fizikal dan kimianya berbeza dari pelarut
Ciri -ciri fizikal dan kimia perubahan pelarut ketika bercampur dengan larut. Sebagai contoh, penyelesaian mempunyai titik mendidih yang lebih besar, titik lebur yang lebih rendah dan juga mempunyai tekanan osmotik yang tinggi berbanding pelarut tulen.
Mereka boleh dipisahkan melalui beberapa proses fizikal dan kimia
Penyelesaian tidak dapat dipisahkan dengan penapisan, sentrifugasi atau penyingkiran. Mereka hanya boleh dipisahkan oleh kaedah fizikal atau kimia seperti penghabluran, penyulingan, penyejatan, osmosis terbalik dan kromatografi, antara lain.
 Instrumen penyulingan
Instrumen penyulingan Jenis penyelesaian kimia
Penyelesaian kimia boleh diklasifikasikan mengikut kepekatan mereka, mengikut keadaan fizikal mereka dan mengikut sifat pelarut:
Menurut kepekatan anda
- Penyelesaian tak tepu: Mereka adalah orang -orang di mana larutan belum mencapai kepekatan maksimum dalam pelarut. Oleh sebab itu, lebih banyak larutan dapat dibubarkan untuk menyediakan penyelesaian yang lebih pekat.
- Penyelesaian tepu: Mereka adalah penyelesaian di mana pelarut tidak dapat lagi larut. Dalam kes ini selalu ada sebahagian daripada larutan tanpa melarutkan. Contohnya, jika kita menambah banyak garam ke gelas dengan air, sebahagian daripada garam ini tidak akan larut dan tinggal di bahagian bawah kaca.
- Penyelesaian superaturated: Ini adalah penyelesaian di mana terdapat lebih banyak larutan terlarut daripada pelarut yang mengakui. Ini dapat dicapai dengan memanaskan penyelesaian tepu untuk membubarkan lebih banyak larut, dan kemudian meninggalkan perlahan sehingga suhu awal. Penyelesaian ini tidak stabil, kerana sebarang gangguan seperti getaran atau zarah kecil habuk di permukaan boleh menyebabkan pemisahan larut berlebihan.
Menurut keadaan fizikal anda
- Penyelesaian cecair: Mereka adalah yang paling biasa. Dalam penyelesaian jenis ini pelarut adalah cecair (seperti air, alkohol, minyak, dll.) Tetapi larutan boleh didapati di mana -mana negeri (pepejal, cecair atau gas). Beberapa contoh penyelesaian cecair adalah air garam, wain dan minuman ringan.
- Penyelesaian pepejal: Dalam kes ini, kedua -dua pelarut dan larutan berada dalam keadaan pepejal. Contoh yang paling biasa dari jenis penyelesaian ini adalah aloi logam seperti gangsa, keluli dan tembaga, tetapi terdapat juga contoh lain seperti kaca.
- Penyelesaian Gaseous: Seperti namanya, mereka adalah campuran homogen di mana semua komponen berada dalam keadaan gas.
Menurut pelarut
- Penyelesaian berair: Jika dalam penyelesaian pelarut adalah air, maka dikatakan bahawa ia adalah penyelesaian berair. Ini adalah penyelesaian yang paling biasa yang dapat dijumpai dalam kehidupan seharian.
- Penyelesaian alkohol: Pelarut yang paling biasa, selepas air, adalah alkohol. Antara alkohol yang paling biasa ialah metanol, etanol dan isopropil alkohol.
- Penyelesaian dalam pelarut organik lain: Terdapat banyak sebatian organik lain yang digunakan sebagai pelarut. Ini termasuk beberapa alkana, kebanyakan eters, keton cecair dan lain -lain.
Contoh penyelesaian kimia
Lemonade
Ini adalah larutan berair yang dibentuk oleh air sebagai pelarut dan jus lemon dan gula seperti larut.
Air laut
Air laut atau air garam adalah larutan berair yang terdiri daripada air dan campuran garam. Di antara garam ini, yang paling banyak adalah natrium klorida (NaCl) yang dikenali sebagai garam meja biasa.
Boleh melayani anda: Mercury Oxide (HG2O)Sirap pekat
Ini adalah larutan berair hampir tepu dengan air gula.
Air berkarbonat
Air berkarbonat, juga dikenali sebagai soda, adalah penyelesaian berair karbon dioksida gas (CO2) Dalam air.
Udara
Udara adalah penyelesaian gas di mana nitrogen boleh dianggap sebagai pelarut dan oksigen dan gas lain sebagai larutan.
Mentega yang dijelaskan
Dengan mencairkan mentega dan keluarkan semua busa, larutan kuning telus yang disebut mentega dijelaskan diperolehi. Ini adalah penyelesaian di mana kedua -dua pelarut dan larutan adalah lemak.
Kaca berwarna
Kaca warna adalah penyelesaian keadaan pepejal, di mana pelarut adalah silika cair dan larutan adalah mineral lain yang memberikan kaca warna ciri -cirinya.
Kopi
Ini adalah penyelesaian berair yang kompleks yang mengandungi banyak larutan (di antaranya kafein) yang memberikan minuman aroma dan rasa ciri.
Keluli
Keluli adalah penyelesaian aloi atau pepejal yang dibentuk oleh besi dan karbon grafit logam.
Plasma darah
Plasma darah adalah penyelesaian yang diperolehi selepas menyentuh darah untuk menghilangkan semua sel dan pepejal yang digantung lain. Ini adalah larutan berair yang cukup tertumpu yang mengandungi beratus -ratus larutan termasuk karbohidrat, asid amino, protein larut dan elektrolit, antara lain.
Rujukan
- Chang, R. dan Goldsby, k. (2014). Kimia. Edisi ke -11. New York: Pendidikan McGraw-Hill.
- Penyelesaian (25 Januari, 2021). Di Wikipedia.org.
- Coklat, t. L., Lemay, e. (2018). Kimia: Sains Pusat. Edisi ke -14. Pearson.
- Krestonosich, s., dan lain lain. (1992). Penyelesaian. Editorial Miró.
- Vidal, J. Ke. (Editor) (1997). Mentor Interaktif - Ensiklopedia Tema Pelajar. Editorial Ocean. Barcelona.

