Konsep, proses dan contoh sublimasi progresif
- 2367
- 199
- Dallas Bernhard
The Sublimasi Progresif Ini adalah proses termodinamik di mana perubahan keadaan endotermik berlaku secara langsung dari pepejal ke gas, tanpa pembentukan cecair sebelumnya. Tingkah laku pepejal di bawah keadaan normal adalah untuk memanaskan dan mencairkan; iaitu cair. Sementara itu, dalam sublimasi pepejal mula merokok secara langsung, tanpa penampilan titisan yang menunjukkan penempatannya.
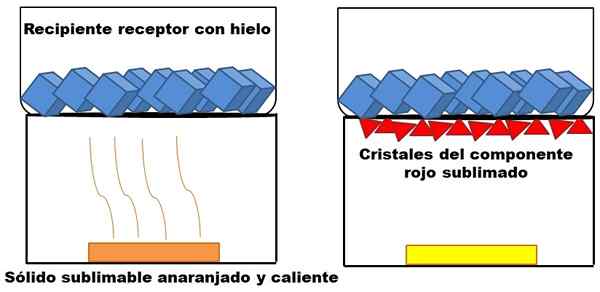
Apa yang diterangkan dalam perenggan teratas diwakili dalam imej yang unggul. Katakan campuran pepejal oren (kiri), yang mula memanaskan. Campuran terdiri daripada dua komponen atau pepejal: satu kuning dan merah yang lain, yang gabungannya menyebabkan warna oren.
 Contoh Sublimasi pepejal oren hipotetikal. Sumber: Gabriel Bolívar.
Contoh Sublimasi pepejal oren hipotetikal. Sumber: Gabriel Bolívar. Pepejal merah sublimal, kerana cecair itu tidak terbentuk tetapi akhirnya didepositkan (segitiga merah) di dasar bekas atas; Yang mengandungi kiub ais, dan oleh itu menawarkan permukaan sejuk. Sementara itu, pepejal kuning kekal tidak berubah oleh haba (segi empat tepat kuning).
Segitiga merah atau kristal disimpan terima kasih kepada permukaan sejuk bekas penerima (kanan), yang menyerap suhunya; Dan walaupun ia tidak ditunjukkan, saiz kiub aisnya mesti berkurangan kerana penyerapan haba. Pepejal kuning tidak dapat disangkal, dan jika dia masih memanaskan lambat laun, dia akan mencairkan.
[TOC]
Konsep Sublimasi Progresif
Proses
Telah dikatakan bahawa sublimasi adalah perubahan keadaan endotermik, kerana agar ia mesti ada penyerapan haba. Jika pepejal menyerap panas tenaga akan meningkat, jadi zarahnya juga akan bergetar pada frekuensi yang lebih besar.
Apabila getaran ini menjadi sangat kuat, mereka akhirnya mempengaruhi interaksi intermolecular (bukan ikatan kovalen); Dan akibatnya, lambat laun zarah akan mengambil lebih banyak jarak antara satu sama lain, sehingga mereka dapat mengalir dan bergerak lebih bebas melalui kawasan ruang.
Boleh melayani anda: penghabluranDalam beberapa pepejal getaran sangat kuat, bahawa sesetengah zarah "dicetuskan" di luar struktur dan bukannya aglomerasi dalam kelompok mudah alih yang menentukan penurunan. Zarah -zarah ini melarikan diri dan mengintegrasikan "gelembung" yang pertama, yang lebih suka membentuk wap pertama pepejal sublimasi.
Ia kemudiannya dituturkan mengenai titik lebur, tetapi dari sublimasi. Walaupun kedua -duanya bergantung kepada tekanan yang memerintah pada pepejal, titik sublimasi lebih banyak; Oleh itu, suhunya berbeza dengan perubahan tekanan (seperti yang berlaku dengan titik mendidih).
Dari struktur pepejal hingga gangguan gas
Dalam sublimasi ia juga dikatakan bahawa terdapat peningkatan entropi sistem. Keadaan tenaga zarah -zarah itu dibatasi oleh kedudukan tetap mereka dalam struktur pepejal, untuk homogenisasi dalam arah mereka yang tidak jelas dan huru -hara dalam keadaan gas, lebih seragam, di mana mereka akhirnya memperoleh tenaga kinetik purata.
Rajah fasa dan titik tiga
Titik sublimasi bergantung kepada tekanan; Kerana sebaliknya, zarah pepejal akan menyerap haba untuk tidak dipecat ke ruang di luar pepejal, tetapi untuk membentuk titisan. Ia tidak akan disahlimasi, tetapi akan mencairkan atau mencairkan, seperti yang paling biasa.
Semakin besar tekanan luaran, semakin kecil kemungkinan sublimasi akan, kerana pepejal untuk cair diwajibkan.
Tetapi pepejal mana yang tidak dapat dipertahankan dan yang tidak? Jawapannya terletak pada rajah fasa p vs t anda, seperti yang ditunjukkan di bawah:
Ia boleh melayani anda: Cruise untuk Crucible: Ciri -ciri, Fungsi, Gunakan Contoh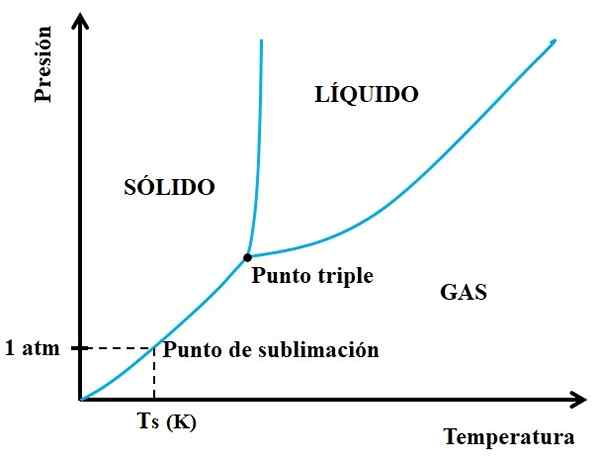 Gambar rajah fasa untuk bahan hipotesis. Sumber: Gabriel Bolívar.
Gambar rajah fasa untuk bahan hipotesis. Sumber: Gabriel Bolívar. Anda perlu melihat pertama di titik tiga dan mengembara peregangan yang lebih rendah: yang memisahkan keadaan pepejal dan gas. Perhatikan bahawa di rantau pepejal, mesti ada penurunan tekanan supaya sublimasi berlaku (tidak semestinya 1 tekanan atmosfera). A atm 1, bahan hipotesis akan sublim akan pada suhu TS yang dinyatakan dalam k.
Semakin lama dan lebih lama bahagian atau lengkung di bawah titik tiga, semakin besar kapasiti pepejal untuk sublim pada suhu yang berbeza; Tetapi jika ia berada di bawah 1 atm, maka ia akan diperlukan dengan jurang yang tinggi untuk mencapai sublimasi, sehingga tekanan dikurangkan (0.0001 atm, sebagai contoh).
Keadaan
Sekiranya titik triple adalah beribu -ribu kali lebih rendah daripada tekanan atmosfera, pepejal tidak akan sublim atau bahkan menggunakan ultra -life (belum lagi kerentanannya untuk mengurai dengan tindakan panas).
Sekiranya ini tidak berlaku, sublimasi dilakukan dengan sederhana, dan mengemukakan pepejal kepada vakum supaya zarah mereka melarikan diri dengan lebih mudah, tanpa memerlukan penyerap banyak haba.
Sublimation menjadi sangat penting apabila mereka sangat pepejal dengan tekanan stim yang tinggi; iaitu tekanan di dalam, mencerminkan kecekapan interaksi. Semakin besar tekanan stimnya, semakin berbau, dan juga lebih mudah.
Contoh
Pembersihan pepejal
Imej pepejal oren dan komponen kemerahannya yang tidak dapat dipulihkan adalah contoh yang mewakili sublimasi mengenai pembersihan pepejal. Segitiga merah boleh diubahsuai seberapa banyak yang diperlukan sehingga kemurnian tinggi dijamin.
Boleh melayani anda: alkoholTeknik ini digunakan terutamanya dengan pepejal wangi. Contohnya: Camphor, Kafein, Benzoine dan Mentol.
Antara pepejal lain yang boleh menyemarakkan sublimasi kita mempunyai: iodin, ais (di ketinggian besar), theobromine (coklat), sakarin, morfin dan ubat -ubatan lain, asas nitrogen dan anthracene.
Sintesis kristal
Kembali ke segitiga merah, sublimasi menawarkan alternatif kepada penghabluran konvensional; Kristal tidak lagi akan disintesis dari penyelesaian, tetapi dengan cara.
Katakan, jika mereka mempunyai dataran merah, pertumbuhan kristal akan mengekalkan geometri ini dan tidak boleh menjadi segi tiga. Kuadrat merah secara beransur -ansur akan tumbuh apabila sublimasi berlaku. Walau bagaimanapun, ia adalah kompleks operasi dan molekul yang kompleks, di mana banyak pembolehubah yang terlibat dilihat.
Contoh -contoh kristal yang disintesis melalui sublimasi adalah: silikon karbida (sic), grafit, arsenik, selenium, fosforus, aluminium nitruro (Aln), kadmium sulfida (Cds), zink seleniuro (ZnSe)2), graphene, antara lain.
Perhatikan bahawa mereka benar -benar dua fenomena yang dipadankan: sublimasi dan pemendapan progresif (atau sublimasi terbalik); Steam berhijrah dari kawasan pepejal ke kawasan atau permukaan yang lebih sejuk, untuk akhirnya mendepositkan dalam bentuk kristal.
Rujukan
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Wikipedia. (2019). Sublimasi (Peralihan Fasa). Diperoleh dari: dalam.Wikipedia.org
- Jones, Andrew Zimmerman. (27 Januari 2019). Sublimasi. Pulih dari: Thoughtco.com
- Sheila Morrissey. (2019). Apa itu Sublimasi dalam Kimia? - Definisi, Proses & Peperiksaan. Kajian. Pulih dari: belajar.com
- Elsevier b.V. (2019). Kaedah Sublimation. Scientedirect. Diperoleh dari: Scientedirect.com
- « Teori Flogist Asal, Prinsip dan Bantahan
- Dimensi Sosial Menjadi Manusia, Pendidikan, Pengetahuan, Kanan, Kesihatan »

