Struktur sulfida tembaga, sifat, kegunaan

- 4863
- 1047
- Anthony Breitenberg
Dia Tembaga sulfida Ia adalah keluarga sebatian bukan organik yang formula kimia umumnya adalah CUxSdan. Yeah x Ia lebih besar daripada dan Ini bermakna sulfida ini lebih kaya dalam tembaga daripada sulfur; Dan jika sebaliknya, x Ia lebih kecil daripada dan, Maka sulfida lebih kaya di sulfur daripada tembaga.
Secara semula jadi, banyak mineral yang mewakili sumber semula jadi kompaun ini mendominasi. Hampir semuanya lebih kaya dalam tembaga daripada sulfur, dan komposisi mereka dinyatakan dan dipermudahkan oleh formula denganxS; di sini x Anda juga boleh mengambil nilai pecahan, menunjukkan pepejal stoikiometrik (CU1.75S, contohnya).
 Sampel mineral Covellita, salah satu daripada banyak sumber semulajadi tembaga sulfida. Sumber: James St. John [CC oleh 2.0 (https: // creativeCommons.Org/lesen/by/2.0)]
Sampel mineral Covellita, salah satu daripada banyak sumber semulajadi tembaga sulfida. Sumber: James St. John [CC oleh 2.0 (https: // creativeCommons.Org/lesen/by/2.0)] Walaupun dalam keadaan asas sulfur berwarna kuning, sebatian derivatifnya kelihatan warna gelap; Seperti itu juga berlaku dengan sulfida tembaga. Walau bagaimanapun, mineral covelita (imej unggul), yang kebanyakannya terdiri daripada CU, mempamerkan perhiasan logam dan iridescence kebiruan.
Mereka boleh disediakan dari sumber tembaga dan sulfur yang berbeza, menggunakan teknik yang berbeza dan mengubah parameter sintesis. Oleh itu, anda boleh mendapatkan nanopartikel cus dengan morfologi yang menarik.
[TOC]
Struktur sulfida tembaga
Pautan
Kompaun ini mempunyai penampilan kristal, jadi anda boleh berfikir dengan segera bahawa ia terdiri daripada ion Cu+ (Tembaga monovalen), CU2+ (Tembaga divalen), s2- E, walaupun, s2- dan s22- (disulfur anion), yang berinteraksi melalui kuasa elektrostatik atau ikatan ionik.
Walau bagaimanapun, terdapat sedikit kovalen antara Cu dan S, dan oleh itu, pautan Cu-S tidak dapat ditolak. Dari alasan ini, struktur kristal CUS (dan semua pepejal yang diperolehnya) mula berbeza daripada yang ditemui atau dicirikan untuk sebatian ionik atau kovalen lain.
Dalam erti kata lain, ia tidak dapat dibincangkan mengenai ion tulen, tetapi di tengah-tengah tarikannya (kation-anion) terdapat sedikit pertindihan orbital luarannya (perkongsian elektron).
Koordinasi di Covelita
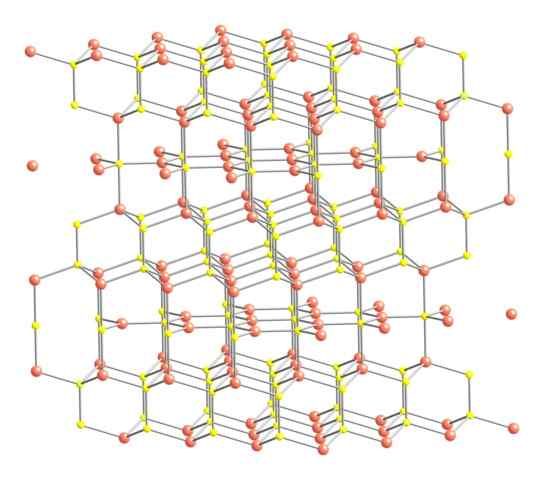 Struktur kristal covellita. Sumber: Benjah-bmm27 [domain awam].
Struktur kristal covellita. Sumber: Benjah-bmm27 [domain awam]. Setelah mengatakan di atas, struktur kristal covelite ditunjukkan dalam imej. Ia terdiri daripada kristal heksagon (ditakrifkan oleh parameter sel unit mereka), di mana ion mengikat dan membimbing dalam koordinasi yang berbeza; Ini, dengan pelbagai jiran berdekatan.
Boleh melayani anda: jenis pautan 02Dalam imej, ion tembaga diwakili dengan sfera merah jambu, manakala sulfur dengan sfera kuning.
Memfokuskan perhatian terlebih dahulu pada sfera merah jambu, akan diperhatikan bahawa ada yang dikelilingi oleh tiga sfera kuning (koordinasi rata trigonal), dan lain -lain untuk empat (koordinasi tetrahedral).
Jenis pertama tembaga, trigonal, dapat dikenalpasti dalam pesawat yang berserenjang dengan wajah heksagon yang mereka berikan kepada pembaca, di mana mereka adalah jenis kedua karbon, tetrahedral.
Menghadiri sekarang ke sfera kuning, ada yang mempunyai lima sfera merah jambu (koordinasi bipyramid trigonal), dan tiga lagi dan sfera kuning (sekali lagi, koordinasi tetrahedral); Di dalamnya sebelum anion disulfida, yang boleh digambarkan dan dalam struktur yang sama dari Covelite:
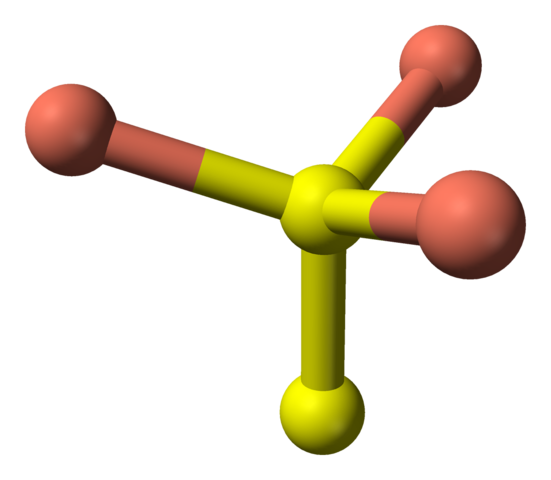 Penyelarasan Tetrahedral Anion Disulfida di Covellita. Sumber: Benjah-bmm27 [domain awam].
Penyelarasan Tetrahedral Anion Disulfida di Covellita. Sumber: Benjah-bmm27 [domain awam]. Formula alternatif
Ada yang ada ion cu2+, Cu+, S2- dan s22-. Walau bagaimanapun, kajian yang dijalankan dengan spektroskopi fotoelektronik XPS (XPS), mereka menunjukkan bahawa semua tembaga adalah seperti kation CU+; Dan oleh itu, formula CUS awal dinyatakan "lebih baik" sebagai (CU+)3(S2-) (S2)-.
Perhatikan bahawa hubungan Cu: s untuk formula sebelumnya terus menjadi 1, dan juga beban dibatalkan.
Kristal lain
Sulfida tembaga boleh mengguna pakai kristal ortorrombik, seperti dalam polimorf, γ-cu2S, dari Calcocita; padu, seperti dalam polimorf lain calcocite, α-cu2S; Tetragonal, di Mineral Anilita, CU1.75S; Monoclinic, di Djurleita, CU1.96S, antara lain.
Bagi setiap kaca yang ditakrifkan terdapat mineral, dan pada gilirannya, setiap mineral mempunyai ciri dan sifatnya sendiri.
Sifat
Umum
Sifat sulfida tembaga adalah tertakluk kepada hubungan cu: s padat mereka. Contohnya, mereka yang membentangkan anion s22- Mereka mempunyai struktur heksagon, dan boleh sama ada semikonduktor atau konduktor logam.
Boleh melayani anda: kalium fosfat (k3po4): struktur, sifat, kegunaanJika sebaliknya kandungan sulfur terdiri daripada anion s2-, Sulfida berkelakuan sebagai semikonduktor, dan juga ada konduktiviti ionik pada suhu tinggi. Ini kerana ion mereka mula bergetar dan bergerak di dalam kristal, dengan itu mengangkut caj elektrik.
Secara optik, walaupun ia juga bergantung pada komposisi tembaga dan sulfurnya, sulfida mungkin atau mungkin tidak menyerap radiasi di rantau inframerah spektrum elektromagnetik. Ciri -ciri optik dan elektrik ini menjadikan bahan -bahan yang berpotensi akan dilaksanakan di peranti yang berbeza.
Pembolehubah lain untuk dipertimbangkan, sebagai tambahan kepada hubungan Cu: s, adalah saiz kristal. Bukan sahaja lebih banyak "sulfur" atau "coppery" sulfida tembaga, tetapi dimensi kristal mereka memberikan kesan yang tidak tepat pada sifat mereka; Oleh itu, saintis tidak sabar -sabar untuk belajar dan mencari aplikasi untuk nanopartikel CUxSdan.
Covelita
Setiap sulfida mineral atau tembaga mempunyai sifat unik. Walau bagaimanapun, mereka semua covelita adalah yang paling menarik dari sudut pandang struktur dan estetik (kerana nada iridescence dan biru). Oleh itu, beberapa sifatnya disebutkan di bawah.
Jisim molar
95,611 g/mol.
Ketumpatan
4.76 g/ml.
Takat lebur
500ºC; Tetapi ia rosak.
Kelarutan air
3.3 · 10-5 G/100 ml pada 18ºC.
Aplikasi
Nanopartikel dalam Perubatan
Bukan sahaja bervariasi saiz zarah sehingga mencapai. Oleh itu, sulfida tembaga boleh membentuk nanospheres, rod, pinggan, filem nipis, sangkar, kabel atau tiub.
Zarah -zarah ini dan morfologi menarik mereka memperoleh aplikasi individu di tanah perubatan yang berbeza.
Contohnya, nanojaulas atau sfera kosong boleh berfungsi sebagai pengangkut dadah di dalam badan. Nanosferas telah digunakan, disokong oleh kaca karbon dan nanotube karbon, untuk berfungsi sebagai pengesan glukosa; Serta agregat mereka sensitif terhadap pengesanan biomolekul seperti DNA.
Ia dapat melayani anda: 6 petunjuk pH semulajadi dan ciri -ciri merekaNanotube cus melebihi nanosferas dalam pengesanan glukosa. Sebagai tambahan kepada biomolekul ini, imunosensor telah direka dari filem nipis CU dan sokongan tertentu untuk pengesanan patogen.
Nanocrystals dan agregat amorf CUS bahkan boleh menyebabkan apoptosis sel kanser, tanpa menyebabkan kerosakan pada sel yang sihat.
Nanosains
Di sub -bahagian anterior dikatakan bahawa nanopartikel mereka telah menjadi sebahagian daripada biosensor dan elektrod. Sebagai tambahan kepada kegunaan sedemikian, saintis dan juruteknik juga telah mengambil kesempatan daripada sifat mereka untuk merancang sel solar, kapasitor, bateri litium, dan pemangkin untuk reaksi organik yang sangat spesifik; unsur -unsur yang sangat diperlukan dalam nanosains.
Ia juga patut disebutkan bahawa apabila mereka disokong pada karbon yang diaktifkan, set NPCUS-CA (CA: Karbon Aktif, dan NP: Nanopartikel) terbukti sebagai penghilang pewarna berbahaya bagi manusia dan oleh itu, berfungsi sebagai pembersih dari pembersih sumber dari sumber air menyerap molekul yang tidak diingini.
Rujukan
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2019). Tembaga sulfida. Diperoleh dari: dalam.Wikipedia.org
- Ivan Grozdanov dan Methodija Najdoski. (Sembilan-belas sembilan puluh lima). Ciri -ciri optik dan elektrik filem sulfida tembaga komposisi berubah -ubah. Jurnal Kimia Negeri Pepejal Volume 114, Isu 2, 1 Februari 1995, halaman 469-475. doi.org/10.1006/JSSC.Sembilan-belas sembilan puluh lima.1070
- Pusat Kebangsaan Maklumat Bioteknologi. (2019). Sulfida tembaga (cus). Pangkalan data PUBCHEM. CID = 14831. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Peter a. Ajibade dan Nandipha l. Botha. (2017). Sintesis, sifat optik dan struktur
- nanocrystals sulfida tembaga dari prekursor molekul tunggal. Jabatan Kimia, Universiti Fort Hare, Beg Persendirian X1314, Alice 5700, Afrika Selatan. Nanomaterials, 7, 32.
- Kerjasama: Pengarang dan editor Volumes III/17E-17F-41C (s.F.). Struktur sulfida tembaga (Cu2s, Cu (2-x) s), parameter latice. Dalam: Madelung atau., Rössler u., Schulz m. (eds) unsur-unsur terikat tanpa tetrahedrally dan sebatian binari i. Landolt-Börnstein-Group III Perkara Pondensed (Data Berangka dan Hubungan Fungsian dalam Sains dan Teknologi), Vol 41c. Springer, Berlin, Heidelberg.
- Momtan, f., Vafaei, a., Ghaedi, m. et al. Korea J. Chem. Eng. (2018). Penggunaan nanopartikel sulfida tembaga dimuatkan karbon aktif untuk penjerapan serentak pewarna terma: metodologi permukaan tindak balas. 35: 1108. doi.org/10.1007/S11814-018-0012-1
- Goel, s., Chen, f., & Cai, w. (2014). Sintesis dan aplikasi bioperubatan nanopartikel sulfida tembaga: dari sensor ke theranostics. Kecil (Weinheim An Der Bergstrasse, Jerman), 10 (4), 631-645. Doi: 10.1002/smll.201301174

