Struktur toluena, sifat, kegunaan, mendapatkan
- 4804
- 1091
- Erick Krajcik
Dia Toluena Ia adalah hidrokarbon aromatik yang formula pekatnya adalah c6H5Ch3 atau Phch3 Dan itu terdiri daripada kumpulan metil (CH3) bersama -sama dengan cincin benzenik atau kumpulan fenil (pH). Ia secara semulajadi ditemui dalam minyak mentah, dalam arang batu, dalam emanasi gunung berapi dan di beberapa pokok, seperti Tolú de América di Selatan.
Pelarut bau ciri ini digunakan terutamanya sebagai bahan mentah perindustrian, dan sebagai pencairan cat. Ia juga digunakan dalam penghapusan parasit yang terdapat dalam kucing dan anjing, seperti ascarid dan anylostomes.
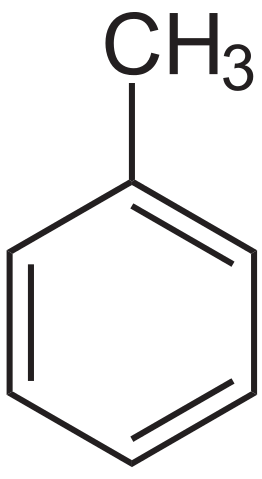
 Formula struktur toluena. Sumber: Neurotoger melalui Wikipedia.
Formula struktur toluena. Sumber: Neurotoger melalui Wikipedia. Toluena diasingkan untuk kali pertama oleh Pierre-Joseph Pelletier dan Philippe Walter, pada tahun 1837, dari Pine Oil. Selanjutnya, Henri Etienne Sainte-Claire DeVille, pada tahun 1841, mengasingkannya dari Tolú Balm dan menunjukkan bahawa produknya sama dengan yang sebelumnya terpencil. Pada tahun 1843, Berzelius membaptisnya sebagai toluin.
Sebilangan besar toluena diperolehi sebagai produk sisi atau menengah dalam proses pengeluaran gas dan penukaran arang batu ke Coke. Ia juga dihasilkan oleh tindak balas yang dibuat di makmal, contohnya, tindak balas benzena dengan metil klorida.
[TOC]
Struktur
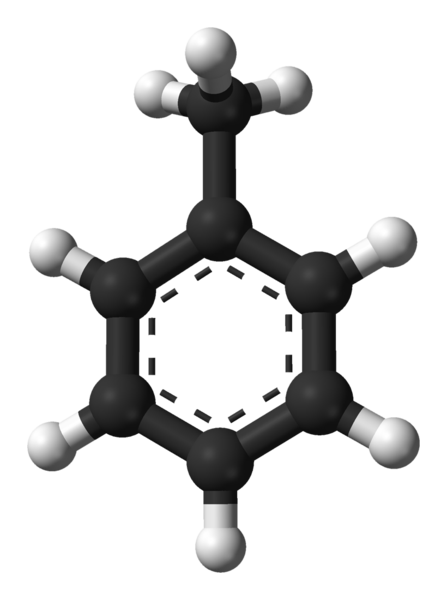 Struktur toluena molekul. Sumber: Ben Mills melalui Wikipedia.
Struktur toluena molekul. Sumber: Ben Mills melalui Wikipedia. Dalam imej unggul kita mempunyai struktur molekul toluena yang diwakili oleh model sfera dan bar. Perhatikan bahawa ia kelihatan sama seperti formula struktur yang ditunjukkan, dengan perbezaan bahawa ia bukan molekul rata sepenuhnya.
Di tengah -tengah cincin benzena, yang dalam kes ini dapat dilihat sebagai kumpulan fenil, pH, watak aromatiknya diserlahkan melalui garis putus -putus. Semua atom karbon mempunyai hibridisasi SP2, Kecuali untuk kumpulan Cho3, yang hibridisasi adalah SP3.
Oleh sebab itu molekul ini tidak sepenuhnya rata: Hydrogens CHO3 Mereka terletak di sudut yang berbeza dari pesawat cincin benzenik.
Dapat melayani anda: tetap pengionanToluena adalah molekul apolar, hidrofobik dan aromatik. Interaksi intermolecularnya didasarkan pada daya penyebaran London, dan dalam interaksi Dipolo-dipolo, kerana pusat cincin itu "dimuatkan" kepadatan elektronik yang disediakan oleh CH3; Walaupun atom hidrogen mempunyai ketumpatan elektronik yang rendah.
Oleh itu, toluena mempunyai beberapa jenis interaksi intermolecular yang mengekalkan molekul cohesif cecair mereka. Ini ditunjukkan dalam titik mendidihnya, 111 ° C, yang tinggi memandangkan ia adalah pelarut apolar.
Sifat
Penampilan fizikal
Cecair tidak berwarna dan telus
Jisim molar
92,141 g/mol
Bau
Manis, ekar dan serupa dengan benzena
Ketumpatan
0.87 g/ml pada 20 ºC
Takat lebur
-95 ºC
Takat didih
111 ºC
Kelarutan
Toluena mempunyai kelarutan yang tidak dapat disangkal di dalam air: 0.52 g/l pada 20 ° C. Ini disebabkan oleh perbezaan polariti antara toluena dan air.
Sebaliknya, toluena larut, atau dalam kes ini, dengan etanol, benzena, etil eter, aseton, kloroform, asid asetik glasial dan disulfida karbon; iaitu, lebih baik diselesaikan dalam pelarut kutub yang kurang.
Indeks pembiasan (nD)
1,497
Goo
0.590 cp (20 ºC)
titik pencucuhan
6 ºC. Toluena mesti dimanipulasi dalam kem pengekstrakan gas dan sejauh mungkin dari sebarang api.
Ketumpatan wap
3.14 dalam hubungan udara = 1. Iaitu, wap mereka tiga kali lebih padat daripada udara.
Tekanan wap
2.8 kPa pada 20 ° C (kira -kira 0.27 atm).
Suhu sendiri
480 ° C
Penguraian
Boleh bertindak balas dengan bersungguh -sungguh dengan bahan pengoksidaan. Apabila dipanaskan untuk penguraian, dia mengeluarkan asap ekar dan menjengkelkan.
Ketegangan permukaan
29.46 mn pada 10 ºC
Momen dipolar
0.36 d
Reaktiviti
Toluena terdedah kepada pengklorinan untuk menghasilkan ortho-chlorotoluene dan para-cllorotoluena. Ia juga mudah untuk dihasilkan untuk menghasilkan nitrotoluena, yang merupakan bahan mentah pewarna.
Boleh melayani anda: berat atomSebahagian daripada toluena digabungkan dengan tiga bahagian asid nitrik untuk menyebabkan trinitrotoluena (TNT): salah satu bahan peledak yang paling terkenal.
Begitu juga, toluena mengalami sulfonasi untuk menjana asid o-toluen-sulfonik dan p-toluen-sulfonik, yang merupakan bahan mentah untuk pembuatan pewarna dan sakarin.
Kumpulan metil toluena mengalami kehilangan hidrogen kerana tindakan asas yang kuat. Kumpulan metil juga mudah terdedah kepada pengoksidaan, jadi ia bertindak balas dengan kalium permanganat menyebabkan asid benzoik dan benzaldehid yang berasal dari.
Aplikasi
Industrialis
 TNT, letupan yang paling simbolik dari semua, berlaku oleh toluena sebagai bahan mentah utama. Sumber: Pixabay.
TNT, letupan yang paling simbolik dari semua, berlaku oleh toluena sebagai bahan mentah utama. Sumber: Pixabay. Toluena digunakan dalam penjelasan lukisan, pencairan cat, kuku yang digilap, pelekat atau gusi pasta, lacquers, dakwat, nilon, plastik, buih poliuretana, kebanyakan minyak, organ vinil, ubat, pewarna, minyak wangi, bahan peledak (TNT).
Dengan cara yang sama, toluena digunakan dalam bentuk toluenosulfonados dalam pembuatan detergen. Toluene juga sangat penting dalam pembuatan simen plastik, kepentingan pewarnaan kosmetik, antibeku, dakwat, asfalt, penanda tetap, simen kenalan, dll.
Pelarut dan pencairan
Toluena digunakan dalam pencairan lukisan, yang memudahkan permohonannya. Ia digunakan untuk membubarkan tepi kit polistirena, dengan itu membolehkan kesatuan bahagian -bahagian yang membentuk model pesawat skala. Di samping itu, ia digunakan dalam pengekstrakan produk semula jadi dari tumbuh -tumbuhan.
Toluena adalah pelarut dakwat yang digunakan di lubang terukir. Simen dicampur dengan getah dan toluena digunakan untuk menampung sebilangan besar produk. Begitu juga, toluena digunakan sebagai pelarut dalam dakwat cetak, lacquers, penyamakan kulit, gam dan disinfektan.
Boleh melayani anda: penyerap molarDan lebih menarik, toluena digunakan sebagai pelarut nanomaterials karbon (seperti nanotube) dan fullerenos.
Yang lain
Campuran benzena, toluena dan xilena (btx) ditambah kepada petrol untuk meningkatkan oktana. Toluene adalah bahan tambahan gas pesawat dan rizab oktana yang tinggi. Ia juga digunakan dalam penjelasan NAFTA.
Toluena membantu dalam penghapusan beberapa spesies ascárides dan anquilostomos, serta tenias yang parasit kucing dan anjing.
Memperoleh
Kebanyakan toluena diperolehi daripada produk suling dari minyak mentah, yang dihasilkan semasa pirolisis hidrokarbon (retak stim). Pembaharuan pemangkin minyak kayu mewakili 87 % daripada toluena yang dihasilkan.
Tambahan 9 % toluena dari petrol pirolisis yang dihasilkan semasa pembuatan etilena dan propilena.
Hulla Tar of Coke Ovens menyumbang 1 % daripada toluena yang dihasilkan, manakala baki 2 % diperolehi sebagai hasil sampingan pembuatan peregangan.
Kesan merosakkan
Toluene adalah pelarut yang dihirup untuk menjadi tinggi, kerana ia mempunyai tindakan narkotik yang mempengaruhi fungsi sistem saraf pusat. Toluena memasuki badan untuk pengambilan, penyedutan dan penyerapan melalui kulit.
Pada tahap pendedahan 200 ppm, pengujaan, euforia, halusinasi, persepsi yang terdistorsi, sakit kepala dan pening mungkin berlaku. Walaupun pendedahan toluena tahap yang lebih tinggi dapat menghasilkan kemurungan, mengantuk dan keburukan.
Apabila penyedutan melebihi kepekatan 10.000 ppm, mampu menghasilkan kematian individu akibat kegagalan pernafasan.
Rujukan
- Graham Solomons t.W., Craig b. Fryhle. (2011). Kimia organik. (10th Edisi.). Wiley Plus.
- Carey f. (2008). Kimia organik. (Edisi keenam). MC Graw Hill.
- Morrison dan Boyd. (1987). Kimia organik. (Edisi Kelima). Addison-Wesley Iberoamericana.
- Pusat Kebangsaan Maklumat Bioteknologi. (2020). Toluena. Pangkalan data PUBCHEM., CID = 1140. Pulih dari: pubchem.NCBI.NLM.NIH.Gov
- Wikipedia. (2020). Toluena. Diperoleh dari: dalam.Wikipedia.org
- Kotak Kejuruteraan, (2018). Toluena - Sifat termophysical. [Dalam talian] pulih dari: EngineeringToolBox.com
- Vedantu. (s.F.). Toluena. Pulih dari: vedantu.com
- « Formula dan Persamaan Gangguan yang merosakkan, Contoh, Latihan
- Struktur, sifat, penggunaan, kesan, kesan sampingan polyvinylpiridone »

