Beryllium Oxide (Beeo)
- 4197
- 1042
- Julius Dibbert
 Struktur kimia beryl oksida
Struktur kimia beryl oksida Apa itu Beryl Oxide?
Dia Beryllium oxide (Beeo) adalah bahan seramik yang, sebagai tambahan kepada kekuatan tinggi dan ketahanan elektriknya, mempunyai kapasiti pengaliran haba yang begitu tinggi yang menjadikan sebahagian daripada reaktor nuklear, bahkan melampaui logam dalam harta terakhir ini.
Sebagai tambahan kepada kegunaannya sebagai bahan sintetik, ia juga boleh didapati dalam alam semula jadi, walaupun jarang. Pengurusannya mesti dijalankan dengan teliti, kerana ia mempunyai keupayaan untuk merosakkan kesihatan manusia secara serius.
Di dunia moden telah diperhatikan bagaimana saintis yang berkaitan dengan syarikat teknologi telah menjalankan penyelidikan untuk membangunkan bahan -bahan canggih untuk aplikasi yang cukup khusus, seperti yang memenuhi bahan semikonduktor dan industri aeroangkasa.
Hasilnya adalah penemuan bahan yang, terima kasih kepada sifat -sifatnya yang sangat berguna dan ketahanan mereka yang tinggi, telah memberi kita peluang untuk maju dari masa ke masa, membolehkan kita membawa teknologi kita ke tahap yang lebih tinggi.
Struktur kimia beryl oksida
Molekul Beryl Oxide (juga dipanggil Berilia) Ia terdiri daripada atom berilium dan salah satu oksigen, kedua -duanya diselaraskan dalam orientasi tetrahedral, dan mengkristal dalam struktur kristal heksagon yang disebut wurtzitas.
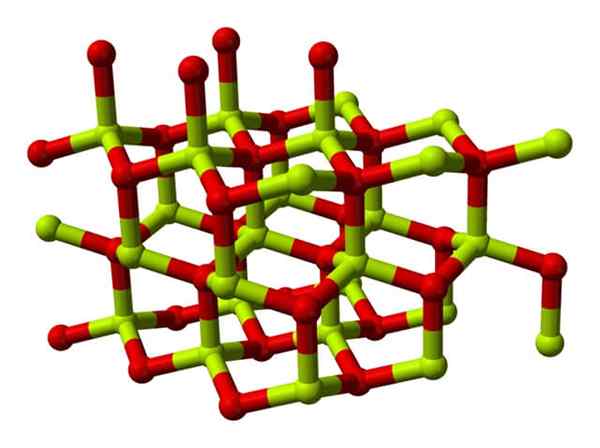 Model struktur kristal beryl oksida. Sumber: Wikimedia Commons
Model struktur kristal beryl oksida. Sumber: Wikimedia Commons Kristal ini mempunyai pusat tetrahedral, yang diduduki oleh BE2+ I2-. Pada suhu tinggi, struktur berilium oksida menjadi jenis tetragonal.
Mendapatkan Beryl Oxide dicapai dengan tiga kaedah: Beryl Carbon Calbon, Dehidrasi Beryl Hydroxide, atau oleh Pencucuhan Beryllium Metalik. Beryllium oksida yang dibentuk pada suhu tinggi tidak aktif, tetapi boleh dibubarkan oleh beberapa sebatian.
Boleh melayani anda: asid klorogenikBeco3 + Haba → lebah + co2 (Penalaan)
Jadilah (oh)2 → Beeo + H2O (dehidrasi)
2 menjadi + atau2 → 2 Beeo (pencucuhan)
Akhirnya, berilium oksida dapat dikurangkan, dan dalam keadaan ini ia akan dibentangkan dalam bentuk molekul diatom.
Sifat oksida bely
Beryllium Oxide dibentangkan sebagai Bromellita, mineral putih yang terdapat di beberapa deposit mangan-hidrero yang kompleks, tetapi lebih sering dijumpai dalam bentuk sintetiknya: pepejal amorf putih yang berlaku dalam bentuk debu.
Juga, kekotoran yang telah terperangkap semasa pengeluaran akan memberikan pelbagai warna kepada sampel oksida.
Titik leburnya terletak di 2.507º C, titik mendidihnya dalam 3.900º C, dan mempunyai ketumpatan 3.01 g/cm3.
Begitu juga, kestabilan kimianya cukup tinggi, hanya bertindak balas dengan wap air pada suhu hampir 1.000º C, dan dapat menahan proses pengurangan karbon dan serangan pada logam cair pada suhu tinggi.
Di samping itu, rintangan mekanikalnya adalah baik, dan boleh diperbaiki dengan reka bentuk dan pembuatan yang mencukupi untuk kegunaan komersial.
Kekonduksian elektrik
Beryllium Oxide adalah bahan seramik yang sangat stabil, dan oleh itu mempunyai ketahanan elektrik yang agak tinggi yang menjadikannya salah satu bahan penebat elektrik terbaik, bersama dengan alumina.
Kerana ini, ia biasanya digunakan untuk peralatan elektrik khusus frekuensi tinggi.
Kekonduksian terma
Beryllium Oxide mempunyai kelebihan yang besar dalam kekonduksian terma: ia dikenali sebagai bahan konduktif haba terbaik kedua di kalangan bukan logam, hanya diatasi oleh berlian, bahan yang jauh lebih mahal dan jarang berlaku.
Boleh melayani anda: ThiolesBagi logam, hanya tembaga dan perak pemindahan yang lebih baik dengan memandu daripada berilium oksida, menjadikannya bahan yang sangat diingini.
Oleh kerana sifat kelakuan haba yang sangat baik, bahan ini terlibat dalam pengeluaran bahan refraktori.
Sifat optik
Oleh kerana sifat kristal yang sama, berilium oksida digunakan untuk penggunaan bahan telus ke ultraviolet di skrin rata dan sel fotovoltaik tertentu.
Begitu juga, kristal berkualiti tinggi boleh berlaku, jadi sifat -sifat ini bertambah baik mengikut proses pembuatan yang digunakan.
Risiko kesihatan
Beryllium Oxide adalah sebatian yang mesti dimanipulasi dengan penuh perhatian, kerana ia pertama kali mempunyai sifat karsinogenik, yang telah dikaitkan dengan penyedutan serbuk atau wap yang berterusan.
Zarah -zarah kecil dalam fasa oksida ini mematuhi paru -paru, dan boleh menghasilkan pembentukan tumor atau penyakit yang dikenali sebagai belliosis.
Berilaiosis adalah penyakit dengan kadar kematian sederhana yang menghasilkan pernafasan, batuk, penurunan berat badan dan demam yang tidak cekap, dan pembentukan granuloma di paru -paru atau organ lain yang terjejas.
Terdapat juga bahaya untuk mengarahkan sentuhan berilium oksida dengan kulit, kerana ia menghakis dan menjengkelkan, dan boleh menyebabkan kerosakan pada permukaan kulit dan membran mukus. Jalan dan tangan pernafasan harus dilindungi ketika bekerja dengan bahan ini, terutama dalam bentuk habuk mereka.
Beryllium oksida menggunakan
Kegunaan beryl oksida dibahagikan terutamanya kepada tiga: aplikasi elektronik, nuklear dan lain -lain.
Boleh melayani anda: apakah erristeneo?Aplikasi elektronik
Keupayaan untuk memindahkan haba ke tahap yang tinggi dan resistiviti elektrik yang baik telah menjadikan Beleril Oxide memperoleh utiliti yang besar sebagai pensil haba.
Penggunaannya dalam litar dalam komputer kapasiti tinggi telah dibuktikan, sebagai tambahan kepada peralatan yang mengendalikan arus elektrik yang tinggi.
Beryllium Oxide adalah telus untuk X -Rays dan Microwave, jadi ia digunakan dalam tingkap terhadap jenis radiasi ini, sebagai tambahan kepada antena, sistem komunikasi dan ketuhar gelombang mikro.
Aplikasi nuklear
Keupayaannya untuk menyederhanakan neutron dan mengekalkan struktur mereka di bawah pengeboman radiasi.
Aplikasi lain
Ketumpatan rendah berilium oksida telah menghasilkan minat dalam industri teknologi aeroangkasa dan ketenteraan, kerana ia dapat mewakili pilihan berat badan yang rendah dalam motor untuk roket dan rompi antibalas.
Akhirnya, ia telah digunakan baru -baru ini sebagai bahan refraktori dalam gabungan logam dalam industri metalurgi.
Rujukan
- Pubchem (s.F.). Beryllium oxide. Diperolehi dari Pubchem.NCBI.NLM.NIH.Gov
- Reade (s.F.). Beryllia/Beryllium Oxide (Beeo). Reade dari Reade.com
- Penyelidikan, c. (s.F.). Beryllium Oxide - Beryllia. Diperoleh dari Azom.com
- Perkhidmatan, n. J. (s.F.). Beryllium oxide. Pulih dari NJ.Gov
- Wikipedia (s.F.). Beryllium oxide. Diperoleh dari dalam.Wikipedia.org

