Tin oksida (ii) struktur, sifat, nomenclature, kegunaan

- 3199
- 677
- Donnie Ryan
Dia Tin Oxide (II) Ia adalah pepejal bukan organik kristal yang dibentuk oleh pengoksidaan timah (SN) oleh oksigen, di mana timah memperoleh valencia 2+. Formula kimianya adalah sno. Dua cara yang berbeza dari sebatian ini diketahui: hitam dan merah. Bentuk biasa dan paling stabil pada suhu bilik adalah pengubahsuaian hitam atau hitam.
Borang ini disediakan oleh hidrolisis klorida timah (ii) (SNCL2) Dalam larutan akueus, yang mana ammonium hidroksida ditambah (NH4OH) untuk mendapatkan endapan oksida terhidrat dari SN (ii) yang formulanya adalah sno.XH2Atau, di mana x<1 (x menor que 1).
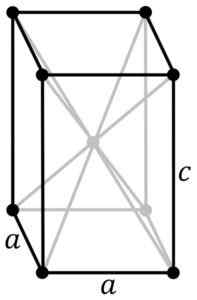 Struktur kristal tetragonal sno hitam-biru. Atom SN terletak di tengah -tengah struktur dan atom oksigen di simpang. PNG Asal oleh Pengguna: Rocha, dikesan di Inkscape oleh Pengguna: Stannered [CC BY-SA 3.0 (http: // creativeCommons.Org/lesen/by-sa/3.0/]] Sumber: Wikipedia Commons
Struktur kristal tetragonal sno hitam-biru. Atom SN terletak di tengah -tengah struktur dan atom oksigen di simpang. PNG Asal oleh Pengguna: Rocha, dikesan di Inkscape oleh Pengguna: Stannered [CC BY-SA 3.0 (http: // creativeCommons.Org/lesen/by-sa/3.0/]] Sumber: Wikipedia Commons Oksida terhidrat adalah pepejal amorf putih, yang kemudian dipanaskan dalam penggantungan hingga 60-70 ºC selama beberapa jam dengan kehadiran NH4Oh, sehingga anda mendapat sno murni kristal hitam.
Bentuk merah sno itu metastable. Ia boleh disediakan dengan menambahkan asid fosforik (h3PO4) - Dengan asid fosforus 22%, h3PO3 - Dan kemudian NH4Oh penyelesaian SNCL2. Pepejal putih yang diperoleh dipanaskan dalam penyelesaian yang sama hingga 90-100 ºC selama kira-kira 10 minit. Dengan cara ini sno kristal merah tulen diperolehi.
Tin Oxide (II) adalah bahan permulaan untuk pengeluaran sebatian timah lain (ii). Atas sebab ini, ia adalah salah satu sebatian timah yang mempunyai kepentingan komersial yang cukup.
Tin Oxide (II) membentangkan ketoksikan yang rendah seperti kebanyakan sebatian timah. Ini disebabkan oleh penyerapan mereka yang lemah dan perkumuhan kain makhluk hidup yang pesat.
Ia dapat melayani anda: Bipe Beraral: Apa, Ciri -ciri, Apa Itu UntukMembentangkan salah satu toleransi terbesar sebatian timah dalam ujian yang dijalankan dengan tikus. Walau bagaimanapun, ia boleh berbahaya jika ia dihirup dalam kuantiti yang banyak.
[TOC]
Struktur
Tin Oxide (ii) Black-Blue
Pengubahsuaian ini mengkristal dengan struktur tetragonal. Ia mempunyai lapisan mengatur.
Penyelidik lain mengesahkan bahawa setiap atom SN dikelilingi oleh 5 atom oksigen yang kira -kira di simpang octahedron, di mana puncak keenam mungkin diduduki oleh sepasang elektron bebas atau tidak berpasangan. Ini dikenali sebagai susunan φ-oktik.
Oksida timah merah (ii)
Bentuk oksida timah ini (ii) mengkristal dengan struktur ortorrombik.
Nomenclature
- Tin Oxide (II)
- Estany Oxide
- Tin Monoxide
- Estany Oxide
Sifat
Keadaan fizikal
Pepejal kristal.
Berat molekul
134.71 g/mol.
Takat lebur
1080 ºC. Ia terurai.
Ketumpatan
6.45 g/cm3
Kelarutan
Tidak larut dalam air sejuk atau panas. Tidak larut dalam metanol, tetapi ia larut dengan cepat dalam asid dan alkali pekat.
Sifat lain
Sekiranya lebih daripada 300 ºC dipanaskan dengan kehadiran udara, oksida timah (II) dengan cepat dioksidakan dalam oksida timah (iv) yang menyampaikan incandescence.
Telah dilaporkan bahawa di bawah keadaan bukan oksidan, pemanasan oksida timah (ii) mempunyai pelbagai hasil mengikut tahap kesucian oksida permulaan. Ia biasanya tidak seimbang dalam logam SN dan timah oksida (IV), SNO2, Dengan pelbagai spesies perantaraan yang akhirnya menjadi sno2.
Tin Oxide (II) adalah amphotero, kerana ia dibubarkan dalam asid untuk memberikan ion SN2+ atau kompleks anion, dan juga larut dalam alkali untuk membentuk penyelesaian ion hidroksi, SN (OH)3-, yang mempunyai struktur piramida.
Ia boleh melayani anda: asid perchloric: formula, ciri dan kegunaanDi samping itu, SNO adalah ejen pengurangan dan bertindak balas dengan cepat dengan asid dan mineral organik.
Ia membentangkan ketoksikan yang rendah jika dibandingkan dengan garam timah yang lain. DL50 (50% dos maut atau dos maut sederhana) pada tikus lebih daripada 10000 mg/kg. Ini bermakna lebih daripada 10 gram setiap kilogram diperlukan untuk membunuh 50% spesimen tikus di bawah tempoh percubaan tertentu. Sebagai perbandingan, TIN Fluoride (ii) membentangkan 188 mg/kg DL50.
Walau bagaimanapun, jika ia disedut untuk masa yang lama, ia disimpan di dalam paru -paru kerana ia tidak diserap dan boleh menghasilkan timah (penyusupan debu SNO di interstices paru -paru).
Aplikasi
Dalam pengeluaran sebatian timah lain (ii)
Reaksi pesatnya dengan asid adalah asas penggunaan yang paling penting, yang merupakan perantara dalam pembuatan sebatian timah yang lain.
Ia digunakan dalam pengeluaran bromida timah (II) (SNBR2), Sianida timah (II) (SN (CN)2) dan hidrat fluoroborat TIN (II) (SN (BF4)2), Antara sebatian timah lain (ii).
Tin fluoroborate (ii) disediakan dengan membubarkan snam. Ini disebabkan, antara lain, dengan kapasiti liputan yang tinggi.
Timah (ii) oksida juga digunakan dalam penyediaan sulfat timah (ii) (SNSO4), oleh tindak balas asid sno dan sulfurik, h2SW4.
SNSO4 Diperoleh, ia digunakan dalam proses tinned untuk pengeluaran plat litar bercetak, untuk selesai hubungan elektrik dan untuk peralatan dapur.
Boleh melayani anda: aluminium karbonat: struktur, sifat, kegunaan Litar bercetak. Tiada pengarang yang boleh dibaca mesin yang disediakan. Abraham del Pozo diasumsikan (berdasarkan tuntutan hak cipta). [Domain Awam] Sumber: Wikimedia Commons
Litar bercetak. Tiada pengarang yang boleh dibaca mesin yang disediakan. Abraham del Pozo diasumsikan (berdasarkan tuntutan hak cipta). [Domain Awam] Sumber: Wikimedia Commons Bentuk terhidrat Sno, Tin Hydrotado (II) Sno.XH2Atau, ia dirawat dengan asid fluorhorhoric untuk mendapatkan fluorida timah (II), SNF2, yang ditambah kepada krim dentifric sebagai ejen untuk memerangi karies.
Dalam perhiasan
Tin Oxide (II) digunakan dalam penyediaan kristal emas dan tembaga-stub kristal. Nampaknya fungsinya dalam aplikasi ini adalah bertindak sebagai ejen pengurangan.
 Jewel dengan Ruby. Sumber: Pixabay
Jewel dengan Ruby. Sumber: Pixabay Kegunaan lain
Ia telah digunakan dalam peranti fotovoltaik untuk pengeluaran elektrik dari cahaya, seperti sel solar.
 Peranti fotovoltaik. Georg slickers [CC BY-SA 2.5 (https: // creativeCommons.Org/lesen/by-sa/2.5)] Sumber: Wikipedia Commons
Peranti fotovoltaik. Georg slickers [CC BY-SA 2.5 (https: // creativeCommons.Org/lesen/by-sa/2.5)] Sumber: Wikipedia Commons Inovasi terkini
Nanopartikel yang diperintahkan telah digunakan dalam elektrod nanotube karbon untuk bateri lithium-gula.
 Sno hidrat nanofibers. Fionán [cc by-sa 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)] Sumber: Wikipedia Commons
Sno hidrat nanofibers. Fionán [cc by-sa 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)] Sumber: Wikipedia Commons Elektrod yang disediakan sno mempamerkan kekonduksian yang tinggi dan sedikit perubahan dalam jumlah dalam pemuatan berulang dan muat turun kitaran.
Di samping itu, SNO memudahkan pemindahan ion/elektron yang cepat semasa tindak balas pengurangan pengoksidaan yang berlaku dalam sistem bateri tersebut.
Rujukan
- Kapas, f. Albert dan Wilkinson, Geoffrey. (1980). Kimia bukan organik maju. Edisi keempat. John Wiley & Sons.
- Tarian, j.C.; Emeléus, h.J.; Sir Ronald Nyholm dan Trotman-Deckenson, ke.F. (1973). Kimia bukan organik yang komprehensif. Jilid 2. Pergamon Press.
- Ensiklopedia Kimia Perindustrian Ullmann. (1990). Edisi Kelima. Jilid A27. VCH Verlagsgellschaft MBH.
- Kirk-Othmer (1994). Ensiklopedia Teknologi Kimia. Jilid 24. Edisi keempat. John Wiley & Sons.
- Ostrakhovitch, Elena ke. Dan cherian, m. George. (2007). Timah. Dalam buku panduan logam toksikologi. Edisi ketiga. Pulih dari Scientedirect.com.
- Kwestroo, w. dan vromans, p.H.G.M. (1967). Penyediaan tiga pengubahsuaian timah tulen (ii) oksida. J. Inorg. Nucl. Chem., 1967, Vol.29, ms.2187-2190.
- Foud, s.S et al. (1992). Sifat optik filem nipis oksida stannous. Czechoslovak Journal of Physics. Februari 1992, Jilid 42, Isu 2. Pulih dari Springer.com.
- A-young Kim et al. (2017). Memesan nanopartikel sno di MWCNT sebagai bahan tuan rumah berfungsi untuk katod bateri lithium-sulfur tinggi. Nano Research 2017, 10 (6). Pulih dari Springer.com.
- Perpustakaan Perubatan Negara. (2019). Stannous Oxide. Pulih dari: pubchem.NCBI.NLM.NIH.Gov

