Besi oksida

- 2381
- 270
- Clarence Greenholt DDS
 Besi Oksida adalah sebatian kimia antara besi dan oksigen
Besi Oksida adalah sebatian kimia antara besi dan oksigen Apa itu Besi Oksida?
Dia Besi oksida Ia adalah sebatian yang terbentuk antara besi dan oksigen. Mereka dicirikan dengan menjadi ionik dan kristal, dan mereka berbaring bertaburan akibat hakisan mineral mereka, menyusun tanah, jisim tumbuhan dan bahkan pedalaman organisma hidup.
Ia adalah salah satu keluarga sebatian yang mendominasi di kerak bumi. Oksida besi diketahui sehingga kini, kebanyakannya berasal dari semula jadi dan lain -lain disintesis di bawah tekanan atau keadaan suhu yang melampau.
Di bahagian atas, bahagian serbuk oksida ferrik ditunjukkan. Warna merah ciri merangkumi besi dari beberapa elemen seni bina dalam apa yang dikenali sebagai karat. Begitu juga, diperhatikan di lereng, gunung atau tanah, dicampur dengan banyak mineral lain, seperti debu kuning Goethita (α-Feooh).
Oksida besi yang paling terkenal adalah hematit (α-Fe2Sama ada3) dan maghemita (ϒ-faith2Sama ada3), kedua -dua polimorf oksida ferrik; Dan sekurang -kurangnya, magnetite (iman3Sama ada4).
Struktur polimorf mereka dan kawasan dangkalnya yang besar dibuat oleh bahan -bahan yang menarik seperti sorbentes, atau untuk sintesis nanopartikel dengan aplikasi yang luas.
Struktur oksida besi
Imej atas adalah perwakilan struktur kristal yang hodoh, salah satu oksida besi di mana besi mempunyai valensi +2. Sfera merah sesuai dengan anion atau2-, Manakala kuning ke kation iman2+.
Perhatikan bahawa setiap iman2+ dikelilingi oleh enam atau2-, membentuk unit koordinasi octahedral.
Oleh itu, struktur hodoh boleh "runtuh" dalam unit hodoh6, Di mana atom pusat adalah iman2+. Dalam kes oxihydroxides atau hidroksida, unit octahedral hodoh3(Oh)3.
Boleh melayani anda: kalsium peroksida (CaO2): sifat, risiko dan kegunaanDalam beberapa struktur, bukannya octahedron, terdapat unit tetrahedral, hodoh4. Atas sebab ini, oksida besi biasanya diwakili dengan octured atau tetrahedra dengan pusat besi.
Struktur oksida besi bergantung pada keadaan tekanan atau suhu, pada iman/atau nisbah (iaitu, berapa banyak oksigen yang ada untuk besi dan sebaliknya), dan Valencia del Hierro (+2, +3 dan, sangat jarang dalam oksida sintetik , +4).
Secara umum, anion besar atau2- Mereka menyelaraskan lembaran yang membentuk lubang yang menjadi tuan rumah kation iman2+ atau iman3+. Oleh itu, terdapat oksida (seperti magnetit) yang mempunyai besi dengan kedua -dua nilai.
Polimorfisme
Oksida besi mempunyai polimorfisme, iaitu, struktur yang berbeza atau pengaturan kristal untuk sebatian yang sama. Ferric Oxide, Iman2Sama ada3, mempunyai sehingga empat polimorf yang mungkin. Hematit, α-fe2Sama ada3, Ia adalah yang paling stabil dari semua; diikuti oleh Maghemita, ϒ-faith2Sama ada3, dan untuk β- iman sintetik2Sama ada3 dan ε- iman2Sama ada3.
Mereka semua mempunyai jenis struktur dan sistem kristal sendiri. Walau bagaimanapun, perkadaran 2: 3 kekal malar, jadi terdapat tiga anion atau2- untuk setiap dua kation iman3+.
Perbezaannya terletak pada bagaimana unit octahedral yang jelek berada6 di angkasa dan bagaimana mereka berkumpul.
Pautan struktur
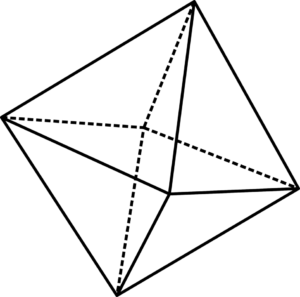 Unit Octahedral Ugly6
Unit Octahedral Ugly6 Unit octahedral yang jelek6 boleh digambarkan dengan bantuan imej yang unggul. Di sudut oktaedro adalah atau2-, Semasa berada di tengahnya, iman2+ atau iman3+(Dalam hal iman2Sama ada3). Cara di mana octahedra ini diatur di angkasa mendedahkan struktur karat.
Walau bagaimanapun, mereka juga mempengaruhi bagaimana mereka menghubungkan. Sebagai contoh, dua octahedra boleh menyertai dua simpang mereka, yang diwakili dengan jambatan oksigen: Fe-o-fe. Begitu juga, octahedra dapat bergabung melalui tepi mereka (bersebelahan antara satu sama lain). Ia kemudiannya diwakili dengan dua jambatan oksigen: Fe- (o)2-Iman.
Boleh melayani anda: klorin oksida (v): sifat, struktur, kegunaanDan akhirnya, octahedra dapat berinteraksi melalui wajah mereka. Oleh itu, perwakilan sekarang akan dengan tiga jambatan oksigen: fe- (o)3-Iman. Cara di mana octahedra dikaitkan, jarak internuclear fe -fe akan berubah dan, oleh itu, sifat fizikal oksida.
Sifat oksida besi
Oksida besi adalah sebatian dengan sifat magnet. Ini boleh menjadi anti, ferro atau ferrimagnetic, dan bergantung pada nilai iman dan bagaimana kation berinteraksi dengan pepejal.
Kerana struktur pepejal sangat bervariasi, dengan cara yang sama sifat fizikal dan kimia mereka.
Contohnya, polimorf dan hidrat iman2Sama ada3 Mereka mempunyai nilai yang berbeza dari titik lebur (yang berkisar antara 1.200 dan 1.600 ° C) dan kepadatan. Walau bagaimanapun, mereka mempunyai kelarutan yang sedikit berikutan iman3+, Jisim molekul yang sama adalah warna coklat dan hampir tidak dibubarkan dalam penyelesaian asid.
Nomenklatur oksida besi
IUPAC menetapkan tiga cara untuk menamakan oksida besi. Ketiga sangat berguna, walaupun untuk oksida kompleks (seperti iman7Sama ada9) Sistematik mengawal yang lain kerana kesederhanaannya.
Nomenklatur sistematik
Nombor oksigen dan besi diambil kira, menamakannya dengan awalan mono-mono-, di-, tri-, dll. Mengikut tatanama ini iman2Sama ada3 dipanggil: Trioksida memberibesi. Dan untuk iman7Sama ada9 Namanya ialah: Heptahierro nonaxide.
Nomenclature stok
Ini menganggap Valencia del Hierro. Sekiranya iman itu2+, Besi Oksida ditulis ... dan valensi dengan nombor Roman terkunci dalam kurungan. Untuk iman2Sama ada3 Namanya ialah: Besi Oksida (III).
Boleh melayani anda: tekanan stim: konsep, contoh dan latihan diselesaikanPerhatikan bahawa iman3+ Ia dapat ditentukan oleh jumlah algebra. Ya2- Ia mempunyai dua caj negatif, dan terdapat tiga daripadanya, tambah -6. Untuk meneutralkan ini -6 mereka memerlukan +6, tetapi ada dua iman, sehingga mereka harus dibahagikan dengan dua, +6/2 = +3:
2x (logam Valencia) + 3 (-2) = 0
Cukup membersihkan valensi iman dalam oksida. Tetapi jika x bukan integer (seperti hampir semua oksida yang tinggal), maka ada campuran iman2+ dan iman3+.
Nomenclature tradisional
Akhiran -ico diberikan kepada awalan ferr- apabila iman mempunyai valencia +3, dan -so ketika valencia adalah 2+. Oleh itu, iman2Sama ada3 dipanggil: Ferric Oxide.
Besi oksida menggunakan
Nanopartikel
Oksida besi mempunyai tenaga penghabluran yang tinggi, yang membolehkan untuk menghasilkan kristal yang sangat kecil tetapi dengan kawasan permukaan yang besar.
Atas sebab ini mereka sangat menarik minat bidang nanoteknologi, di mana mereka merancang dan mensintesis nanopartikel oksida (NPS) untuk tujuan tertentu:
- Sebagai pemangkin.
- Sebagai takungan dadah atau gen di dalam badan.
- Dalam reka bentuk permukaan deria untuk pelbagai jenis biomolekul: protein, gula, lemak.
- Untuk menyimpan data magnet.
Pigmen
Kerana sesetengah oksida sangat stabil, mereka berfungsi untuk pewarna tekstil atau memberikan warna terang ke permukaan bahan apa pun. Dari mosaik lantai -lukisan merah, kuning dan oren (walaupun hijau) -plastik, kulit ke kerja seni bina.
Rujukan
- Pemegang Amanah Kolej Dartmouth (18 Mac 2004). Stoikiometri oksida besi. Diambil dari: Dartmouth.Edu
- Ryosuke Sinmyo et al. (8 September 2016). Penemuan Fe7Sama ada9: Oksida besi baru dengan struktur monoklinik yang kompleks. Pulih dari: alam semula jadi.com
- M. Cornell, u. Schwertmann. Oksida besi: struktur, sifat, tindak balas, kejadian dan kegunaan [pdf]. Wiley-VCH. Diambil dari: EPSC511.Wustl.Edu

