Amina

- 4760
- 236
- Ms. Edgar Carroll
Apakah amina?
The amina Mereka adalah sebatian organik yang berasal dari ammonia. Di dalamnya terdapat kesatuan kovalen antara karbon dan nitrogen. Sememangnya, molekul nitrogen secara kinetik tidak aktif; Tetapi terima kasih kepada penetapan biologi, ia menjadi ammonia, yang seterusnya mengalami reaksi alkilasi berikutnya.
Apabila ammonia "disewa", ia menggantikan satu, dua atau tiga daripada tiga hidrogennya dengan atom karbon. Karbon ini mungkin berasal dari kumpulan sewa (r) atau aril (AR). Oleh itu, terdapat amina alifatik (linear atau bercabang), dan aromatik.
Amina adalah pangkalan organik yang lebih kuat daripada ammonia yang sama. Mereka mudah ditanggalkan dari bahan tumbuhan, dan secara amnya mempunyai interaksi yang kuat dengan matriks neuron organisma; Oleh itu, banyak ubat dan ubat terdiri daripada amina dengan struktur dan substituen yang kompleks.
Struktur amina
 Formula umum untuk amina. Sumber: Mache, Wikimedia Commons.
Formula umum untuk amina. Sumber: Mache, Wikimedia Commons. Walaupun ia berbeza -beza bergantung kepada sifat r, persekitaran elektronik atom nitrogen adalah sama bagi mereka semua: tetrahedral. Tetapi, mempunyai beberapa elektron yang tidak dikongsi pada atom nitrogen (··), geometri molekul menjadi piramida. Ini begitu dengan ammonia dan amina.
Aminas boleh diwakili dengan tetrahedron, dan juga seperti yang dilakukan dengan sebatian karbon. Oleh itu, NH3 dan ch4 Mereka ditarik seperti tetrahedra, di mana pasangan (··) terletak di salah satu simpang di atas nitrogen.
Kedua -dua molekul adalah aquiral; Walau bagaimanapun, mereka mula membentangkan kreinya kerana H mereka menggantikannya. Amina r2NH adalah aquiral jika kedua r adalah berbeza. Walau bagaimanapun, ia tidak mempunyai sebarang konfigurasi untuk membezakan enantiomer dari yang lain (seperti yang berlaku dengan pusat karbon kiral).
Ini kerana enantiomer:
R2N-H | H-nr2
Mereka ditukar dengan kelajuan supaya tidak dapat diasingkan; dan oleh itu, struktur amina dianggap sebagai akuir walaupun semua substituen dalam atom nitrogen berbeza.
Sifat amina
Polariti
Amina adalah sebatian kutub, kerana kumpulan NH Amino2, Kerana mempunyai atom nitrogen elektrogen, ia menyumbang kepada momen dipole molekul. Perhatikan bahawa nitrogen mempunyai keupayaan untuk menderma ikatan hidrogen, yang umumnya mempunyai titik mendidih dan gabungan yang tinggi.
Ciri -ciri fizikal
Di dunia kimia, ketika bercakap tentang amina, perbuatan sukarela menutup hidungnya. Ini kerana, secara umum, mereka biasanya mempunyai bau yang tidak menyenangkan, yang sebahagiannya kelihatan seperti ikan busuk.
Ia dapat melayani anda: Reaksi MaillardDi samping itu, amina cecair biasanya mempunyai warna kekuningan, yang meningkatkan ketidakpercayaan visual yang mereka hasilkan.
Kelarutan air
Amina cenderung tidak larut dalam air kerana, walaupun dapat membentuk jambatan hidrogen dengan H₂o, komponen organik majoriti adalah hidrofobik. Semakin banyak kumpulan r, semakin kurang kelarutan mereka di dalam air akan.
Apabila terdapat asid di tengah, bagaimanapun, kelarutan meningkat dengan pembentukan apa yang dikenali sebagai garam amina. Di dalamnya, nitrogen mempunyai beban separa yang positif, yang menarik secara elektrostal ke pangkalan anion atau asid konjugasi.
Asas
Amina adalah pangkalan organik yang lebih kuat daripada ammonia. Semakin besar ketumpatan elektronik di sekitar atom nitrogen, semakin asasnya; iaitu, asid medium akan tidak bersemangat dengan lebih cepat. Sekiranya amina sangat asas, ia juga boleh merebut proton dari alkohol.
Jenis (primer, menengah, tertiari)
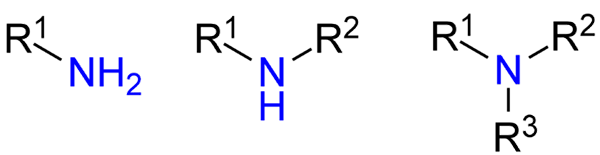 Jenis amina. Sumber: Jü melalui Wikipedia.
Jenis amina. Sumber: Jü melalui Wikipedia. Walaupun mereka belum dibentangkan secara rasmi, rujukan telah dibuat kepada amina primer, menengah dan tertiari (imej atas, dari kiri ke kanan).
Amina utama (RNH2) adalah monosusttuidas; Menengah (r2NH), dibubarkan, dengan dua kumpulan alcomile atau aril; dan tertiari (r3N), adalah trisustuid, dan kekurangan hidrogen.
Semua amina yang ada diperoleh dari tiga jenis ini, jadi kepelbagaian dan interaksi mereka dengan matriks biologi dan neuron sangat besar.
Secara umum, amina tertiari dijangka menjadi yang paling asas; Walau bagaimanapun, pernyataan sedemikian tidak boleh dibuat tanpa mengetahui struktur r.
Pembentukan amina
Ammonia Alkylation
Pada mulanya ia disebutkan bahawa amina berasal dari ammonia; Oleh itu, cara paling mudah untuk membentuknya adalah melalui alkilasi mereka. Untuk melakukan ini, lebihan ammonia bertindak balas dengan alkil halida, diikuti dengan penambahan pangkalan untuk meneutralkan garam amina:
NH3 + Rx => rnh3+X- => Rnh2
Perhatikan bahawa langkah -langkah ini membawa kepada amina utama. Amina sekunder dan bahkan tertiari juga boleh dibentuk, jadi prestasi untuk satu produk berkurangan.
Beberapa kaedah latihan, seperti sintesis Gabriel, membolehkan untuk mendapatkan amina utama supaya produk lain yang tidak diingini tidak terbentuk.
Boleh melayani anda: etil alkohol: struktur, sifat, kegunaan, memperolehBegitu juga, keton dan aldehid dapat dikurangkan dengan kehadiran ammonia dan amina utama, untuk menimbulkan amina menengah dan tertiari.
Hidrogenasi pemangkin
Sebatian nitro dapat dikurangkan dengan kehadiran hidrogen dan pemangkin untuk berubah menjadi amina yang sepadan.
Arno2 => Rnah2
Nitrilos, RC≡N, dan Amidas, RCONR2, Mereka juga dikurangkan untuk memberi amina utama dan tertiari.
Nomenclature
Bagaimana amina dinamakan? Kebanyakan masa mereka dinamakan mengikut r, kumpulan aquilo atau aril. Kepada nama R, berasal dari alkana, perkataan 'amine' ditambah kepadanya pada akhirnya.
Oleh itu, Ch3Ch2Ch2NH2 Ia adalah propilamine. Sebaliknya, ia hanya boleh dilantik sebagai alkane dan bukan sebagai kumpulan R: propanamine.
Cara pertama untuk menamakannya adalah seperti yang diketahui dan digunakan.
Apabila terdapat dua kumpulan NH2, Alkane dilantik dan kedudukan kumpulan amino disenaraikan. Oleh itu, h2Nch2Ch2Ch2Ch2NH2 Ia dipanggil: 1.4-butanodiamine.
Sekiranya terdapat kumpulan oksigen, seperti OH, keutamaan harus diberikan kepada NH2, yang dilantik sebagai substituen. Contohnya, Hoch2Ch2Ch2NH2 dipanggil: 3-aminopropanol.
Dan berkenaan dengan amina menengah dan tertiari, huruf N dibuat untuk menunjukkan kumpulan r. Rantai terpanjang akan menyimpan nama sebatian. Oleh itu, Cho3NHCH2Ch3 Ia dipanggil: n-methylethylamine.
Penggunaan amina
Pewarna
Amina aromatik utama boleh berfungsi sebagai bahan permulaan untuk sintesis pewarna azo. Pada mulanya, amina bertindak balas untuk membentuk garam diazonium, yang membentuk sebatian dengan copulation bumbung (atau gandingan diazoik).
Oleh kerana pewarnaannya yang kuat, ia digunakan dalam industri tekstil sebagai bahan pencelupan; Contohnya: metil oren, coklat 138 langsung, matahari terbenam kuning dan ponceau.
Dadah dan Dadah
Banyak ubat bertindak dengan agonis dan antagonis neurotransmiter amina semulajadi. Contoh:
-Chloropheniramine adalah antihistamin yang digunakan dalam kawalan proses alahan kerana pengambilan beberapa makanan, demam hay, sengatan serangga, dll.
-Chlorpromazine adalah ejen sedatif, bukan induktor tidur. Ia melegakan kecemasan dan bahkan digunakan dalam rawatan beberapa gangguan mental.
-Ephedrine dan Phenymphedrine digunakan sebagai dekongestan saluran pernafasan.
Boleh melayani anda: osmolarity-Amitriptaline dan imipramine adalah amina tertiari yang digunakan dalam rawatan kemurungan. Kon antidepresan tricyclic diklasifikasikan oleh struktur mereka.
-Analgesik opioid seperti morfin, codeline dan heroin adalah amina tertiari.
Rawatan Gas
Beberapa amina, termasuk diglycolamine (DGA) dan dietolamine (DEA), digunakan dalam penghapusan gas karbon dioksida (CO2) dan hidrogen sulfida (h2S) hadir dalam gas asli dan kilang penapis.
Kimia Pertanian
Metilamin adalah sebatian perantara dalam sintesis bahan kimia yang digunakan dalam pertanian seperti herbisida, racun racun, racun serangga, dan biosida.
Pembuatan resin
Metilamines digunakan semasa penjelasan resin pertukaran ion, boleh digunakan dalam deionisasi air.
Nutrien haiwan
Trimethylamine (TMA) digunakan terutamanya dalam pengeluaran klorida klorida, suplemen vitamin B yang digunakan dalam ayam, ayam belanda dan babi.
Industri getah
Minyak dimethylamine (DMA) adalah pengemulsi untuk digunakan dalam pengeluaran getah sintetik. DMA digunakan secara langsung sebagai pengubah pempolimeran dalam fasa wap butadiena, dan sebagai penstabil lateks getah asli dan bukannya ammonia
Pelarut
Dimethylamine (DMA) dan monomethylamine (MMA) digunakan untuk mensintesis pelarut polar polar timethylformamide (DMF), dimethylacetamide (DMAC) dan N-methylpiridone (NMP) (NMP).
Antara aplikasi DMF, termasuk: salutan uretana, pelarut benang akrilik, pelarut reaksi dan pelarut pengekstrakan.
DMAC digunakan dalam pembuatan pewarna dan pelarut benang. Akhirnya, NMP digunakan dalam penapisan minyak pelincir, pickup dan salutan enamel.
Contoh amina
Kokain
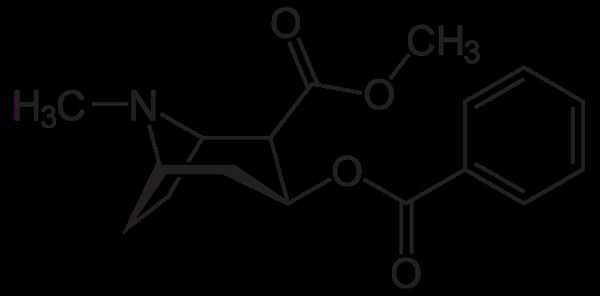 Molekul kokain. Neurotokeker, Wikimedia Commons
Molekul kokain. Neurotokeker, Wikimedia Commons Kokain digunakan sebagai anestetik tempatan dalam beberapa jenis pembedahan mata, telinga dan tekak. Seperti yang dilihat, ia adalah amina tertiari.
Nikotin
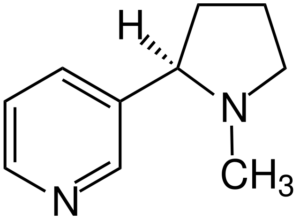 Molekul nikotin. Sumber: Jü [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)], dari Wikimedia Commons
Molekul nikotin. Sumber: Jü [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)], dari Wikimedia Commons Nikotin adalah ejen utama ketagihan tembakau dan kimia tertiari. Nikotin yang terdapat di asap tembakau diserap dengan cepat dan sangat beracun.
Morfin
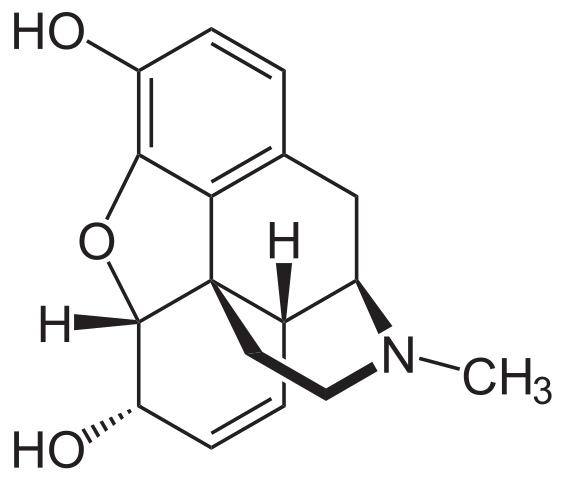 Molekul morfin. Sumber: Neurotoger [Domain Awam], dari Wikimedia Commons
Molekul morfin. Sumber: Neurotoger [Domain Awam], dari Wikimedia Commons Ini adalah salah satu analgesik yang paling berkesan untuk melegakan kesakitan, terutama kanser. Sekali lagi, amina tertiari.
Serotonin
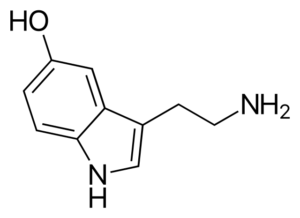 Serotonin molekul. Sumber: Harbin [Domain Awam], dari Wikimedia Commons
Serotonin molekul. Sumber: Harbin [Domain Awam], dari Wikimedia Commons Serotonin adalah neurotransmitter amina. Pada pesakit yang tertekan, kepekatan metabolit utama serotonin menurun. Tidak seperti amina lain, ini adalah yang utama.
Rujukan
- Methylamines: Kegunaan dan aplikasi. Pulih dari: chemours.com
- Penyelidikan Pasaran Ketelusan. (s.F.). Amina: Fakta dan Kegunaan Penting. Pulih dari: TransparencyMarketResearch.com

