Struktur Bifthalate Potassium, Nomenclature, Kegunaan, Risiko
- 2411
- 730
- Julius Dibbert
Dia Potassium bifthalate Ia adalah sebatian kimia, pepejal, putih, larut, yang secara komersil dalam keadaan kemurnian tinggi. Ia digunakan sebagai corak utama untuk menyeragamkan penyelesaian dalam kelayakan asid-asas; Ia juga digunakan sebagai penyelesaian penampan untuk memastikan pH penyelesaian stabil.
Ia adalah sebatian yang stabil, bukan hygroscopic, yang memudahkan penyediaan penyelesaian kerana ia tidak menyerap air semasa proses berat. Ia boleh disediakan oleh tindak balas antara asid fotal dan larutan KOH, di mana hidrogen molekul asid phthalic digantikan oleh atom kalium.
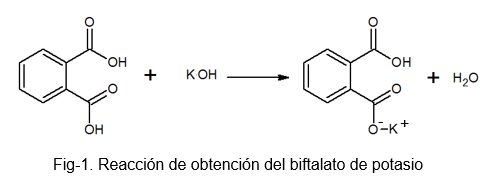
Potassium bifthalate menerima nama ini kerana dalam molekulnya terdapat hidrogen yang sedikit berasid. Hidrogen ini adalah yang terdapat dalam kumpulan -OH yang terletak betul -betul di sebelah kumpulan karbonil, yang merupakan sebahagian daripada karboksil yang tidak bertindak balas. Garam jenis ini dikenali sebagai garam asid, kerana ia tidak benar -benar neutral.
[TOC]
Struktur kimia

Formula
C6H4Coohcook = c8H5 KO4
Nomenclature
- Potassium bifthalate.
- Asid kalium phthalate.
- Potassium hydrogenofthalate.
Sifat
Ketumpatan
1,636 g/ml.
Jisim molar
204.22 g/mol.
Kelarutan
Air dan alkohol.
Takat lebur
295 ° C dengan penguraian.
Aspek
Putih -ke -putih pepejal.
Berat tertentu
1.64 gr/cm3.
Kajian derivatif kalium bifthalate
Pengukuran derichrographic telah menunjukkan bahawa penguraian kalium bifthalate bermula antara 190 ° C dan 200 ° C, dan penyediaan bukan hygroscopic boleh disediakan antara 100 ° C dan 150 ° C.
Penguraian diteruskan dalam tiga langkah, yang kelajuannya bergantung pada kadar peningkatan suhu: phthalate dipbotassium pertama kali terbentuk, anhidrida phtalic dan air dihapuskan.
Boleh melayani anda: kalsium klorida (CaCl2)Perubahan Entalpía juga boleh diperolehi daripada derivatif, ini menghasilkan maklumat mengenai mekanisme tambahan penguraian haba dan perubahan keadaan sampel.
Penggunaan dan aplikasi
Kompaun ini digunakan dalam kimia analisis dalam titrasi atau penilaian asid-asas sebagai corak utama untuk penyeragaman dalam penyediaan penyelesaian dari sebatian yang berbeza.
Penyeragaman asas (alkali = naOH)
Apabila menyediakan penyelesaian NaOH, ia tidak dapat dijamin bahawa kepekatan yang mana penyelesaiannya tetap betul; Ini kerana NaOH adalah bahan pepejal yang sangat hygroscopic (menyerap udara dari udara), dan untuk menimbangnya ia tetap dengan kelembapan, yang menjadikan jumlah bahan bukan yang paling optimum.
Setelah penyelesaian disediakan, perlu mengetahui dengan tepat apakah kepekatannya tetap.
Untuk ini, penyelesaian disediakan dengan phthalate asid kalium, yang merupakan corak utama (disebabkan oleh kestabilan yang tinggi); Beberapa titisan penunjuk asid fenolphthalein ditambah dan larutan NaOH sebagai tajuk ditambah sehingga warna merah jambu disimpan dalam larutan phthalate asid kalium.
Dengan data yang diperoleh, pengiraan yang berkaitan dibuat untuk mencari kepekatan sebenar NaOH.
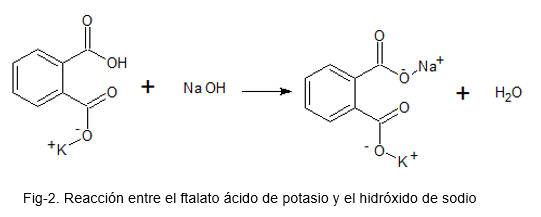
Imej berikut menggambarkan tindak balas kimia antara asid kalium phthalate dan natrium hidroksida.

Sebagai penyelesaian penampan dalam penentuan pH
Penyelesaian penampan atau penampan adalah yang dibentuk oleh garam asid dan asid, ini menyebabkan ia kekal dalam keadaan sedemikian rupa sehingga nilai pH tidak berubah apabila sejumlah kecil asid atau asas ditambah.
Boleh melayani anda: gravimetri: analisis gravimetrik, kaedah, kegunaan dan contohRisiko
- Pendedahan Kebakaran. Seperti kebanyakan pepejal organik, ada kemungkinan kebakaran pada suhu tinggi atau dengan bersentuhan dengan sumber pencucuhan mungkin berlaku.
- Debu halus yang tersebar di udara dalam kepekatan yang mencukupi, dan dengan kehadiran sumber pencucuhan, adalah potensi letupan habuk berbahaya.
- Ia adalah bahan yang stabil pada suhu bilik dan dalam keadaan penyimpanan yang mencukupi. Haba dan kelembapan yang berlebihan harus dielakkan.
- Ia boleh tidak serasi dengan oksidan yang kuat seperti asid nitrik.
- Penguraian boleh membentuk oksida karbon yang beracun.
Mengenai kesihatan
- Dengan pengambilan secara tidak sengaja, ia boleh menyebabkan muntah, cirit -birit dan kerengsaan dalam membran kerana keasidan mereka.
- Dengan penyedutan, ia menyebabkan kerengsaan di saluran udara dan batuk.
- Di kulit ia menyebabkan kerengsaan.
- Di mata ia menyebabkan kerengsaan, kemerahan dan kesakitan.
- Ia dianggap bahawa ia bukan bahan karsinogenik, teratogenik atau mutagenik.
Kecemasan dan pertolongan cemas
- Basuh mata dengan banyak air, keluarkan perlahan sekiranya membawa mereka dan membiarkan air berjalan melalui mata tanpa disentuh dengan tangan.
- Sekiranya ada hubungan dengan kulit, keluarkan pakaian dan kasut, basuh dengan banyak air dan basuh pakaian dengan baik sebelum menggunakan lagi.
- Sekiranya berlaku pengambilan, elakkan daripada menimbulkan muntah, minum air.
- Sekiranya penyedutan, ambil orang itu untuk bernafas udara segar; Sekiranya Nafas Sukar, Bekalan Oksigen.
- Dalam semua kes meminta bantuan perubatan segera.
- Sekiranya kebocoran atau tumpahan, kumpulkan produk di dalam bekas yang bersih dan cuba membuat habuk tidak bersurai.
Ia dapat melayani anda: apakah kesan negatif yang kita ada dengan kelarutan air?Langkah -langkah perlindungan peribadi
- Tinggal dari tempat minuman, makanan dan makanan disimpan (makanan haiwan kesayangan).
- Gunakan topeng anti habuk, neoprena atau sarung tangan PVC. Pada masa ini, sarung tangan nitril digunakan.
- Pakai pakaian yang mencukupi yang meliputi kebanyakan badan, termasuk kasut atau kasut yang dilindungi dan kasut.
- Pengudaraan ekzos tempatan disyorkan, dengan sistem pengekstrak udara, dengan mengambil kira arah angin yang utama.
- Produk ini boleh didapati di dalam air, ia tidak diserap di atas tanah, ia tidak boleh bioakumulable atau terbiodegradasi, ia tidak dijangka mempengaruhi kehidupan akuatik. Walau bagaimanapun, pada masa membuangnya, ia mesti dilakukan dengan bantuan kakitangan khusus: jangan buang dengan longkang.
- Simpan di kawasan oren/hijau, tempat kering dan berventilasi segar, dan dipisahkan dari bahan yang tidak serasi.
Rujukan
- Merck, (s.f), merckmillipore.com
- Chang R.,(1992), Kimia, (edisi keempat), Mexico, McGraw-Hill Inter-American dari Mexico S.A, dari C.V
- Reagen Kimia Meyer, (s.f), lembaran data keselamatan, kalium bifthalate, pulih dari, reagentsmeyer.com.mx
- Belcher, r.,Erdey, l.,Paulik, f.,Liptay.G.,(Julai 1960), Potassium Hydrogenophthatefthalate Fire, Scientedirect, Jilid 5, Isu 1, Halaman 53-57, org/10.1016/0039-9140 (60) 80205-6

