Struktur, sifat natrium borohidrida (NABH4)

- 4532
- 369
- Delbert Dare
Dia Natrium boron Ia adalah pepejal bukan organik yang formula kimianya adalah nabh4. Ia boleh dianggap wakil borohydruros alkali dan yang paling biasa dari ini. Ia adalah pepejal putih kristal.
Apabila bersentuhan dengan air, Nabh4 boleh menjana haba dan hidrogen h2 yang bahan bakar, jadi ia mesti dikendalikan dengan berhati -hati. Untuk kemudahan yang dapat menghasilkan ion hidrida h-, Natrium boron adalah sebatian yang agak rendah, jadi ia digunakan secara meluas dalam tindak balas kimia untuk tujuan ini.
 Natrium borohidrida, NABH4, pepejal. Ondřej Mangl [domain awam]. Sumber: Wikimedia Commons.
Natrium borohidrida, NABH4, pepejal. Ondřej Mangl [domain awam]. Sumber: Wikimedia Commons. Harta pengurangannya juga digunakan dalam industri kertas, kerana ia membolehkan untuk meningkatkan ciri -ciri kecerahan dan kestabilan pulpa dan kertas ketika bertindak terhadap pengoksidaan selulosa, komponen utama kertas.
Kerana di hadapan air, ia dapat dengan mudah membentuk hidrogen, kemungkinan menggunakannya sebagai sumber hidrogen yang boleh diterbalikkan dalam sel bahan bakar juga telah disiasat.
Ia mempunyai kegunaan lain berdasarkan harta pengurangannya, seperti dalam industri farmaseutikal.
[TOC]
Struktur
Natrium Boron adalah sebatian ionik. Ia dibentuk oleh anion borohydride [BH4]- Bersama -sama dengan natrium na+.
Anion [bh4]- Ia adalah tetrahedral.
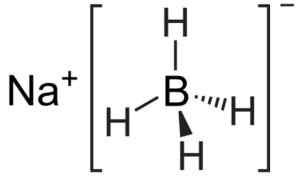 Struktur natrium borohidrida. Kemikungen [domain awam]. Sumber: Wikimedia Commons.
Struktur natrium borohidrida. Kemikungen [domain awam]. Sumber: Wikimedia Commons. Struktur Lewisnya adalah seperti berikut:
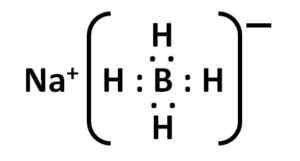 Struktur elektronik nabh lewis4. Pengarang: Marilú Stea.
Struktur elektronik nabh lewis4. Pengarang: Marilú Stea. Nomenclature
-Natrium boron
-Natrium tetrahydroate
-Natrium tetrahydrurorat
Ciri-ciri fizikal
Keadaan fizikal
Pepejal putih kristal.
Berat molekul
37.84 g/mol
Suhu sendiri
~ 220 ºC
Suhu penguraian
> 250 ºC
Ketumpatan
1,074 g/cm3 pada 20 ºC
Boleh melayani anda: Grignard Reagent: Penyediaan, Aplikasi, ContohKelarutan
NABH4 Ia agak larut dalam air (55 g/100ml pada 25 ° C), di mana sebahagiannya hidrolisis. Ia larut dalam tetrahydrofurano (THF) dan tidak larut dalam eter diik.
Sifat kimia
Natrium boron dibubarkan di dalam air, di mana ia mengalami penguraian awal atau hidrolisis yang menjadikan penyelesaian asas, yang menghalang hidrolisis berikutnya.
[Bh4]- + H2O → B (oh)3 + H2↑ + OH-
Ini dijelaskan kerana [bh4]- berinteraksi dengan h+ Air, di mana h+ Ambil Hidrida H Anion- Untuk membentuk h2. Boleh dikatakan bahawa BH3 bersaing dengan h+ Untuk hydride h-.
Dalam hidrolisis sederhana berasid selesai kerana kelimpahan ion h+.
NABH4 Ia stabil di udara kering. Tidak menentu.
Oleh kerana kandungan ion hidrida, natrium boron adalah sebatian pengurangan. Ia membolehkan untuk mengurangkan kumpulan karbonil C = o c-oh, iaitu, sebatian karbonil kepada alkohol.
NABH4 Dengan sendirinya ia tidak mengurangkan ikatan berganda c = c, bahkan konjugasi dengan kumpulan karbonil -c = c -c (= o)-.
Walau bagaimanapun, apabila bersentuhan dengan asid protonik (seperti HCl) atau asid Lewis (seperti BCL3 atau Alcl3) Diborano b terbentuk2H6. Dan jika tindak balas ini dijalankan dengan kehadiran sebatian organik dengan ikatan berganda c = c diborano b2H6 Melakukan hydrobacion ini.
Dengan kehadiran pemangkin yang sesuai dan keadaan tertentu natrium boron dapat mengurangkan pelbagai jenis kumpulan berfungsi.
Risiko
Panas tindak balas hidrolisis di dalam air sudah cukup untuk menghidupkan hidrogen yang terbentuk di dalamnya. Oleh itu, penting untuk berhati -hati apabila memanipulasinya.
NABH4 Ia mudah dihidupkan dan mudah dibakar.
Memperoleh
Reaksi penyediaan nabh biasa4 Ia melalui natrium hidrida nah dan b (och3)3 pada suhu kira -kira 250 ºC:
Ia boleh melayani anda: elektrolisis air4 nah + b (OCH3)3 → NABH4 + 3 naoch3
Aplikasi
Dalam tindak balas kimia pengurangan
Kerana menjadi sumber hones h-, NABH4 Ia adalah sebatian pengurangan dan digunakan untuk menyediakan sebatian kimia lain. Untuk melakukan ini, ia digunakan dalam pelarut kutub apratotik, iaitu, tanpa proton h+, seperti dimetilsulfoksida, hexamethylphosphoral dan dimetiloformamida.
Ia digunakan sebagai ejen pengurangan dalam tindak balas kimia organik dan bukan organik.
Ia membolehkan untuk mengurangkan aldehida ke alkohol utama dan keton ke alkohol sekunder.
Ia juga mengurangkan alkil halida kepada hidrokarbon seperti iododan ke Dekan.
Jika ia bertindak sendiri, apabila membuat pengurangan tidak menjejaskan kumpulan fungsi lain seperti ester, asid karboksilik, nitril dan sulfon.
Harta yang tidak mengurangkan ikatan ganda c = c, bahkan tidak konjugasi dengan kumpulan karbonil -c = c-c (= o)-, membolehkan anda menyediakan alkohol tak tepu -c = c-ch2-Oh.
Untuk mengurangkan sebatian aromatik nitrados ke anilin yang sepadan mereka memerlukan kehadiran pemangkin seperti kobalt klorida atau timah. Mengurangkan disulfida ke thioles.
Dengan kehadiran keadaan dan pemangkin yang sesuai ia membolehkan untuk mengurangkan asid karboksilik, ester, di tengah -tengah, nitril, imine, epoksida dan juga ikatan berganda dan triple.
Dalam h2 Dalam sel bahan bakar
NABH4 Ia boleh diubah menjadi sel bahan bakar.
NABH4 Dengan kehadiran larutan alkali KOH atau NaOH ia dihidrolisis dan menghasilkan hidrogen H2 yang boleh digunakan sebagai bahan bakar dalam bateri bahan api elektrolit polimer.
Ia juga telah disiasat sebagai bahan h untuk penyimpanan h h2 secara terbalik.
Nanopartikel NABH disintesis4 dan menstabilkan dengan surfaktan. Selepas rawatan dengan NICL2 Lapisan pelindung atau salutan dibentuk yang mengawal pembebasan h2 benar -benar terbalik.
Ia boleh melayani anda: perak nitrat (AgNO3): Struktur, sifat, kegunaan, ketoksikanBahan nanometrik baru ini akan membolehkan penggunaan h2 Sebagai bahan bakar yang bersih dan boleh diperbaharui dihasilkan.
 Kenderaan yang berfungsi dengan sel bahan api hidrogen. Dr. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)]. Sumber: Wikimedia Commons.
Kenderaan yang berfungsi dengan sel bahan api hidrogen. Dr. Artur Braun (Arturbraun) [CC BY-SA 4.0 (https: // creativeCommons.Org/lesen/by-sa/4.0)]. Sumber: Wikimedia Commons. Dalam industri pulpa dan kertas
Natrium boron digunakan untuk meningkatkan kecerahan dan sifat fizikal lain pulpa dan kertas.
Degradasi matriks selulosa kertas berlaku melalui proses kompleks yang melibatkan pengoksidaan. Kumpulan hidroksil mengoksidakan karbonil dan karboksil, ini membawa kepada perubahan warna kertas dan menurun sifat fizikal.
Semasa merawat pulpa atau kertas dengan NABH4, Ini mengurangkan aldehid dan keton kepada kumpulan -OH tanpa menjejaskan kumpulan karboksilik asid, meningkatkan kestabilan dan kecerahan kepada nilai yang lebih besar daripada inisial.
 NABH4 membolehkan meningkatkan kecerahan kertas. Pengarang: Rawpixel. Sumber: Pixabay.
NABH4 membolehkan meningkatkan kecerahan kertas. Pengarang: Rawpixel. Sumber: Pixabay. Dalam beberapa kegunaan
Natrium boron digunakan untuk merawat air kumbahan, sebagai ejen yang tidak betul dalam industri makanan dan minuman, sebagai ejen salutan dan untuk rawatan permukaan, dalam pengeluaran tembakau, di kulit industri farmaseutikal, tekstil dan tekstil.
Rujukan
- Kristian, m.L. dan Aguey-Zinsou, k.-F. (2012). Strategi shell teras yang membawa kepada kapasiti penyimpanan hidrogen yang boleh diterbalikkan tinggi untuk NABH4. ACS Nano 2012, 6, 9, 7739-7751. Pulih dari pub.ACS.org.
- Nora de Souza, m.V. dan alves v., T.R. (2006). Metodologi terkini yang dimediasi oleh natrium borohidrida dalam pengurangan kelas sebatian yang berlainan. Aplikasi. Organometal. Chem. 2006; 20: 798-810. Diperolehi dari perpustakaan dalam talian.Wiley.com.
- Imamoto, t. (1991). Pengurangan. Natrium borohydride. Dalam memahami sintesis organik. Pulih dari Scientedirect.com.
- Tang, l.C. (1986) Penstabilan kertas melalui rawatan natrium borohidrida. Dalam bahan tekstil dan kertas bersejarah. Bab 24. Halaman 427-441. Kemajuan dalam Kimia, Jilid 212. Pulih dari pub.ACS.org.
- Kapas, f. Albert dan Wilkinson, Geoffrey. (1980). Kimia bukan organik maju. Edisi keempat. John Wiley & Sons.
- Morrison, Robert Thornton; Dan Boyd, Robert Neilson. 1992. Kimia organik. Prentice-Hall. ISBN 81-203-0765-8.
- Atau.S. Perpustakaan Perubatan Negara. (2019). Natrium borohydride. Pulih dari: pubchem.NCBI.NLM.NIH.Gov.
- « Ciri -ciri dan contoh fenomena sosial
- Cobalt Chloride (COCL2 (Struktur, Nomenclature, Properties »

