Haba laten
- 3476
- 411
- Erick Krajcik
Apa itu haba terpendam?
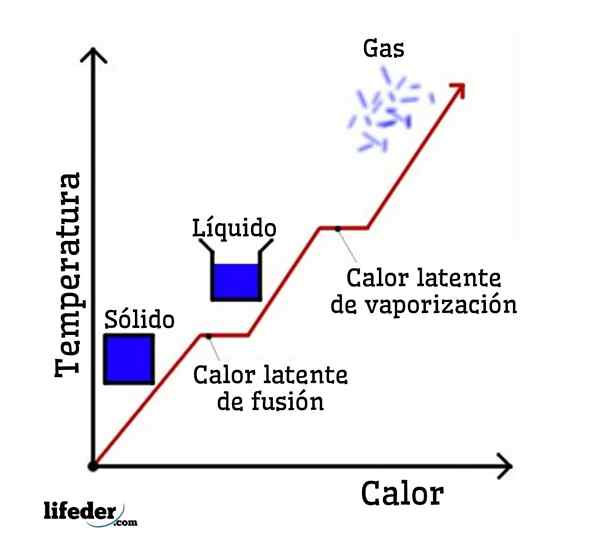
Panas laten adalah jumlah haba yang perlu diserap atau melepaskan bahan untuk mengubah keadaan fizikal atau fasa, mengekalkan suhu malar semasa proses itu. Haba yang dibekalkan atau dilepaskan tidak ditunjukkan, ia tidak "merasa" seperti biasa dalam variasi suhu; Oleh itu, istilah panas laten.
Kata laten berasal dari perkataan Latin "latenns" yang bermaksud tersembunyi, jadi haba laten berkelakuan seolah -olah tidak wujud apabila suhu tetap. Tetapi ada: apa yang berlaku ialah ia dimakan sepenuhnya dalam perubahan fasa atau keadaan fizikal.
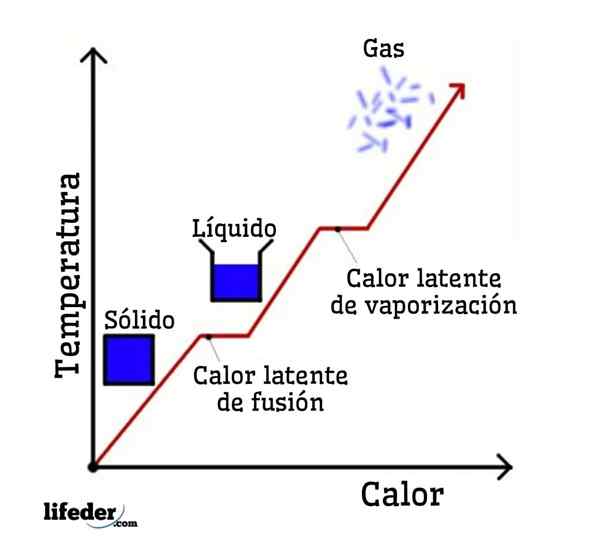
Jika air diambil sebagai contoh, perubahan fasa adalah seperti berikut: ais (pepejal) mencairkan air cecair (cecair) dalam proses yang dipanggil fusion; dan air cair pula menguap untuk berubah menjadi wap air (gas) ke dalam proses yang dipanggil pengewapan.
Sebaliknya, wap air disejukkan kepada air cair dalam proses yang dipanggil pemeluwapan; dan air cair menjadi ais lagi dalam proses yang disebut pemejalan.
Setiap perubahan fasa ini mempunyai haba laten yang berkaitan, yang boleh positif (penyerapan) atau negatif (pelepasan).
Panas lebur laten
 Perubahan dari pepejal ke cecair; Fusion
Perubahan dari pepejal ke cecair; Fusion Ia adalah jumlah haba yang mesti dibekalkan kepada jumlah bahan pepejal tertentu untuk mengubah keadaan fizikalnya dari pepejal hingga cecair. Semasa gabungan tidak ada perubahan suhu, jadi sementara pepejal ditubuhkan atau mencairkan cecair yang dihasilkan daripadanya mempunyai suhu yang sama dengan keseluruhan pepejal.
Umumnya, haba ini ditentukan di titik gabungan biasa, yang merupakan suhu di mana pepejal mula bergabung di bawah tekanan atmosfera. Pada suhu ini terdapat keseimbangan atau kehadiran serentak pada masa yang sama keadaan pepejal dan keadaan cair.
Boleh melayani anda: Pemboleh ubah kategori: Ciri dan contohKeadaan pepejal dicirikan oleh kehadiran struktur padat disebabkan oleh kewujudan ikatan kimia yang besar, yang memberikan ketegaran struktur. Untuk transformasi pepejal kepada cecair, interaksi ini mesti dipecahkan, jadi ia dimakan (menyerap) tenaga untuk tujuan itu.
Contoh biasa ialah apabila ais krim dimakan, dibentuk oleh air, gula dan bahan lain. Adalah biasa untuk memerhatikan bahawa ais krim, jika ia tidak dimakan dengan cepat, mula mencairkan, iaitu, untuk mencairkan. Ini berlaku apabila suhu ais krim mencapai titik lebur ais.
Contoh
Beberapa contoh pemanasan fusion laten yang dinyatakan dalam J/G akan disenaraikan; Iaitu, tenaga yang gram pepejal mesti diserap untuk mencairkan pada titik lebur:
-ICE 334.0
-380 aluminium.0
-Sulfur 38.1
-Tembaga 134.0
-Ethanol 104.0
-Mercury 11.8
-Emas 64.5
-Perak 80.3
-Memimpin 24.5
-Tungsten 184
Ais menyerap sangat panas bukan kerana interaksinya lebih kuat, tetapi kerana ia mampu menghilangkan haba antara kristalnya.
Haba laten pengewapan
Ia adalah jumlah haba yang menyerap sejumlah bahan untuk bergerak dari keadaan cecair ke keadaan gas di titik mendidih biasa. Iaitu, ia adalah haba yang cecair menyerap apabila ia mendidih dan menjadi gas tanpa peningkatan suhu.
Di pangkuan bendalir, molekul bahan dapat berinteraksi dengan pembentukan jambatan hidrogen dan untuk daya tarikan antara molekul. Untuk lulus bahan dari keadaan cair ke keadaan gas anda harus mengatasi daya ini, jadi anda perlu membekalkan haba.
Panas sensitif menjadi yang menyerap cecair hanya untuk meningkatkan suhunya, yang bergantung pada haba tertentu. Sementara.
Ia boleh melayani anda: lengkung penentukuran: Apa itu, bagaimana untuk melakukannya, contohnyaContoh
Berikut adalah contoh beberapa cecair dengan pemanasan pengewapan masing -masing yang dinyatakan semula dalam J/G:
-Asid asetik 402
-Acetone 518
-Air 2256
-Etil Alkohol 846
-Sulfur 1510
-Benzene 390
-Karbon dioksida 574
-Klorin 293
-Ether 377
-Glycerin 974
-Mercury 295
-Oksigen 214
Perhatikan haba terpendam air cair yang besar: 1 g air cair (kira -kira 1 ml) perlu menyerap 2256 j untuk menguap. Air cecair masih menghilangkan haba yang diterima lebih baik berbanding dengan ais.
Haba pemejalan laten
Ia adalah haba yang mesti melepaskan sejumlah bahan untuk bergerak dari keadaan cairnya ke keadaan pepejalnya pada titik pemejalan atau pembekuan. Sekali lagi, sehingga cecair tidak sepenuhnya menguatkan, suhu akan tetap malar.
Proses pemejalan adalah terbalik kepada proses penggabungan, jadi nilai -nilai haba laten pemejalan dan haba laten gabungan adalah sama, tetapi tanda -tanda bertentangan.
Molekul bahan dalam keadaan cecair bergerak dengan kebebasan kerana tenaga yang mereka ada. Oleh itu, untuk bergerak ke fasa pepejal molekul mesti melepaskan tenaga dalam bentuk haba, yang membolehkan interaksi yang lebih besar antara molekul bahan.
Interaksi antara molekul nikmat pembentukan ikatan kimia fasa pepejal. Contoh ini berlaku apabila air cair diletakkan di dalam bekas untuk pembentukan ais di dalam peti sejuk. Peti sejuk beku mengekstrak haba dari air cair dan dikuatkan untuk menjadi ais.
Contoh
Berikut adalah beberapa contoh pemanasan pemanasan laten (dalam j/g) untuk beberapa cecair:
Boleh melayani anda: lubang putih: sejarah, teori dan bagaimana ia terbentuk-Air (-334)
-Aluminium (-380)
-Sulfur (-38)
-Tembaga (-134)
-Etanol (-104)
Haba pemeluwapan laten
Ia adalah jumlah haba yang mesti dilepaskan atau dibebaskan dari jumlah bahan tertentu, untuk bergerak dari keadaan gas ke keadaan cecair. Gas yang dipendekkan dan cecair yang terbentuk mengekalkan suhu yang sama semasa pemeluwapan.
Pemeluwapan adalah proses yang bertentangan dengan pengewapan. Panas pemeluwapan laten mempunyai nilai yang sama dengan haba laten pengewapan, tetapi dengan tanda bertentangan, dan pada titik mendidih. Contohnya adalah apabila dimasak dan stim dipendekkan di bahagian dalam periuk.
Molekul Gaseous bergerak bebas didorong oleh tenaga yang mereka ada. Oleh itu, mereka mesti melepaskan tenaga untuk membolehkan interaksi intermolecular keadaan cecair ditubuhkan antara molekul bahan.
Secara semula jadi terdapat banyak contoh lain dari fenomena pemeluwapan air. Wap air naik di atmosfera dan memeluk dalam awan dalam bentuk titisan air.
Terdapat juga kehadiran titisan air di segelas kereta, produk pemeluwapan air disebabkan oleh penurunan suhu pada awal pagi, yang membentuk Rocío.
Contoh
Akhirnya, pemantauan pemeluwapan laten masing -masing dinyatakan sekali lagi, dalam J/G: akan disenaraikan untuk beberapa wap:
-Asid asetik (-402)
-Acetone (-518)
-Air (-2256)
-Etil alkohol (-846)
-Sulfur (-1510)
-Benzene (-390)
Rujukan
- Whitten, Davis, Peck & Stanley. (2008). Kimia. (8th ed.). Pembelajaran Cengage.
- Walter J. Moore. (1963). Kimia Fizikal. Dalam kinetik kimia. Edisi keempat, Longmans.
- Wikipedia. (2020). Haba laten. Diperoleh dari: dalam.Wikipedia.org
- Editor enyclopaedia Britannica. (2020). Haba laten. Pulih dari: Britannica.com
- Kotak Alat Kejuruteraan. (2003). Cecair: Panas laten penyejatan. Diperolehi dari: EngineeringToolbox.com
- Pembelajaran Lumen. (s.F.). Perubahan fasa dan haba yang menonjol. Pulih dari: kursus.Lumenning.com

