Struktur Asid Karbonat (H2CO3), sifat, sintesis, kegunaan

- 764
- 40
- Erick Krajcik
Dia asid karbonik Ia adalah sebatian bukan organik, walaupun ada orang -orang yang membahaskan bahawa ia sebenarnya organik, yang formula kimianya adalah h2Co3. Oleh itu, ia adalah asid diprotik, mampu mendermakan dua ion h+ ke persekitaran berair untuk menjana dua kation molekul h3Sama ada+. Dari dia ion bikarbonat yang terkenal (HCO3-) dan karbonat (CO32-).
Asid pelik ini, mudah, tetapi pada masa yang sama terlibat dalam sistem di mana banyak spesies mengambil bahagian dalam keseimbangan wap cecair, dibentuk dari dua molekul bukan organik asas: air dan karbon dioksida. Kehadiran co2 Unwound selalu diperhatikan bahawa terdapat gelembung di dalam air, naik ke permukaan.
 Kaca dengan air gas, salah satu minuman yang paling biasa yang mengandungi asid karbonik. Sumber: Pxhere.
Kaca dengan air gas, salah satu minuman yang paling biasa yang mengandungi asid karbonik. Sumber: Pxhere. Fenomena ini sering dilihat dalam minuman ringan dan air berkarbonat.
Dalam kes air berkarbonat atau gasfiified (imej unggul), jumlah tersebut telah dibubarkan2 bahawa tekanan stim anda lebih daripada tekanan atmosfera berganda. Dengan mengungkapnya, perbezaan tekanan di dalam botol dan luaran mengurangkan kelarutan CO2, Jadi gelembung yang akhirnya melarikan diri dari cecair muncul.
Ke tahap yang lebih rendah, perkara yang sama berlaku di mana -mana jisim air segar atau garam: apabila mereka memanaskan mereka, mereka akan melepaskan kandungan dibubarkan mereka2.
Walau bagaimanapun, CO2 Ia bukan sahaja dibubarkan, tetapi mengalami transformasi dalam molekulnya yang menjadikannya h2Co3; Asid yang mempunyai kehidupan yang sangat kecil, tetapi cukup untuk menandakan perubahan mesurable dalam pH persekitaran pelarut berair, dan juga menghasilkan sistem penampan karbonat yang unik.
[TOC]
Struktur
Molekul
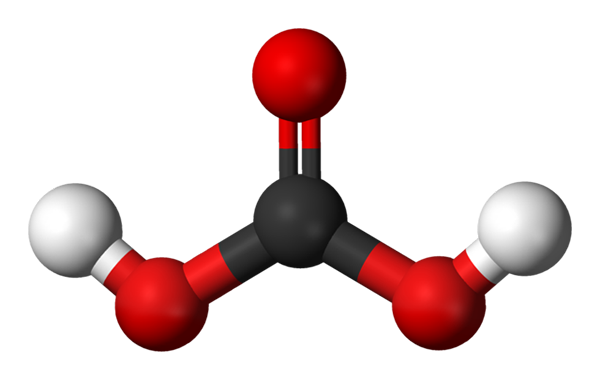 Molekul asid karbonik yang diwakili dengan model sfera dan bar. Sumber: Jynto dan Ben Mills melalui Wikipedia.
Molekul asid karbonik yang diwakili dengan model sfera dan bar. Sumber: Jynto dan Ben Mills melalui Wikipedia. Naik kita mempunyai molekul h2Co3, diwakili dengan sfera dan bar. Sfera merah sesuai dengan atom oksigen, hitam ke atom karbon, dan atom hidrogen putih.
Perhatikan bahawa bermula dari imej anda boleh menulis formula lain yang sah untuk asid ini: CO (OH)2, Di mana CO menjadi kumpulan karbonil, C = O, dikaitkan dengan dua kumpulan hidroksil, oh. Apabila terdapat dua kumpulan OH, mampu mendermakan atom hidrogen mereka, kini difahami dari mana asalnya+ Dikeluarkan di tengah.
 Struktur molekul asid karbonik.
Struktur molekul asid karbonik. Perhatikan bahawa Formula Co (OH)2 Ia boleh ditulis sebagai ohcooh; iaitu, jenis rcooh, di mana r menjadi dalam kes ini kumpulan OH.
Atas sebab ini, sebagai tambahan kepada fakta bahawa molekul terdiri daripada atom oksigen, hidrogen dan karbon, terlalu biasa dalam kimia organik, bahawa asid karbonik dianggap oleh sesetengahnya sebagai sebatian organik. Walau bagaimanapun, di bahagian sintesisnya akan dijelaskan mengapa orang lain menganggapnya sebagai sifat bukan organik dan bukan organik.
Boleh melayani anda: dihydroxyacetone: struktur, sifat, mendapatkan, menggunakanInteraksi molekul
Molekul h2Co3 Dapat dikomentari bahawa geometrinya adalah trigonal rata, dengan karbon terletak di tengah segitiga. Dalam dua simpulnya, ia mempunyai kumpulan OH, yang merupakan penderma jambatan hidrogen; Dan pada baki yang lain, atom oksigen kumpulan c = o, penerima jambatan hidrogen.
Oleh itu, h2Co3 Ia mempunyai kecenderungan yang kuat untuk berinteraksi dengan protik atau pelarut oksigen (dan juga nitrogen).
Dan secara kebetulan, air memenuhi kedua -dua ciri ini, dan pertalian h adalah seperti itu2Co3 untuknya yang hampir segera memberikannya h+ Dan keseimbangan hidrolisis yang melibatkan spesies HCO mula ditubuhkan3- dan h3Sama ada+.
Itulah sebabnya kehadiran air terurai asid karbonik dan menjadikan penebatnya sebagai sebatian murni terlalu rumit.
Asid karbonik tulen
Kembali ke molekul H2Co3, Bukan sahaja ia rata, mampu mewujudkan jambatan hidrogen, tetapi ia juga boleh membentangkan cis-trans isomeía; Ini, dalam imej kita mempunyai isomer cis, dengan dua h menunjuk ke arah yang sama, sementara di dalam isomer trans mereka akan menunjuk ke arah yang bertentangan.
Isomer cis adalah yang paling stabil dari kedua -duanya, dan itulah sebabnya ia adalah satu -satunya yang biasanya diwakili.
Pepejal tulen h2Co3 Ia terdiri daripada struktur kristal yang terdiri daripada lapisan atau molekul daun berinteraksi dengan jambatan hidrogen sampingan. Ini dijangkakan, sebagai molekul h2Co3 Rata dan segitiga. Apabila sublimal, senja kitaran muncul (h2Co3)2, yang disertai oleh dua jambatan hidrogen c = o - oh.
Simetri jam2Co3 Ia belum dapat ditakrifkan oleh saat -saat. Ia dianggap mengkristal sebagai dua polimorf: α-H2Co3 dan β- H2Co3. Walau bagaimanapun, α-H2Co3, disintesis berdasarkan campuran cho3COOH-CO2, Ia menunjukkan bahawa ia sebenarnya cho3Oroh: Ster asid karbonik monometri.
Sifat
Disebutkan bahawa h2Co3 Ia adalah asid diprotik, jadi anda boleh mendermakan dua ion h+ ke medium yang menerimanya. Apabila medium ini adalah air, persamaan pemisahan atau hidrolisisnya adalah:
H2Co3(Ac) + h2Atau (l) HCO3-(Ac) + h3Sama ada+(Ac) (ka1 = 2.5 × 10-4)
HCO3-(Ac) + h2Atau (l) co32-(Ac) + h3Sama ada+(Ac) (ka2 = 4.69 × 10-11)
HCO3- Ia adalah anion bikarbonat atau hidrogenokarbonat, dan CO32- Anion karbonat. Mereka juga menunjukkan pemalar keseimbangan masing -masing, KA1 dan ka2. Menjadi ka2 lima juta kali lebih kecil daripada ka1, Pembentukan dan kepekatan CO32- Mereka hina.
Jadi, walaupun ia adalah asid diprotik, h kedua+ Anda hampir tidak dapat melepaskannya. Walau bagaimanapun, kehadiran CO2 dibubarkan dalam kuantiti yang cukup untuk mengasingkan medium; Dalam kes ini, air, menurunkan nilai pH (di bawah 7).
Boleh melayani anda: gabunganBercakap mengenai asid karbonik secara praktikal merujuk kepada penyelesaian berair di mana spesies HCO mendominasi3- dan h3Sama ada+; Ia tidak dapat diasingkan oleh kaedah konvensional, kerana percubaan paling sedikit akan menggantikan keseimbangan kelarutan CO2 ke pembentukan gelembung yang akan melarikan diri dari air.
Sintesis
Pembubaran
Asid karbonik adalah salah satu sebatian yang paling mudah untuk disintesis. Sebagai? Kaedah yang paling mudah adalah untuk gelembung, dengan bantuan jerami atau sorbet, udara yang kami menghembus nafas dalam jumlah air. Kerana kita menghembus nafas pada Essence Co2, Gelembung ini di dalam air, melarutkan sebahagian kecil.
Apabila kita melakukan ini, tindak balas berikut berlaku:
Co2(g) + h2Atau (l) h2Co3(Ac)
Tetapi pada gilirannya, kelarutan CO mesti dipertimbangkan2 dalam air:
Co2(g) co2(Ac)
Kedua -dua co2 seperti h2Atau molekul bukan organik, jadi h2Co3 Tidak organik sejak titik ini dilihat.
Baki wap cecair
Akibatnya kita mempunyai sistem dalam keseimbangan yang sangat bergantung pada tekanan separa Co2, serta suhu cecair.
Contohnya, jika tekanan CO2 Ia meningkat (sekiranya kita meniup udara dengan lebih banyak daya melalui sorbet), lebih banyak h akan membentuk2Co3 dan pH akan menjadi lebih berasid; Oleh kerana, baki pertama bergerak ke kanan.
Sebaliknya, jika kita memanaskan pembubaran h2Co3, Kelarutan CO akan berkurang2 Di dalam air kerana ia adalah gas, dan keseimbangan kemudian akan bergerak ke kiri (akan ada kurang h2Co3). Serupa jika kita cuba memohon vakum: CO2 Ia akan melarikan diri serta molekul air, yang akan menggerakkan baki ke kiri lagi.
Pepejal tulen
Di atas membolehkan untuk mencapai kesimpulan: dari penyelesaian h2Co3 Tidak ada cara untuk mensintesis asid ini sebagai pepejal tulen melalui kaedah konvensional. Walau bagaimanapun, telah dilakukan, sejak 90 -an abad yang lalu, bermula dari campuran padat Co2 dan h2Sama ada.
Ke Campuran Pepejal ini2-H2Atau pada 50% ia dibombardir dengan proton (sejenis sinaran kosmik), sehingga kedua -dua komponen tidak akan melarikan diri dan pembentukan h berlaku2Co3. Untuk tujuan ini, campuran CHO juga telah digunakan3Oh-co2 (Ingat α-H2Co3).
Kaedah lain adalah melakukan perkara yang sama tetapi secara langsung menggunakan ais kering, tidak lebih.
Daripada tiga kaedah saintis NASA dapat mencapai kesimpulan: asid karbonik murni, pepejal atau gas, boleh wujud dalam ais krim Musytari, di glasier Martian, dan dalam komet, di mana campuran pepejal itu sentiasa disinari untuk sinar kosmik.
Boleh melayani anda: Pipet Volumetrik: Ciri, Kegunaan, Penentukuran dan KesalahanAplikasi
Asid karbonik itu sendiri adalah sebatian tanpa utiliti. Walau bagaimanapun, penyelesaiannya boleh menyediakan penyelesaian redaman berdasarkan rakan -rakan HCO3-/Co32- atau h2Co3/HCO3-.
Terima kasih kepada penyelesaian ini dan tindakan enzim anhydrase karbonik, yang terdapat dalam sel darah merah, CO2 Dihasilkan dalam pernafasan boleh diangkut dalam darah ke paru -paru, di mana ia akhirnya dilepaskan untuk dihembuskan di luar badan kita.
Bubjueo dari co2 Ia mengambil kesempatan daripada minum minuman sensasi yang menyenangkan dan ciri yang mereka tinggalkan di kerongkong mereka ketika meminumnya.
Juga, kehadiran h2Co3 Ia mempunyai kepentingan geologi dalam pembentukan stalaktit batu kapur, kerana ia melarutkan mereka perlahan -lahan sehingga mereka berasal dari kemasan mereka.
Dan sebaliknya, penyelesaian mereka boleh digunakan untuk menyediakan beberapa bikarbonat logam; Walaupun ia lebih menguntungkan dan mudah menggunakan garam bikarbonat (NAHCO3, Sebagai contoh).
Risiko
Asid karbonik mempunyai kehidupan yang sangat kecil dalam keadaan normal (mereka menganggarkan bahawa kira -kira 300 nanodetik), yang hampir tidak berbahaya kepada alam sekitar dan makhluk hidup. Walau bagaimanapun, seperti yang dinyatakan sebelum ini, itu tidak menyiratkan bahawa ia tidak dapat menghasilkan perubahan yang membimbangkan dalam pH air laut, yang mempengaruhi fauna laut.
Sebaliknya, "risiko" yang benar berada dalam pengambilan air yang dibasuh, kerana jumlah CO2 dibubarkan di dalamnya jauh lebih besar daripada air biasa. Walau bagaimanapun, dan sekali lagi, tidak ada kajian yang menunjukkan bahawa minum air gasified mewakili risiko yang mematikan; Sekiranya anda mencadangkannya untuk cepat dan memerangi pencernaan.
Satu -satunya kesan negatif yang diperhatikan pada mereka yang minum air ini adalah perasaan kenyang, kerana perut mereka dipenuhi dengan gas. Daripada ini (belum lagi minuman ringan, kerana ia terdiri daripada lebih daripada sekadar asid karbonik), boleh dikatakan bahawa sebatian ini tidak toksik sama sekali.
Rujukan
- Hari, r., & Underwood, a. (1989). Kimia Analisis Kuantitatif (ed kelima.). Pearson Prentice Hall.
- Shiver & Atkins. (2008). Kimia bukan organik. (Edisi Keempat). MC Graw Hill.
- Wikipedia. (2019). ASID KARBONIK. Diperoleh dari: dalam.Wikipedia.org
- Danielle Reid. (2019). Asid Karbonik: Pembentukan, Struktur & Video Persamaan Kimia. Kajian. Pulih dari: belajar.com
- Götz Bucher & Wolfram Sander. (2014). Menjelaskan struktur asid karbonik. Vol. 346, isu 6209, pp. 544-545. Doi: 10.1126/Sains.1260117
- Lynn Yarris. (22 Oktober 2014). Wawasan baru mengenai asid karbonik di dalam air. Berkeley Lab. Pulih dari: newscenter.lbl.Gov
- Claudia Hammond. (14 September 2015). Adakah air berkilauan sangat teruk untuk anda? Diperolehi dari: BBC.com
- Jürgen Bernard. (2014). Asid karbonik pepejal dan gas. Institut Kimia Fizikal. Universiti Innsbruck.
- « Undang -undang pemindahan haba, bentuk penghantaran, contoh
- 15 faedah epal untuk kesihatan fizikal dan mental »

